Clear Sky Science · it
Un modello fondamentale per il restauro multi-compito e cross-distribuzione delle immagini di microscopia a fluorescenza
Visioni più nitide del mondo cellulare nascosto
La biologia moderna si affida ai microscopi per osservare la vivace attività all'interno delle cellule, ma le immagini che otteniamo sono spesso granulose, sfocate o prive di dettagli fini. Questo articolo presenta FluoResFM, un nuovo modello di intelligenza artificiale (IA) progettato per ripulire e rendere più nitide le immagini di microscopia a fluorescenza in molti esperimenti diversi, tutto all'interno di un singolo sistema. Per gli scienziati significa immagini più chiare con meno tentativi ed errori; per i pazienti e il pubblico indica scoperte biologiche e approfondimenti medici più rapidi e affidabili basati su dati di qualità superiore.
Perché le immagini di microscopia sono così difficili da ottenere bene
I microscopi a fluorescenza rivelano proteine, membrane e organelli facendoli brillare, ma c'è un compromesso: usare luce delicata per proteggere le cellule viventi spesso produce immagini rumorose, deboli e sfocate. I ricercatori si sono rivolti all'apprendimento profondo per riparare queste immagini, addestrando reti neurali a rimuovere il rumore, correggere la sfocatura o aumentare la risoluzione usando coppie di immagini a bassa e alta qualità. Tuttavia, la maggior parte degli strumenti esistenti sono specialisti ristretti. Un modello può funzionare solo per denoising di una struttura particolare, un altro solo per affinare un certo tipo di microscopio. Quando un tale modello viene applicato a una nuova struttura o configurazione di imaging, può fallire gravemente, inventando dettagli falsi o distorcendo quelli reali — un problema serio quando gli scienziati si affidano a queste immagini per misure precise.
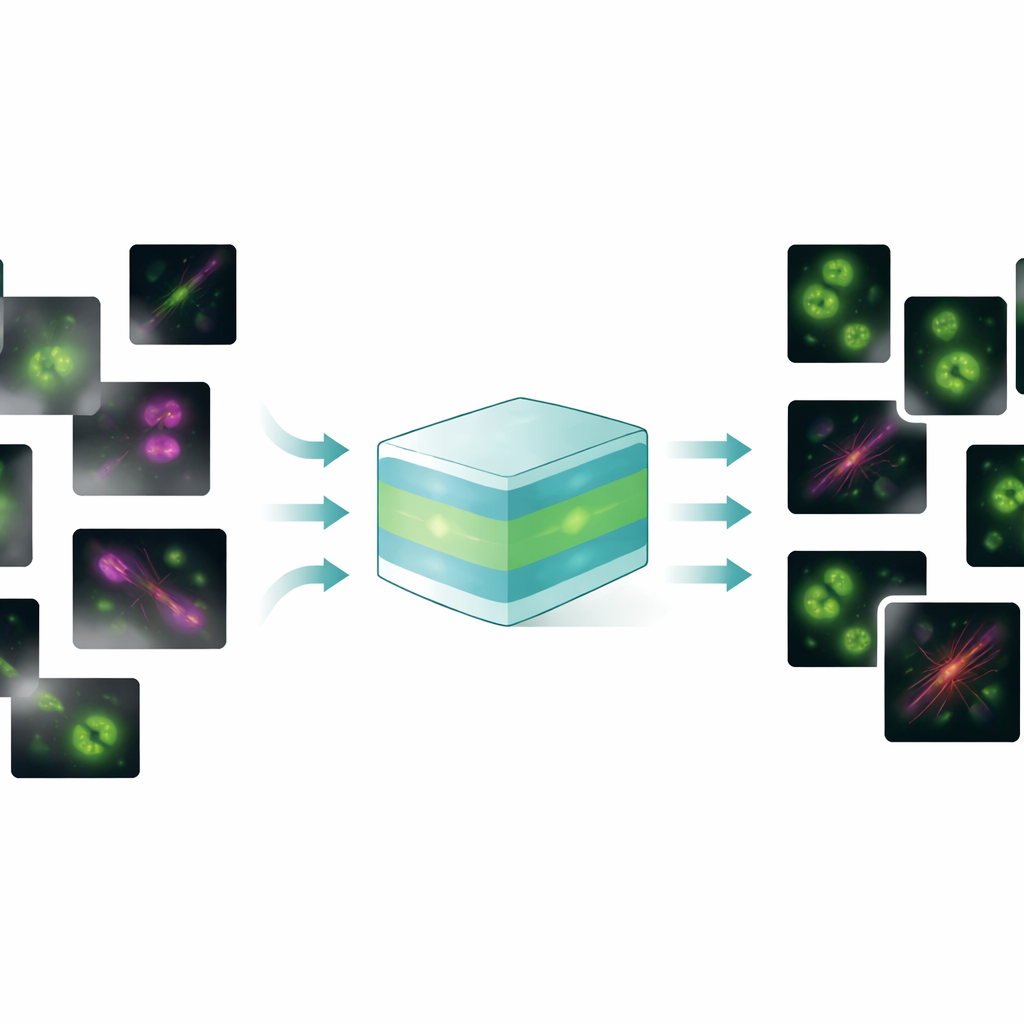
Un modello per affrontare molti problemi d'immagine
FluoResFM mira a essere un generalista: un modello fondamentale in grado di gestire diversi compiti di restauro — denoising, deblurring (deconvoluzione) e super-risoluzione — su molti tipi di strutture cellulari e microscopi in un unico quadro unificato. Gli autori lo hanno addestrato su oltre 4,3 milioni di patch d'immagine che coprono più di 20 strutture biologiche, da pozzi rivestiti di clatrina e microtubuli fino a nuclei, lisosomi e reticolo endoplasmatico, raccolte in una grande varietà di condizioni di imaging. Al suo nucleo, FluoResFM usa un'architettura in stile U‑Net, un design comune per l'elaborazione di immagini biomediche, ma è guidato da informazioni aggiuntive: brevi descrizioni testuali che codificano quale compito viene eseguito, quale struttura è presente e come sono state acquisite le immagini. Questi prompt testuali vengono convertiti in caratteristiche numeriche usando un modello linguaggio–visione biomedico pre-addestrato e poi fusi con le caratteristiche dell'immagine all'interno della rete tramite layer di attenzione. In pratica, al modello non viene detto solo “pulisci questa immagine” ma “rimuovi il rumore da un'immagine di microtubuli acquisita con questo tipo di microscopio verso questo tipo di riferimento”, il che lo aiuta a scegliere il tipo di correzione più appropriato.
Come la guida testuale migliora la qualità dell'immagine
Quando gli autori hanno confrontato FluoResFM con un precedente modello fondamentale di riferimento e con una versione dello stesso senza guida testuale, il modello consapevole del testo è risultato chiaramente superiore. Su centinaia di dataset interni e 51 dataset esterni mai visti prima, FluoResFM ha prodotto immagini più vicine ai riferimenti di alta qualità secondo molteplici misure di nitidezza, similarità ed errore. Si è dimostrato particolarmente abile nel risolvere caratteristiche ravvicinate come pori ad anello nell'involucro nucleare o reti di microtubuli aggrovigliate, evitando la tendenza a fondere insieme strutture vicine. I prompt testuali hanno anche fornito un potente meccanismo di indirizzamento. Cambiare la descrizione del compito da “denoising” a “super-risoluzione” (concettualmente) ha portato la stessa rete a eseguire operazioni molto diverse sulle stesse immagini in ingresso. Allo stesso modo, specificare il tipo di struttura sbagliato ha indotto il modello a ricostruire pattern fuorvianti, come trasformare una rete reticolare in macchie puntiformi, sottolineando sia la flessibilità del modello sia l'importanza di una conoscenza a priori corretta.
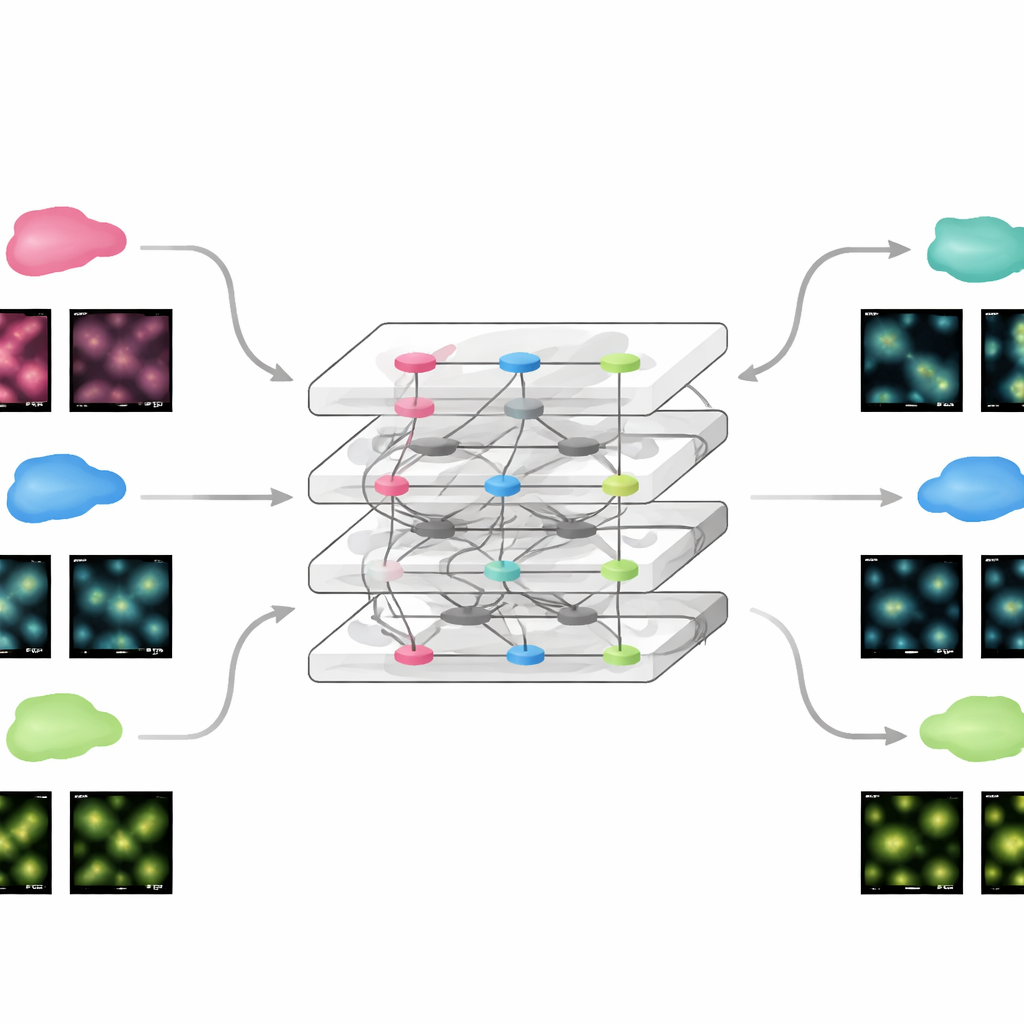
Adattarsi rapidamente a nuovi esperimenti
Poiché FluoResFM parte da una base ampia di esperienza, può essere messo a punto su nuovi dati usando sorprendentemente poche informazioni aggiuntive. Il team ha mostrato che aggiornando solo una piccola parte della rete con una singola immagine di esempio proveniente da un nuovo dataset, il modello raggiungeva prestazioni comparabili a quelle di reti profonde convenzionali addestrate da zero su centinaia di immagini. Questo valeva per immagini statiche e per filmati time‑lapse di strutture cellulari in movimento, dove il modello adattato migliorava sia la chiarezza sia la stabilità delle misurazioni nel tempo. La stessa strategia ha permesso di estendere FluoResFM oltre i compiti originali a nuove attività come il restauro volumetrico tridimensionale, proiezioni superficiali da 3D a 2D, uniformare la risoluzione lungo assi diversi e gestire fattori di ingrandimento maggiori. In tutti questi casi, il modello ha prodotto strutture più nitide e un migliore accordo quantitativo con i dati di riferimento.
Aiutare altri strumenti a vedere meglio le cellule
FluoResFM non è solo un modo per ottenere immagini esteticamente migliori; rafforza anche gli strumenti di analisi downstream che dipendono dalla qualità delle immagini. Quando gli autori hanno inserito le immagini restaurate in popolari programmi di segmentazione automatica usati per delineare nuclei, membrane e organelli, quegli strumenti hanno rilevato più oggetti, ne hanno perso di meno e hanno prodotto forme più coerenti con la verità di riferimento derivata da esperti. Questo miglioramento è stato osservato in dozzine di dataset che comprendevano molti tipi di cellule e strutture. Per abbassare la barriera d'uso quotidiano, il team ha confezionato FluoResFM come plugin per napari, un visualizzatore di immagini interattivo ampiamente usato, così che i biologi possano restaurare immagini e affinare il modello nei loro flussi di lavoro abituali senza dover scrivere codice.
Cosa significa questo per la microscopia futura
In termini semplici, questo lavoro dimostra che un singolo modello di IA guidato da testo può ripulire e rendere più nitide un'ampia gamma di immagini di microscopia a fluorescenza, adattarsi rapidamente a nuovi esperimenti e migliorare le prestazioni di altri strumenti di analisi. Intrecciando conoscenza su ciò che viene immaginato, come è stato acquisito e quale tipo di miglioramento si desidera, FluoResFM produce immagini più affidabili rispetto a reti specifiche per compito addestrate in isolamento. Con l'aggiunta di più dati e compiti, tali modelli fondamentali potrebbero diventare compagni standard dei microscopi, trasformando istantanee grezze e imperfette in finestre affidabili sull'architettura nascosta e sulla dinamica delle cellule viventi.
Citazione: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Parole chiave: microscopia a fluorescenza, restauro di immagini, apprendimento profondo, modelli fondamentali, imaging cellulare