Clear Sky Science · fr
Un modèle fondamental pour la restauration multi-tâche et inter-distributions des images de microscopie à fluorescence
Des vues plus nettes du monde cellulaire caché
La biologie moderne dépend des microscopes pour observer l’activité foisonnante à l’intérieur des cellules, mais les images que nous capturons sont souvent granuleuses, floues ou dépourvues de détails fins. Cet article présente FluoResFM, un nouveau modèle d’intelligence artificielle (IA) conçu pour nettoyer et affiner les images de microscopie à fluorescence à travers de nombreuses expériences, le tout au sein d’un seul système. Pour les scientifiques, cela signifie des images plus claires avec moins d’essais-erreurs ; pour les patients et le grand public, cela ouvre la voie à des découvertes biologiques et des insights médicaux plus rapides et plus fiables, fondés sur des données de meilleure qualité.
Pourquoi il est si difficile d’obtenir de bonnes images en microscopie
Les microscopes à fluorescence révèlent protéines, membranes et organites en les faisant briller, mais il y a un compromis : utiliser une lumière douce pour protéger les cellules vivantes produit souvent des images bruitées, peu lumineuses et floues. Les chercheurs ont recours à l’apprentissage profond pour réparer ces images, en entraînant des réseaux neuronaux à supprimer le bruit, inverser le flou ou augmenter la résolution à partir d’exemples d’images de mauvaise et de bonne qualité. Toutefois, la plupart des outils existants sont des spécialistes étroits. Un modèle peut fonctionner uniquement pour le débruitage d’une structure particulière, un autre uniquement pour le renforcement d’un type de microscope. Lorsqu’un tel modèle est appliqué à une nouvelle structure ou à un nouveau montage d’imagerie, il peut échouer spectaculairement, inventant de faux détails ou déformant des éléments réels — un problème sérieux quand les scientifiques s’appuient sur ces images pour des mesures précises.
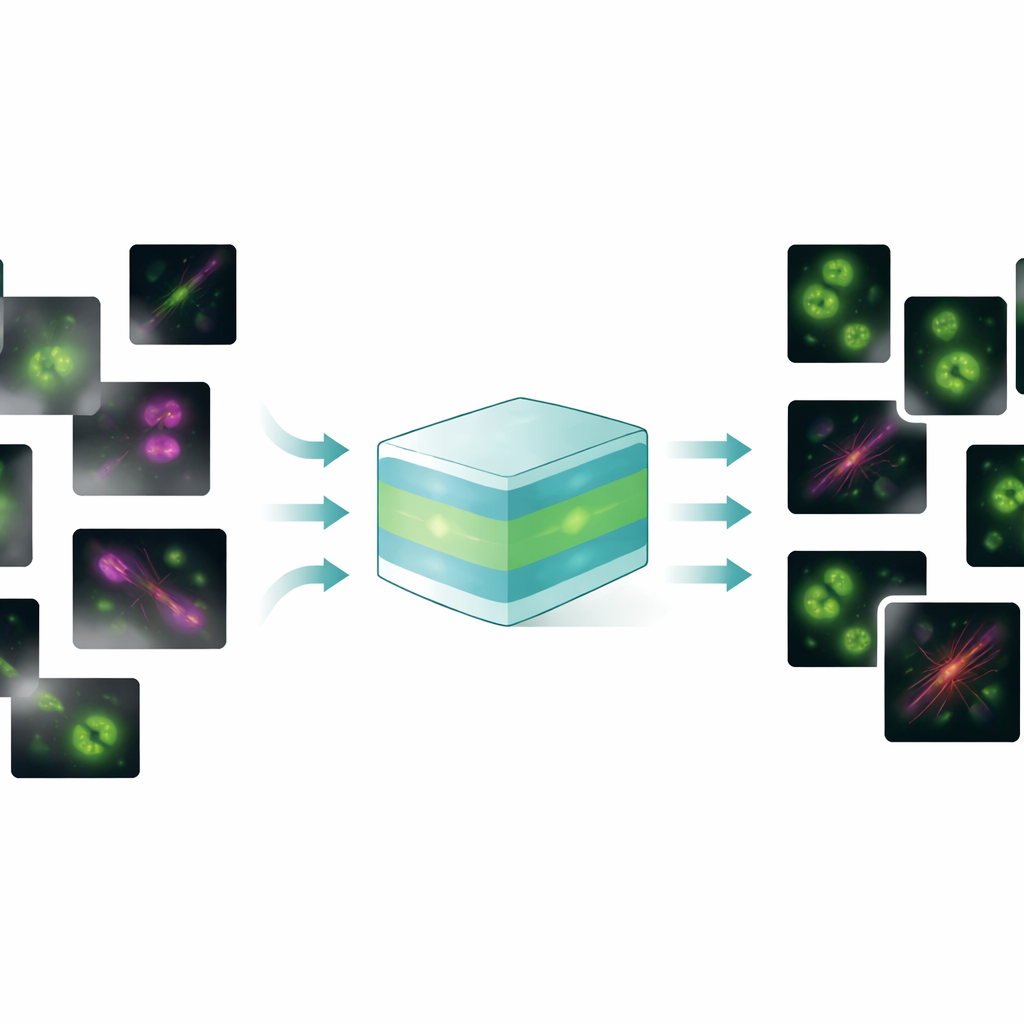
Un modèle pour traiter de nombreux problèmes d’image
FluoResFM vise à être un généraliste : un modèle fondamental capable de gérer plusieurs tâches de restauration — débruitage, déconvolution (défloutage) et super-résolution — pour de nombreux types de structures cellulaires et de microscopes au sein d’un cadre unifié. Les auteurs l’ont entraîné sur plus de 4,3 millions de patchs d’images couvrant plus de 20 structures biologiques, des puits recouverts de clathrine et des microtubules aux noyaux, lysosomes et réticulum endoplasmique, collectés dans une grande variété de conditions d’imagerie. Au cœur de FluoResFM se trouve une architecture de type U‑Net, une conception courante pour le traitement d’images biomédicales, mais elle est guidée par des informations supplémentaires : de courtes descriptions textuelles qui codent la tâche à accomplir, la structure présente et la manière dont les images ont été acquises. Ces invites textuelles sont converties en caractéristiques numériques à l’aide d’un modèle pré-entraîné bio-médical vision‑langage, puis fusionnées avec les caractéristiques d’image à l’intérieur du réseau via des couches d’attention. En pratique, le modèle se voit dire non seulement « nettoie cette image » mais « débruite une image de microtubules provenant de ce type de microscope vers ce type de cible », ce qui l’aide à choisir le bon type de correction.
Comment la guidance textuelle améliore la qualité d’image
Quand les auteurs ont comparé FluoResFM à un modèle fondamental antérieur de premier plan et à une version du même modèle sans guidance textuelle, la version avec texte l’emporte nettement. Sur des centaines de jeux de données internes et 51 jeux de données externes inédits, FluoResFM a produit des images plus proches des références de haute qualité selon plusieurs mesures de netteté, de similarité et d’erreur. Il était particulièrement performant pour résoudre des éléments proches les uns des autres, comme des pores annulaires dans l’enveloppe nucléaire ou des réseaux de microtubules entremêlés, et il évitait la tendance à amalgamer des structures voisines. Les invites textuelles ont aussi fourni un puissant mécanisme de pilotage. Changer la description de la tâche de « débruitage » à « super-résolution » a conduit le même réseau à effectuer des opérations très différentes sur des images d’entrée identiques. De même, spécifier un mauvais type de structure a poussé le modèle à reconstruire des motifs trompeurs, par exemple transformer un réseau réticulé en taches ponctuelles, soulignant à la fois la flexibilité du modèle et l’importance d’une connaissance a priori correcte.
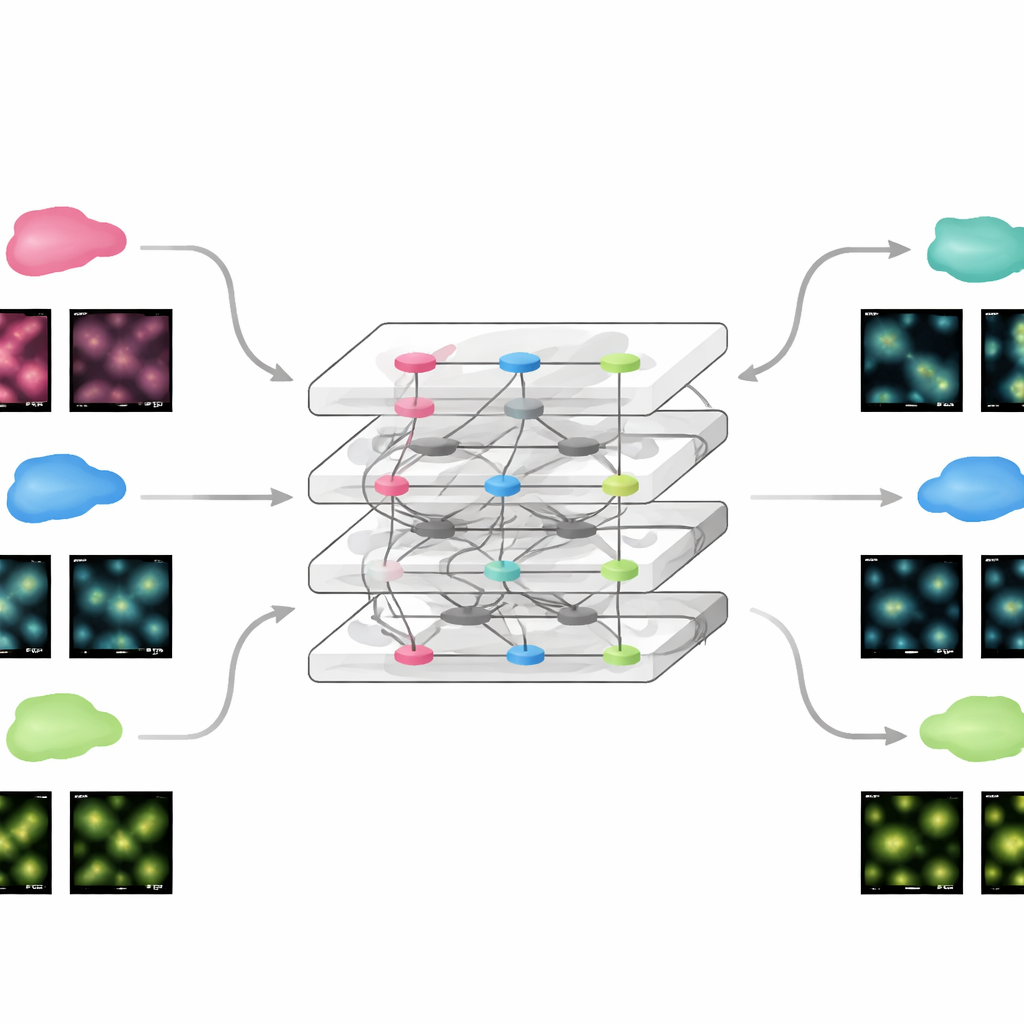
Une adaptation rapide à de nouvelles expériences
Parce que FluoResFM part d’une base d’expérience large, il peut être adapté à de nouvelles données en utilisant remarquablement peu d’informations supplémentaires. L’équipe a montré qu’en ne mettant à jour qu’une petite partie du réseau avec un seul exemple d’image provenant d’un nouveau jeu de données, le modèle atteignait des performances comparables à celles de réseaux profonds conventionnels entraînés depuis zéro sur des centaines d’images. Cela valait pour des images statiques comme pour des films en time-lapse de structures cellulaires en mouvement, où le modèle affiné améliorait à la fois la clarté et la stabilité des mesures dans le temps. La même stratégie a permis d’étendre FluoResFM au-delà de ses tâches d’entraînement initiales vers de nouvelles fonctions telles que la restauration volumique tridimensionnelle, les projections de surface de 3D vers 2D, l’uniformisation de la résolution selon différents axes et la gestion de facteurs d’agrandissement plus élevés. Dans tous ces cas, le modèle produisait des structures plus nettes et une meilleure concordance quantitative avec les données de référence.
Aider d’autres outils à mieux voir les cellules
FluoResFM n’est pas seulement un moyen d’obtenir de belles images ; il renforce aussi les outils d’analyse downstream qui dépendent de la qualité d’image. Lorsque les auteurs ont fourni les images restaurées à des programmes de segmentation automatisée populaires utilisés pour délimiter noyaux, membranes et organites, ces outils ont détecté plus d’objets, en ont manqué moins et ont produit des formes plus conformes aux vérités terrain établies par des experts. Cette amélioration a été observée sur des dizaines de jeux de données couvrant de nombreux types cellulaires et structures. Pour abaisser la barrière d’utilisation quotidienne, l’équipe a empaqueté FluoResFM sous forme de plugin pour napari, un visualiseur d’images interactif largement utilisé, afin que les biologistes puissent restaurer des images et affiner le modèle dans leurs flux de travail habituels sans avoir besoin d’écrire du code.
Ce que cela signifie pour la microscopie future
En termes simples, ce travail montre qu’un modèle d’IA unique guidé par du texte peut nettoyer et affiner une large gamme d’images de microscopie à fluorescence, s’adapter rapidement à de nouvelles expériences et améliorer les performances d’autres outils d’analyse. En tissant ensemble des connaissances sur ce qui est imagé, comment cela a été capturé et quel type d’amélioration est souhaité, FluoResFM produit des images plus fiables que des réseaux spécialisés entraînés isolément sur des tâches uniques. À mesure que davantage de données et de tâches seront ajoutées, de tels modèles fondamentaux pourraient devenir des compagnons standards des microscopes, transformant des instantanés bruts imparfaits en fenêtres fiables sur l’architecture cachée et la dynamique des cellules vivantes.
Citation: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Mots-clés: microscopie à fluorescence, restauration d'image, apprentissage profond, modèles fondamentaux, imagerie cellulaire