Clear Sky Science · nl
Een foundation-model voor multi-task herstel van fluorescentiemicroscopiebeelden over verschillende datasets
Scherpere blik op de verborgen wereld in cellen
Moderne biologie is afhankelijk van microscopen om het drukke leven binnen cellen te observeren, maar de beelden die we vastleggen zijn vaak korrelig, onscherp of missen fijne details. Dit artikel introduceert FluoResFM, een nieuw kunstmatig intelligentie (AI)-model dat is ontworpen om fluorescentiemicroscopiebeelden te reinigen en te verscherpen over vele verschillende experimenten, allemaal binnen één systeem. Voor wetenschappers betekent dit duidelijkere beelden met minder vallen en opstaan; voor patiënten en het publiek wijst het op snellere, betrouwbaardere biologische ontdekkingen en medische inzichten gebaseerd op data van hogere kwaliteit.
Waarom microscopiebeelden zo lastig goed te krijgen zijn
Fluorescentiemicroscopen tonen eiwitten, membranen en organellen door ze te laten gloeien, maar daar staat een afweging tegenover: het gebruik van zacht licht om levende cellen te beschermen levert vaak ruisige, zwakke en onscherpe beelden op. Onderzoekers hebben deep learning ingezet om deze beelden te herstellen, door neurale netwerken te leren ruis te verwijderen, onscherpte ongedaan te maken of resolutie te verhogen met voorbeelden van lage- en hoge-kwaliteit beeldparen. De meeste bestaande hulpmiddelen zijn echter smalle specialisten. Het ene model werkt mogelijk alleen voor het denoisen van een specifiek structuurtype, een ander alleen voor het verscherpen bij een bepaald microscooptype. Wanneer zo’n model op een nieuwe structuur of imaging-opstelling wordt toegepast, kan het sterk falen, nepdetails verzinnen of echte details vervormen — een ernstig probleem wanneer wetenschappers op deze beelden vertrouwen voor precieze metingen.
Één model voor veel beeldproblemen
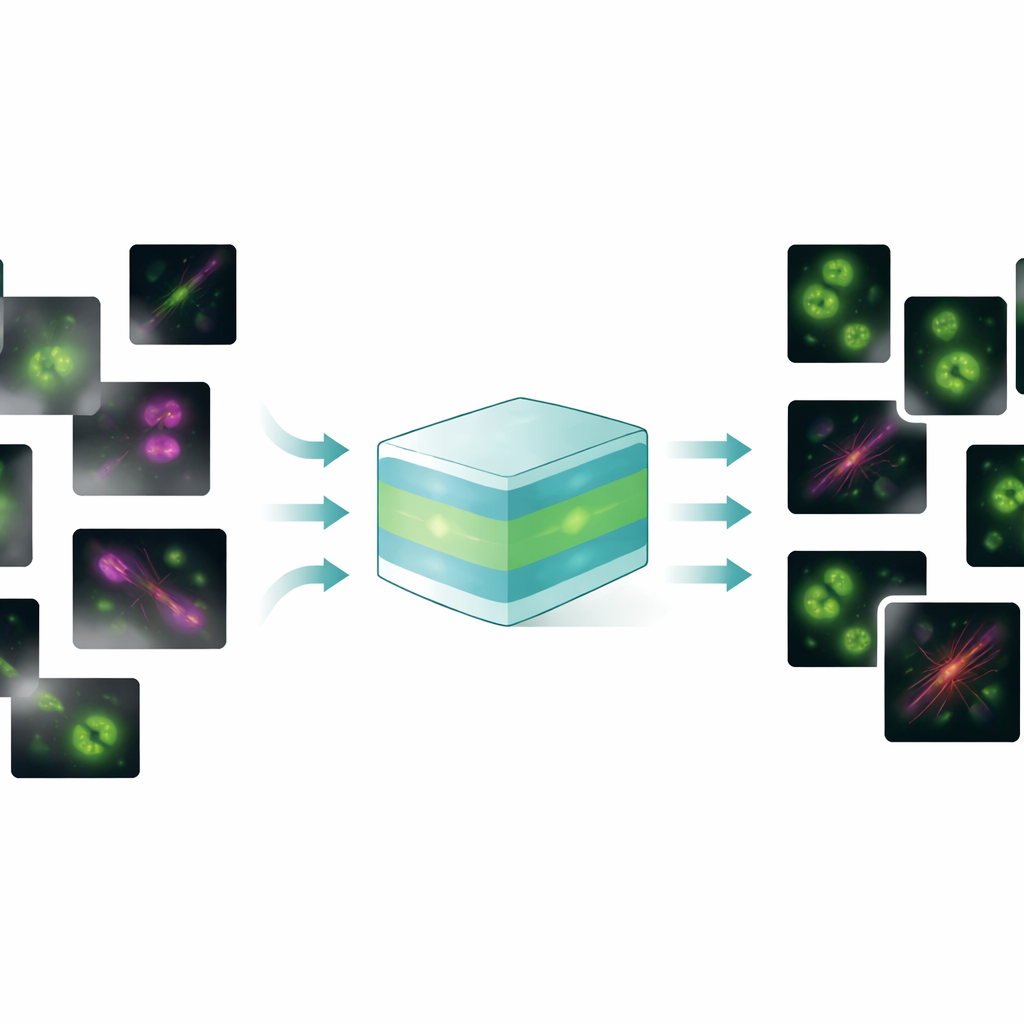
FluoResFM streeft ernaar een generalist te zijn: een foundation-model dat meerdere hersteltaken aankan—denoising, deblurring (deconvolutie) en super-resolutie—voor veel typen celstructuren en microscopen binnen één verenigd raamwerk. De auteurs trainden het op meer dan 4,3 miljoen beeldpatches die meer dan 20 biologische structuren omvatten, van clathrine-bedekte putjes en microtubuli tot kernen, lysosomen en het endoplasmatisch reticulum, verzameld onder een grote verscheidenheid aan beeldcondities. In de kern gebruikt FluoResFM een U‑Net-achtige architectuur, een veelgebruikt ontwerp voor biomedische beeldverwerking, maar het wordt gestuurd door extra informatie: korte tekstuele beschrijvingen die coderen welke taak wordt uitgevoerd, welke structuur aanwezig is en hoe de beelden zijn verkregen. Deze textprompts worden omgezet in numerieke features met een vooraf getraind biomedisch taal–visie model en vervolgens samengevoegd met beeldfeatures binnen het netwerk via attention-lagen. In wezen krijgt het model niet alleen te horen „reinig deze afbeelding” maar „denoise een microtubulusbeeld van dit soort microscoop richting dat soort referentie”, wat helpt de juiste correctie te kiezen.
Hoe tekstgeleiding de beeldkwaliteit verbetert
Toen de auteurs FluoResFM vergeleken met een toonaangevend eerder foundation-model en met een versie zonder tekstgeleiding, kwam het tekstbewuste model duidelijk als winnaar uit de bus. Over honderden interne datasets en 51 eerder ongeziene externe datasets produceerde FluoResFM beelden die dichter bij de hoogwaardige referenties lagen volgens meerdere maten voor scherpte, overeenstemming en fout. Het was bijzonder goed in het resolueren van dicht bij elkaar liggende structuren zoals ringvormige poriën in de kernmembraan of verwarde microtubuli-netwerken, en het vermeed de neiging naburige structuren samen te smeren. De tekstuele prompts boden ook een krachtig stuurmechanisme. Het veranderen van de taakomschrijving van „denoising” naar „super-resolutie” liet hetzelfde netwerk conceptueel heel verschillende bewerkingen uitvoeren op identieke invoerbeelden. Evenzo veroorzaakte het specificeren van het verkeerde structuurtype dat het model misleidende patronen reconstrueerde, zoals het veranderen van een reticulair netwerk in puntachtige vlekken, wat zowel de flexibiliteit van het model als het belang van correcte voorkennis onderstreept.
Snel aanpassen aan nieuwe experimenten
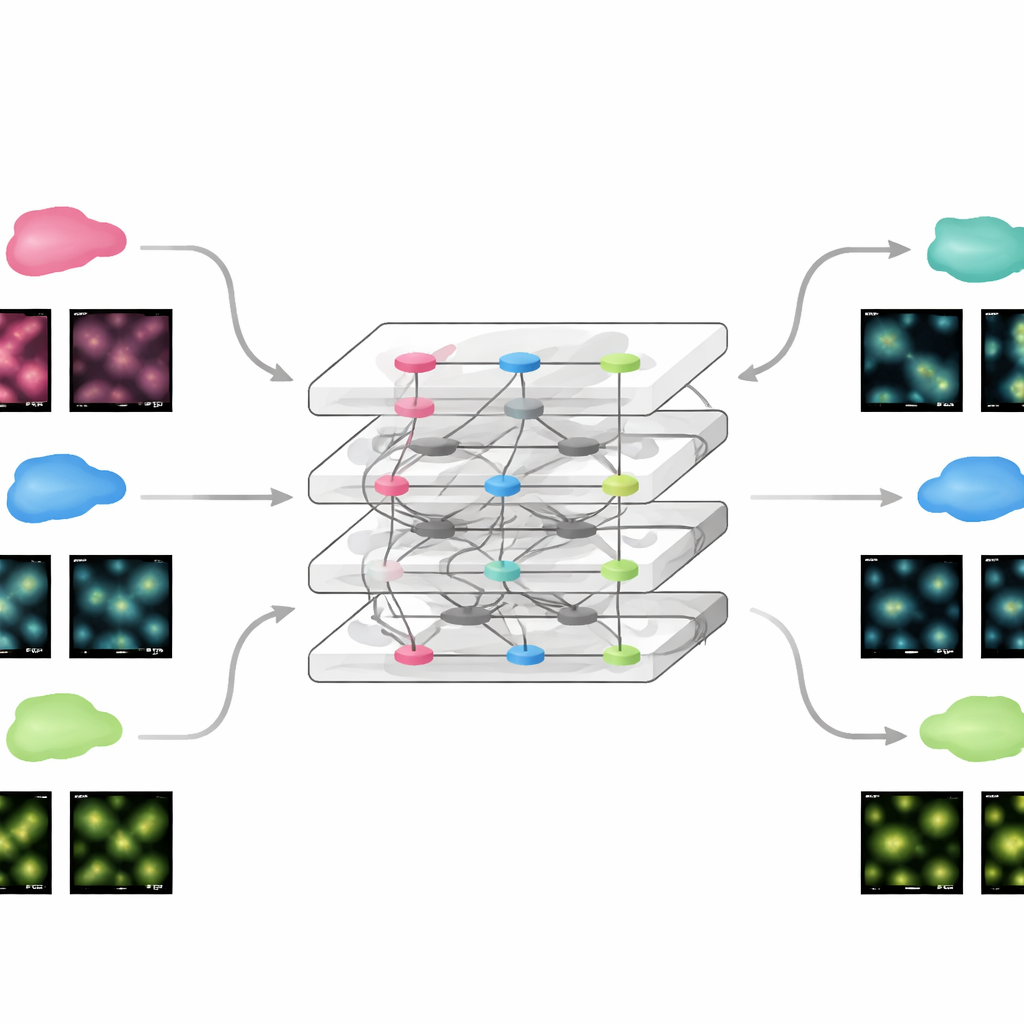
Omdat FluoResFM begint vanuit een brede basis van ervaring, kan het met opmerkelijk weinig aanvullende informatie op nieuwe data worden fijn-afgestemd. Het team toonde aan dat door slechts een klein deel van het netwerk bij te werken met één voorbeeldafbeelding uit een nieuwe dataset, het model prestaties bereikte vergelijkbaar met conventionele diepe netwerken die vanaf nul op honderden afbeeldingen werden getraind. Dit gold zowel voor statische beelden als voor time-lapse films van bewegende cellulaire structuren, waarbij het fijn-afgestelde model zowel de helderheid als de stabiliteit van metingen in de tijd verbeterde. Met dezelfde strategie kon FluoResFM worden uitgebreid buiten zijn oorspronkelijke trainingstaken naar nieuwe taken zoals driedimensionaal volumherstel, oppervlakteprojecties van 3D naar 2D, het egaliseren van resolutie langs verschillende assen, en het omgaan met hogere vergrotingsfactoren. In al deze gevallen produceerde het model duidelijkere structuren en betere kwantitatieve overeenstemming met referentiedata.
Andere tools helpen cellen helderder te zien
FluoResFM is niet alleen een manier om mooie plaatjes te maken; het versterkt ook downstream-analysetools die afhankelijk zijn van beeldkwaliteit. Wanneer de auteurs herstelde beelden invoerden in gangbare automatische segmentatieprogramma’s die worden gebruikt om kernen, membranen en organellen af te bakenen, detecteerden die tools meer objecten, misten er minder en leverden vormen op die beter overeenkwamen met door experts afgeleide grondwaarheid. Deze verbetering werd gezien over tientallen datasets met veel celtypen en structuren. Om de drempel voor dagelijks gebruik te verlagen, hebben de auteurs FluoResFM verpakt als een plugin voor napari, een veelgebruikt interactieve beeldviewer, zodat biologen beelden kunnen herstellen en het model kunnen fijn-afstemmen binnen hun gebruikelijke workflows zonder code te hoeven schrijven.
Wat dit betekent voor toekomstige microscopie
Simpel gezegd toont dit werk aan dat één enkel, tekst-gestuurd AI-model een breed scala aan fluorescentiemicroscopiebeelden kan reinigen en verscherpen, zich snel kan aanpassen aan nieuwe experimenten en de prestaties van andere analysetools kan verbeteren. Door kennis over wat wordt afgebeeld, hoe het is vastgelegd en welk soort verbetering gewenst is te verweven, produceert FluoResFM betrouwbaardere beelden dan taak-specifieke netwerken die geïsoleerd worden getraind. Naarmate meer data en taken worden toegevoegd, zouden dergelijke foundation-modellen standaardpartners van microscopen kunnen worden, waardoor onvolmaakte ruwe snapshots veranderen in betrouwbare vensters op de verborgen architectuur en dynamiek van levende cellen.
Bronvermelding: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Trefwoorden: fluorescentiemicroscopie, beeldherstel, deep learning, foundation-modellen, celafbeelding