Clear Sky Science · es
Un modelo base para la restauración multitarea y cruzada de distribuciones de imágenes de microscopía de fluorescencia
Vistas más nítidas del mundo celular oculto
La biología moderna depende de los microscopios para observar la vida bulliciosa dentro de las células, pero las imágenes que capturamos a menudo son granuladas, borrosas o carecen de detalles finos. Este artículo presenta FluoResFM, un nuevo modelo de inteligencia artificial (IA) diseñado para limpiar y agudizar imágenes de microscopía de fluorescencia en muchos experimentos diferentes, todo dentro de un único sistema. Para los científicos, esto significa imágenes más nítidas con menos ensayo y error; para los pacientes y el público, apunta hacia descubrimientos biológicos y hallazgos médicos más rápidos y fiables, basados en datos de mayor calidad.
Por qué las imágenes de microscopía son tan difíciles de obtener correctamente
Los microscopios de fluorescencia revelan proteínas, membranas y orgánulos haciéndolos brillar, pero hay una compensación: usar luz suave para proteger las células vivas a menudo produce imágenes ruidosas, tenues y borrosas. Los investigadores han recurrido al aprendizaje profundo para reparar estas imágenes, entrenando redes neuronales para eliminar ruido, deshacer el desenfoque o aumentar la resolución usando pares de ejemplos de baja y alta calidad. Sin embargo, la mayoría de las herramientas existentes son especialistas estrechos. Un modelo puede funcionar solo para desruido de una estructura particular, otro solo para enfocar un tipo concreto de microscopio. Cuando un modelo así se aplica a una estructura o configuración de imagen nueva, puede fallar estrepitosamente, inventando detalles falsos o distorsionando los reales —un problema serio cuando los científicos dependen de esas imágenes para mediciones precisas.
Un modelo para resolver muchos problemas de imagen
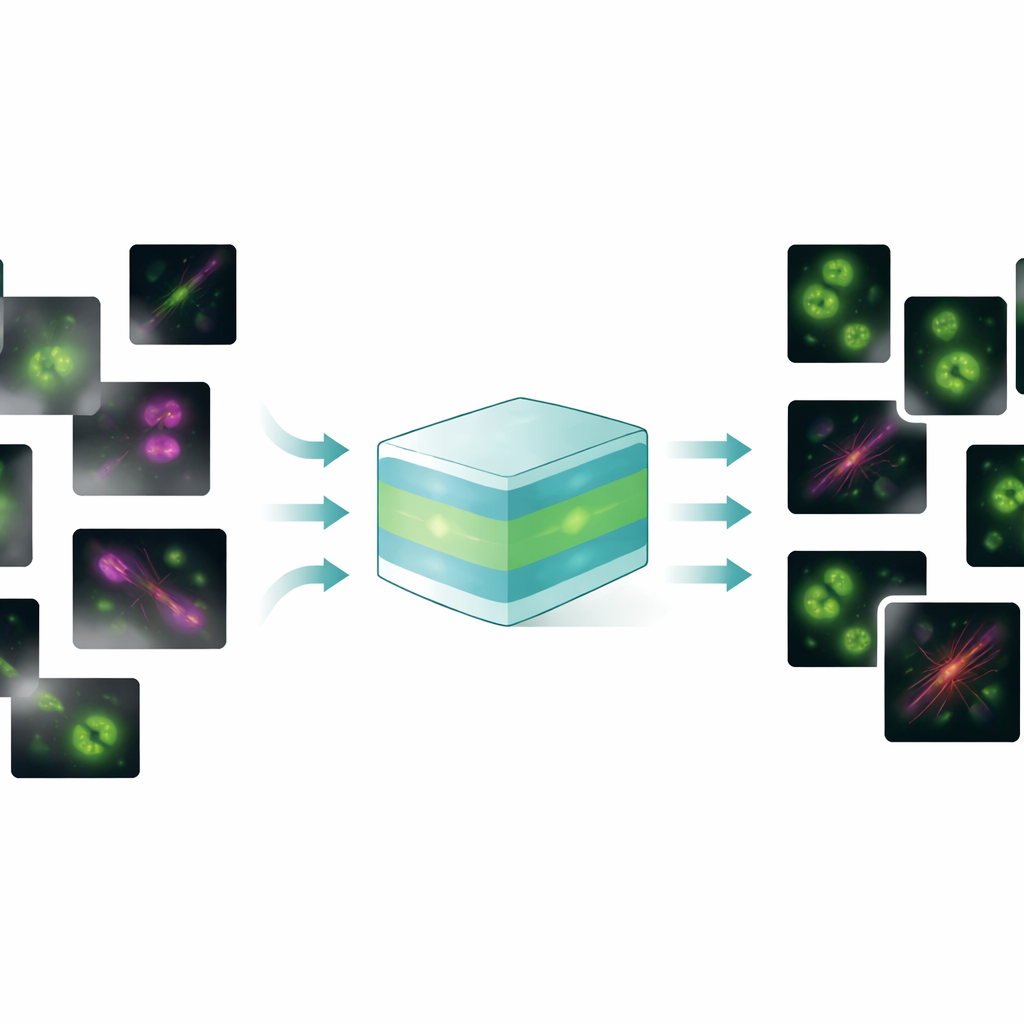
FluoResFM aspira a ser un generalista: un modelo base capaz de abordar varias tareas de restauración —desruido, desenfoque (deconvolución) y superresolución— en muchos tipos de estructuras celulares y microscopios dentro de un único marco unificado. Los autores lo entrenaron con más de 4,3 millones de parches de imagen que abarcan más de 20 estructuras biológicas, desde fosas recubiertas de clatrina y microtúbulos hasta núcleos, lisosomas y retículo endoplásmico, recogidos en una amplia variedad de condiciones de adquisición. En su núcleo, FluoResFM utiliza una arquitectura tipo U-Net, un diseño habitual para el procesamiento de imágenes biomédicas, pero está guiado por información adicional: descripciones textuales breves que codifican qué tarea se realiza, qué estructura está presente y cómo se adquirieron las imágenes. Estos indicios textuales se convierten en características numéricas mediante un modelo preentrenado biomédico de lenguaje y visión, y luego se fusionan con las características de la imagen dentro de la red a través de capas de atención. En efecto, al modelo no solo se le dice “limpia esta imagen”, sino “desruido para una imagen de microtúbulo de este tipo de microscopio hacia este tipo de objetivo”, lo que le ayuda a elegir el tipo de corrección adecuado.
Cómo la guía textual mejora la calidad de la imagen
Cuando los autores compararon FluoResFM con un destacado modelo base anterior y con una versión del propio modelo sin guía textual, el modelo consciente del texto claramente salió por delante. A lo largo de cientos de conjuntos de datos internos y 51 conjuntos de datos externos no vistos anteriormente, FluoResFM produjo imágenes más cercanas a las referencias de alta calidad según múltiples medidas de nitidez, similitud y error. Fue especialmente bueno resolviendo características muy próximas, como poros anulares en la envoltura nuclear o redes enredadas de microtúbulos, y evitó la tendencia a difuminar estructuras vecinas. Los indicios textuales también proporcionaron un potente mecanismo de direccionamiento. Cambiar la descripción de la tarea de “desruido” a “superresolución” (conceptualmente) llevó a la misma red a realizar operaciones muy distintas sobre imágenes de entrada idénticas. De forma similar, especificar el tipo de estructura equivocado hizo que el modelo reconstruyera patrones engañosos, como convertir una red reticular en puntos, subrayando tanto la flexibilidad del modelo como la importancia de un conocimiento previo correcto.
Adaptación rápida a nuevos experimentos
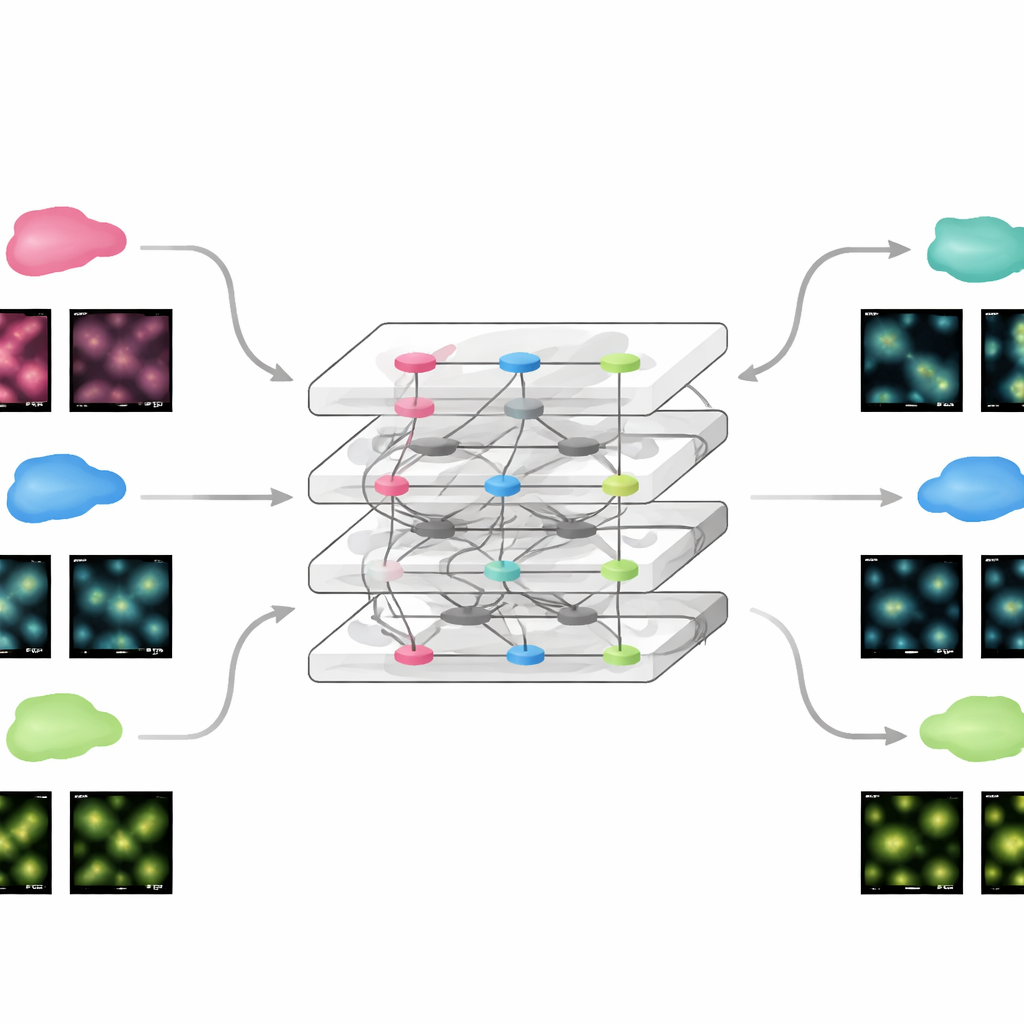
Puesto que FluoResFM parte de una base amplia de experiencia, puede ajustarse a nuevos datos usando una cantidad notablemente pequeña de información adicional. El equipo demostró que actualizando solo una pequeña parte de la red con un único ejemplo de imagen de un nuevo conjunto de datos, el modelo alcanzaba un rendimiento comparable al de redes profundas convencionales entrenadas desde cero con cientos de imágenes. Esto se mantuvo tanto para imágenes estáticas como para películas en lapso temporal de estructuras celulares en movimiento, donde el modelo afinado mejoró tanto la claridad como la estabilidad de las mediciones a lo largo del tiempo. La misma estrategia permitió extender FluoResFM más allá de sus tareas originales a otras nuevas, como restauración volumétrica tridimensional, proyecciones de superficie de 3D a 2D, homogeneizar la resolución a lo largo de distintos ejes y manejar factores de aumento mayores. En todos estos casos, el modelo produjo estructuras más claras y un mejor acuerdo cuantitativo con los datos de referencia.
Ayudar a otras herramientas a ver las células con mayor claridad
FluoResFM no es solo una forma de obtener imágenes estéticamente mejores; también fortalece las herramientas de análisis posteriores que dependen de la calidad de la imagen. Cuando los autores introdujeron imágenes restauradas en programas de segmentación automáticos populares usados para delimitar núcleos, membranas y orgánulos, esas herramientas detectaron más objetos, fallaron menos y produjeron formas que concordaban mejor con el dato de referencia elaborado por expertos. Esta mejora se observó en docenas de conjuntos de datos con muchos tipos de células y estructuras. Para bajar la barrera de uso diario, el equipo empaquetó FluoResFM como un complemento para napari, un visor de imágenes interactivo ampliamente utilizado, de modo que los biólogos puedan restaurar imágenes y afinar el modelo dentro de sus flujos de trabajo habituales sin necesidad de escribir código.
Qué significa esto para la microscopía futura
En términos simples, este trabajo muestra que un único modelo de IA guiado por texto puede limpiar y agudizar una amplia gama de imágenes de microscopía de fluorescencia, adaptarse rápidamente a nuevos experimentos y mejorar el rendimiento de otras herramientas de análisis. Al entrelazar conocimiento sobre qué se está imaginando, cómo se capturó y qué tipo de mejora se desea, FluoResFM produce imágenes más confiables que las redes específicas de tarea entrenadas de forma aislada. A medida que se añadan más datos y tareas, estos modelos base podrían convertirse en compañeros estándar de los microscopios, transformando instantáneas crudas imperfectas en ventanas fiables sobre la arquitectura oculta y la dinámica de las células vivas.
Cita: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Palabras clave: microscopía de fluorescencia, restauración de imágenes, aprendizaje profundo, modelos base, imágenes celulares