Clear Sky Science · sv
En grundmodell för flervals återställning över fördelningar av fluorescensmikroskopibilder
Tydligare vyer av den dolda cellvärlden
Modern biologi är beroende av mikroskop för att iaktta det livliga livet inne i cellerna, men bilderna vi fångar är ofta korniga, suddiga eller saknar fina detaljer. Denna artikel presenterar FluoResFM, en ny artificiell intelligens (AI)-modell avsedd att rengöra och skärpa fluorescensmikroskopibilder över många olika experiment, allt i ett enda system. För forskare innebär det tydligare bilder med mindre trial-and-error; för patienter och allmänheten pekar det mot snabbare, mer tillförlitliga biologiska upptäckter och medicinska insikter baserade på data av högre kvalitet.
Varför mikroskopibilder är så svåra att få rätt
Fluorescensmikroskop visar proteiner, membran och organeller genom att få dem att lysa, men det finns en kompromiss: att använda svagt ljus för att skydda levande celler ger ofta brusiga, mörka och suddiga bilder. Forskare har vänt sig till djupinlärning för att reparera dessa bilder, genom att lära neurala nätverk att ta bort brus, ångra oskärpa eller öka upplösningen med hjälp av exempelpar av låg- och högkvalitativa bilder. Men de flesta befintliga verktyg är smala specialister. En modell kanske bara fungerar för att avbrusa en viss struktur, en annan endast för att skärpa en viss mikroskoptyp. När en sådan modell tillämpas på en ny struktur eller avbildningskonfiguration kan den misslyckas kraftigt, uppfinna falska detaljer eller förvränga verkliga—ett allvarligt problem när forskare förlitar sig på dessa bilder för precisa mätningar.
En modell för många bildproblem
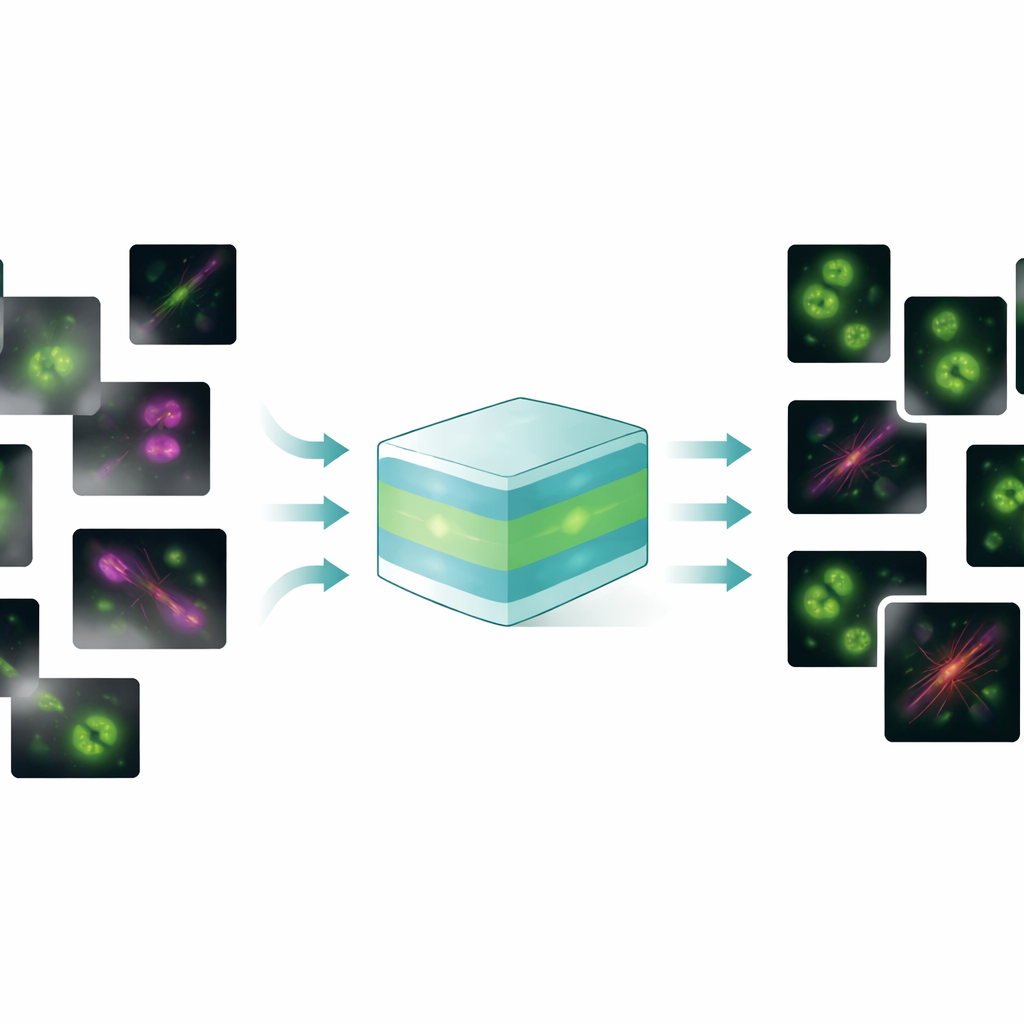
FluoResFM strävar efter att vara en generalist: en grundmodell som kan hantera flera återställningsuppgifter—avbrusning, avoskärpning (dekonvolution) och superupplösning—över många typer av cellstrukturer och mikroskop i en enda enhetlig ram. Författarna tränade den på mer än 4,3 miljoner bildlappar som täcker över 20 biologiska strukturer, från clathrin-belagda gropar och mikrotubuli till kärnor, lysosomer och endoplasmatiskt retikulum, insamlade under en mängd olika avbildningsförhållanden. I kärnan använder FluoResFM en U‑Net-liknande arkitektur, en vanlig design för biomedicinsk bildbehandling, men den styrs av extra information: korta textbeskrivningar som kodar vilken uppgift som utförs, vilken struktur som finns och hur bilderna togs. Dessa textpromptar omvandlas till numeriska funktioner med en förtränad biomedicinsk språk–visionsmodell och fusas sedan med bildfunktioner inne i nätverket via attentionlager. I praktiken får modellen alltså instruktionen inte bara "rengör den här bilden" utan "avbrusa en mikrotubuli-bild från den här typen av mikroskop mot den här typen av mål", vilket hjälper den att välja rätt sorts korrigering.
Hur textstyrning förbättrar bildkvaliteten
När författarna jämförde FluoResFM med en ledande tidigare grundmodell och med en version av sig själv utan textstyrning, framstod den textmedvetna modellen tydligt som bättre. Över hundratals interna dataset och 51 tidigare osedda externa dataset producerade FluoResFM bilder som låg närmare högkvalitativa referenser enligt flera mått på skärpa, likhet och fel. Den var särskilt bra på att upplösa tätt liggande strukturer som ringformiga porer i kärnmembranet eller intrasslade mikrotubulinät, och undvek tendensen att smeta ihop intilliggande strukturer. Textpromptarna gav också en kraftfull styrmekanism. Att ändra uppgiftsbeskrivningen från "avbrusning" till "superupplösning" (konceptuellt) ledde till att samma nätverk utförde mycket olika operationer på identiska ingångsbilder. På samma sätt orsakade specificering av fel strukturtyp att modellen rekonstruerade vilseledande mönster, som att förvandla ett retikulärt nätverk till punktliknande fläckar, vilket understryker både modellens flexibilitet och vikten av korrekt förkunskap.
Snabb anpassning till nya experiment
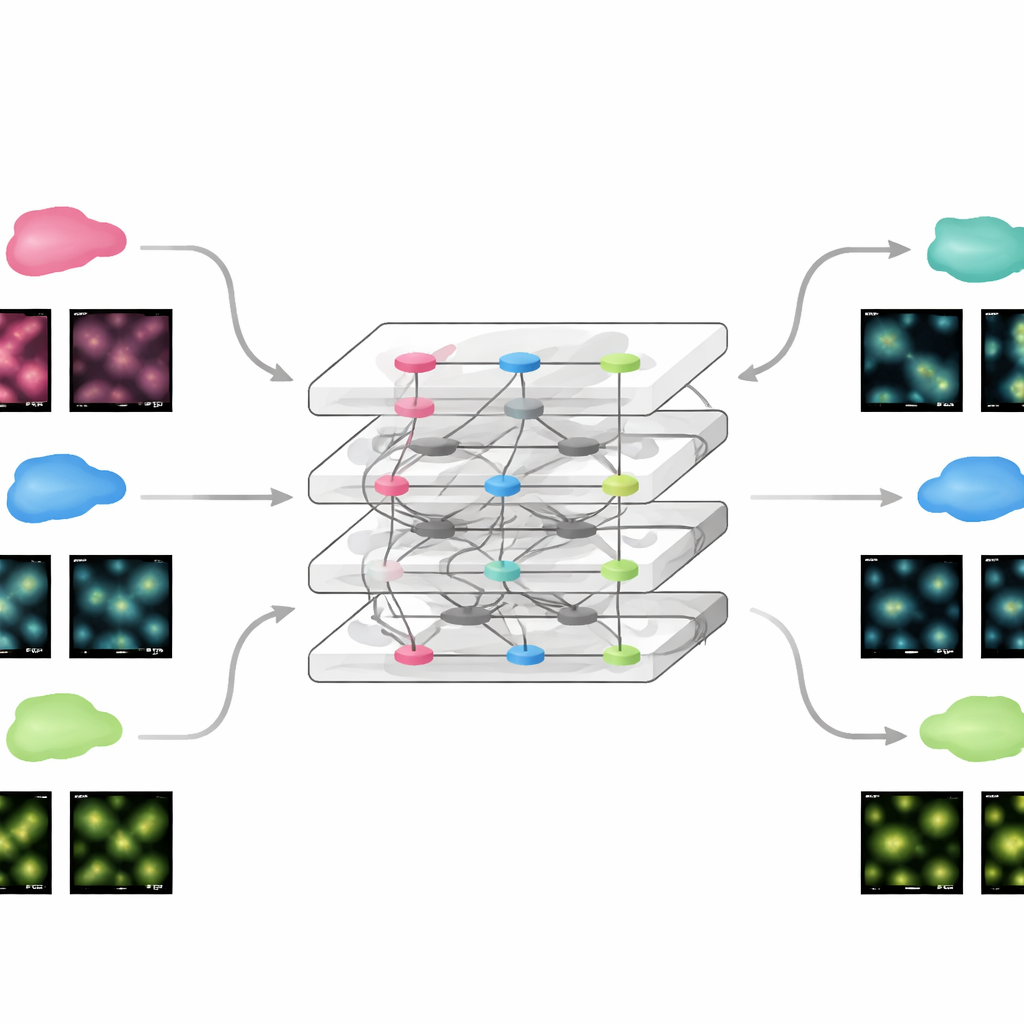
Eftersom FluoResFM börjar från en bred erfarenhetsbas kan den finjusteras till ny data med förvånansvärt lite ytterligare information. Teamet visade att genom att uppdatera endast en liten del av nätverket med en enda exempelbild från ett nytt dataset nådde modellen prestanda jämförbar med konventionella djupa nätverk tränade från grunden på hundratals bilder. Detta gällde både statiska bilder och tidsseriefilmer av rörliga cellstrukturer, där den finjusterade modellen förbättrade både tydlighet och stabiliteten i mätningarna över tid. Samma strategi gjorde det möjligt att utöka FluoResFM bortom dess ursprungliga träningsuppgifter till nya som tredimensionell volymåterställning, yprojektioner från 3D till 2D, att göra upplösningen mer jämn längs olika axlar och hantera högre förstoringstal. I samtliga fall producerade modellen tydligare strukturer och bättre kvantitativ överensstämmelse med referensdata.
Hjälper andra verktyg att se celler tydligare
FluoResFM är inte bara ett sätt att skapa snygga bilder; det stärker också efterföljande analysverktyg som är beroende av bildkvalitet. När författarna matade återställda bilder till populära automatiska segmenteringsprogram som används för att avgränsa kärnor, membran och organeller, upptäckte dessa verktyg fler objekt, missade färre och producerade former som stämde bättre överens med expertframställd referens. Denna förbättring sågs över flera dussin dataset med många celltyper och strukturer. För att sänka tröskeln för dagligt bruk paketerade teamet FluoResFM som ett plugin för napari, en allmänt använd interaktiv bildvisare, så att biologer kan återställa bilder och finjustera modellen inom sina vanliga arbetsflöden utan att behöva skriva kod.
Vad detta betyder för framtidens mikroskopi
Enkelt uttryckt visar detta arbete att en enda, textstyrd AI-modell kan rengöra och skärpa ett brett spektrum av fluorescensmikroskopibilder, anpassa sig snabbt till nya experiment och förbättra prestandan hos andra analysverktyg. Genom att väva samman kunskap om vad som avbildas, hur det fångades och vilken typ av förbättring som önskas, producerar FluoResFM mer pålitliga bilder än uppgiftsspecifika nätverk tränade isolerat. När fler data och uppgifter läggs till kan sådana grundmodeller bli standardföljare till mikroskop, som förvandlar ofullkomliga råbilder till tillförlitliga fönster mot levande cellers dolda arkitektur och dynamik.
Citering: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Nyckelord: fluorescensmikroskopi, bildåterställning, djupinlärning, grundmodeller, cellavbildning