Clear Sky Science · de
Ein Foundation-Modell zur multitasking- und distributionsübergreifenden Wiederherstellung von Fluoreszenzmikroskopie-Bildern
Schärfere Einblicke in die verborgene Welt der Zellen
Die moderne Biologie ist auf Mikroskope angewiesen, um das lebhafte Innenleben von Zellen zu beobachten, doch die aufgenommenen Bilder sind oft körnig, verschwommen oder es fehlen feine Details. Diese Arbeit stellt FluoResFM vor, ein neues Modell der künstlichen Intelligenz (KI), das entwickelt wurde, Fluoreszenzmikroskopie-Bilder über viele verschiedene Experimente hinweg in einem einzigen System zu bereinigen und zu schärfen. Für Wissenschaftler bedeutet das klarere Bilder mit weniger Trial-and-Error; für Patienten und die Öffentlichkeit kann es zu schnelleren, verlässlicheren biologischen Entdeckungen und medizinischen Erkenntnissen auf Basis hochwertigerer Daten führen.
Warum Mikroskopbilder so schwer korrekt zu erhalten sind
Fluoreszenzmikroskope machen Proteine, Membranen und Organellen sichtbar, indem sie sie zum Leuchten bringen, doch das hat seinen Preis: Um lebende Zellen zu schonen, wird oft schwaches Licht eingesetzt, was zu verrauschten, dunklen und unscharfen Bildern führt. Forschende nutzen Deep Learning, um diese Bilder zu reparieren, indem neuronale Netze aus Beispielen mit niedriger und hoher Qualität lernen, Rauschen zu entfernen, Unschärfen zu korrigieren oder die Auflösung zu erhöhen. Die meisten vorhandenen Werkzeuge sind jedoch enge Spezialisten: Ein Modell funktioniert möglicherweise nur für das Entrauschen einer bestimmten Struktur, ein anderes nur für das Schärfen eines speziellen Mikroskoptyps. Wird ein solches Modell auf eine neue Struktur oder ein anderes Aufnahme-Setup angewendet, kann es dramatisch versagen, indem es falsche Details erfindet oder echte verzerrt — ein graves Problem, wenn Wissenschaftler sich auf diese Bilder für präzise Messungen verlassen.
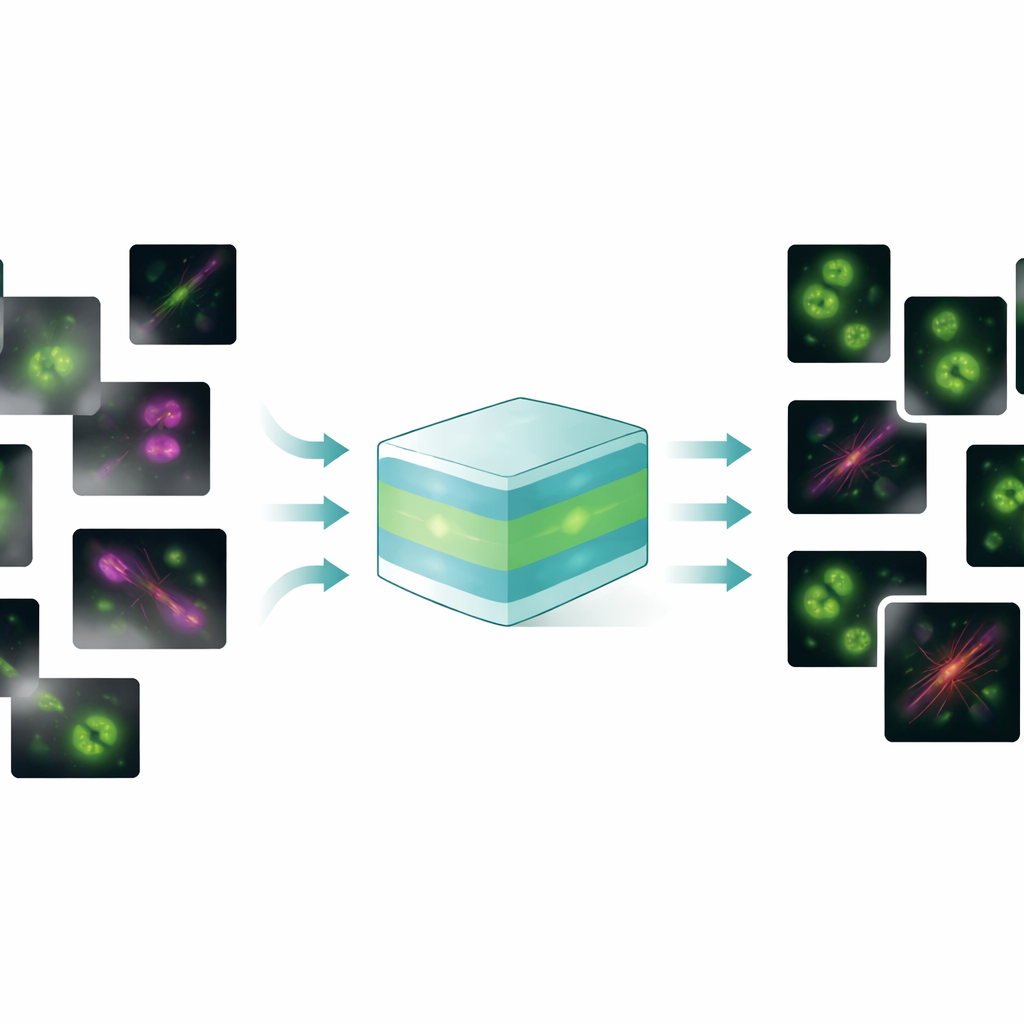
Ein Modell für viele Bildprobleme
FluoResFM zielt darauf ab, ein Generalist zu sein: ein Foundation-Modell, das mehrere Wiederherstellungsaufgaben — Entrauschen, Entschärfung (Deconvolution) und Super-Resolution — für viele Arten von Zellstrukturen und Mikroskopen in einem einzigen, einheitlichen Rahmen bewältigen kann. Die Autorinnen und Autoren trainierten es mit mehr als 4,3 Millionen Bildausschnitten, die über 20 biologische Strukturen abdecken, von clathrinbedeckten Gruben und Mikrotubuli bis hin zu Zellkernen, Lysosomen und endoplasmatischem Retikulum, gesammelt unter sehr unterschiedlichen Aufnahmebedingungen. Im Kern verwendet FluoResFM eine U‑Net-artige Architektur, ein verbreitetes Design in der biomedizinischen Bildverarbeitung, wird jedoch durch zusätzliche Informationen geleitet: kurze Textbeschreibungen, die codieren, welche Aufgabe ausgeführt wird, welche Struktur vorhanden ist und wie die Bilder aufgenommen wurden. Diese Textprompts werden mit einem vortrainierten biomedizinischen Sprach-Bild-Modell in numerische Merkmale umgewandelt und dann über Aufmerksamkeitslayer mit Bildmerkmalen im Netzwerk verschmolzen. Effektiv wird dem Modell nicht nur gesagt „bereinige dieses Bild“, sondern „entrausche ein Mikrotubuli-Bild von diesem Mikroskoptyp hin zu diesem Zieltyp“, was ihm hilft, die richtige Art der Korrektur zu wählen.
Wie Textsteuerung die Bildqualität verbessert
Als die Autorinnen und Autoren FluoResFM mit einem früheren führenden Foundation-Modell und mit einer Version ohne Textsteuerung verglichen, ging das textbewusste Modell klar als Sieger hervor. Über hunderte interne Datensätze und 51 zuvor ungesehene externe Datensätze erzeugte FluoResFM Bilder, die anhand mehrerer Maße für Schärfe, Ähnlichkeit und Fehler näher an den hochqualitativen Referenzen lagen. Besonders gut war es darin, dicht beieinander liegende Strukturen zu trennen, wie ringförmige Poren in der Kernhülle oder verfilzte Mikrotubuli-Netzwerke, und es vermied das Verschmieren benachbarter Strukturen. Die textuellen Prompts lieferten zudem einen starken Steuermechanismus: Durch die Änderung der Aufgabenbeschreibung von „Entrauschen“ zu „Super-Resolution“ führte dasselbe Netzwerk konzeptionell sehr unterschiedliche Operationen auf identischen Eingabebildern aus. Ebenso führte die Angabe des falschen Strukturtyps dazu, dass das Modell irreführende Muster rekonstruierte, etwa ein netzartiges Gebilde in punktartige Flecken zu verwandeln, was sowohl die Flexibilität des Modells als auch die Bedeutung korrekter Vorinformationen unterstreicht.
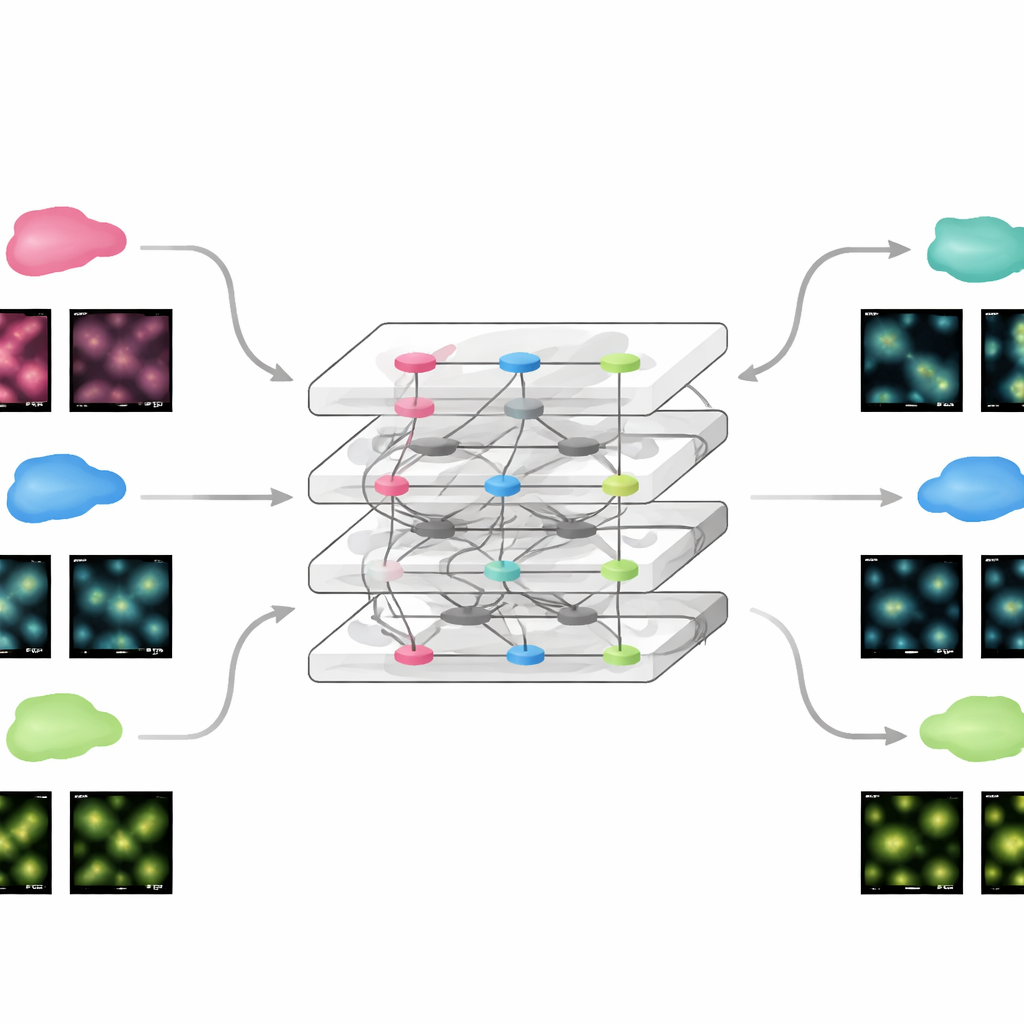
Schnelle Anpassung an neue Experimente
Weil FluoResFM auf einer breiten Erfahrungsgrundlage startet, lässt es sich mit erstaunlich wenig zusätzlicher Information an neue Daten feinabstimmen. Das Team zeigte, dass durch Aktualisierung nur eines kleinen Teils des Netzwerks mit einem einzigen Beispielbild aus einem neuen Datensatz das Modell Leistungen erreichte, die mit konventionellen Deep-Netzwerken vergleichbar waren, die von Grund auf mit Hunderten Bildern trainiert wurden. Dies galt sowohl für statische Bilder als auch für Zeitrafferfilme bewegter zellulärer Strukturen, bei denen das feinabgestimmte Modell sowohl die Klarheit als auch die Stabilität von Messungen über die Zeit verbessertes. Mit derselben Strategie ließ sich FluoResFM über die ursprünglichen Trainingsaufgaben hinaus auf neue Aufgaben erweitern, etwa die Wiederherstellung dreidimensionaler Volumina, Projektionsabbildungen von 3D nach 2D, Angleichung der Auflösung entlang verschiedener Achsen und das Handling höherer Vergrößerungsfaktoren. In all diesen Fällen produzierte das Modell klarere Strukturen und bessere quantitative Übereinstimmung mit Referenzdaten.
Andere Werkzeuge dabei unterstützen, Zellen klarer zu sehen
FluoResFM ist nicht nur ein Mittel, hübsche Bilder zu erzeugen; es stärkt auch nachgelagerte Analysewerkzeuge, die von Bildqualität abhängen. Wenn die Autorinnen und Autoren wiederhergestellte Bilder in populäre automatisierte Segmentierungsprogramme einspeisten, die Zellkerne, Membranen und Organellen umreißen, entdeckten diese Werkzeuge mehr Objekte, verfehlten weniger und erzeugten Formen, die besser mit von Experten erstelltem Ground Truth übereinstimmten. Diese Verbesserung zeigte sich über Dutzende Datensätze mit vielen Zelltypen und Strukturen. Um die Nutzung im Alltag zu erleichtern, stellten die Forschenden FluoResFM als Plugin für napari bereit, einen weit verbreiteten interaktiven Bildbetrachter, sodass Biologinnen und Biologen Bilder restaurieren und das Modell innerhalb ihrer gewohnten Workflows feinabstimmen können, ohne Code schreiben zu müssen.
Was das für die zukünftige Mikroskopie bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass ein einziges, textgelenktes KI-Modell eine breite Palette von Fluoreszenzmikroskopie-Bildern bereinigen und schärfen, sich schnell an neue Experimente anpassen und die Leistung anderer Analysewerkzeuge steigern kann. Indem es Wissen darüber verbindet, was abgebildet wird, wie es erfasst wurde und welche Art von Verbesserung gewünscht ist, erzeugt FluoResFM vertrauenswürdigere Bilder als aufgabenspezifische Netzwerke, die isoliert trainiert wurden. Mit zunehmender Menge an Daten und Aufgaben könnten solche Foundation-Modelle zu standardmäßigen Begleitern von Mikroskopen werden und unvollkommene Rohaufnahmen in verlässliche Fenster auf die verborgene Architektur und Dynamik lebender Zellen verwandeln.
Zitation: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Schlüsselwörter: Fluoreszenzmikroskopie, Bildwiederherstellung, Deep Learning, Foundation-Modelle, Zellbildgebung