Clear Sky Science · pl
Model podstawowy do wielozadaniowej rekonstrukcji obrazów mikroskopii fluorescencyjnej między dystrybucjami
Bardziej wyraźne spojrzenia na ukryty świat komórek
Współczesna biologia opiera się na mikroskopach, by obserwować tętniące życiem wnętrze komórek, ale obrazy, które pozyskujemy, często są ziarniste, rozmyte lub pozbawione drobnych detali. W artykule zaprezentowano FluoResFM, nowy model sztucznej inteligencji (AI) zaprojektowany do oczyszczania i wyostrzania obrazów mikroskopii fluorescencyjnej w wielu różnych eksperymentach, w ramach jednego systemu. Dla naukowców oznacza to wyraźniejsze obrazy przy mniejszej liczbie prób i błędów; dla pacjentów i społeczeństwa — szybsze i bardziej wiarygodne odkrycia biologiczne oraz wnioski medyczne oparte na danych wyższej jakości.
Dlaczego obrazy mikroskopowe są tak trudne do uzyskania
Mikroskopy fluorescencyjne uwidaczniają białka, błony i organelle przez ich świecenie, ale istnieje kompromis: używanie łagodnego światła w celu ochrony żywych komórek często skutkuje zaszumionymi, ciemnymi i rozmytymi obrazami. Naukowcy zwrócili się ku uczeniu głębokiemu, aby naprawiać takie obrazy — ucząc sieci neuronowe usuwać szum, odwracać rozmycie czy poprawiać rozdzielczość na podstawie par obrazów niskiej i wysokiej jakości. Jednak większość dostępnych narzędzi to wąscy specjaliści. Jeden model może działać jedynie do odszumiania konkretnej struktury, inny tylko do wyostrzania dla określonego typu mikroskopu. Gdy taki model zostanie zastosowany do nowej struktury lub innego ustawienia obrazowania, może zawieść — wymyślając fałszywe szczegóły lub zniekształcając prawdziwe — co jest poważnym problemem, gdy naukowcy polegają na tych obrazach przy precyzyjnych pomiarach.
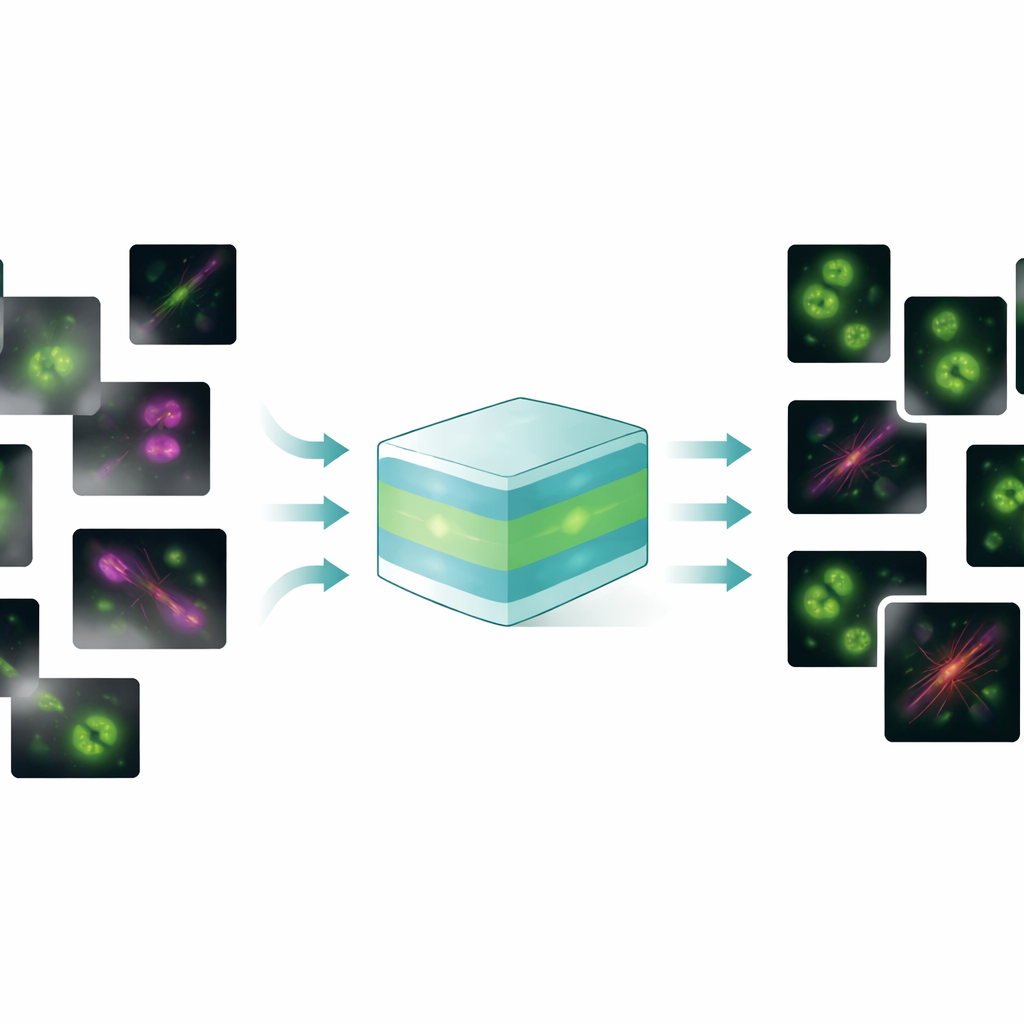
Jeden model do wielu problemów obrazowych
FluoResFM ma być generalistą: modelem podstawowym zdolnym do wykonywania różnych zadań rekonstrukcyjnych — odszumiania, odtwarzania ostrości (dekonwolucji) i super-rozdzielczości — dla wielu typów struktur komórkowych i mikroskopów w jednym zunifikowanym systemie. Autorzy trenowali go na ponad 4,3 miliona łatkach obrazów obejmujących ponad 20 struktur biologicznych, od zagłębień pokrytych klatryniną i mikrotubul po jądra, lizosomy i siateczkę śródplazmatyczną, zebranych w rozmaitych warunkach obrazowania. W rdzeniu FluoResFM wykorzystuje architekturę w stylu U‑Net, powszechne rozwiązanie w przetwarzaniu obrazów biomedycznych, ale jest ona kierowana dodatkowymi informacjami: krótkimi opisami tekstowymi, które kodują wykonywane zadanie, obecność danej struktury i sposób pozyskania obrazów. Te tekstowe wskazówki konwertowane są na cechy numeryczne za pomocą wstępnie wytrenowanego modelu łączącego język i wizję w dziedzinie biomedycznej, a następnie łączone z cechami obrazowymi w sieci przez warstwy uwagi. W praktyce modelowi mówi się nie tylko „oczyszcz ten obraz”, lecz „odszum obraz mikrotubuli z tego typu mikroskopu w kierunku takiego celu”, co pomaga mu dobrać właściwy rodzaj korekcji.
Jak wskazówki tekstowe poprawiają jakość obrazów
Gdy autorzy porównali FluoResFM z czołowym wcześniejszym modelem podstawowym i z wersją bez wskazówek tekstowych, model z uwzględnieniem tekstu wyraźnie wyszedł na prowadzenie. Na setkach wewnętrznych zestawów danych i 51 wcześniej nieznanych zewnętrznych zbiorach, FluoResFM generował obrazy bliższe wysokiej jakości odniesieniom według wielu miar ostrości, podobieństwa i błędu. Szczególnie dobrze radził sobie z rozdzielaniem blisko położonych struktur, takich jak pierścieniowe otwory w otoczce jądrowej czy splątane sieci mikrotubul, i unikał skłonności do zlewania sąsiednich struktur. Tekstowe podpowiedzi dawały też potężny mechanizm sterowania. Zmiana opisu zadania z „odszumiania” na „super-rozdzielczość” (koncepcyjnie) powodowała, że ta sama sieć wykonywała zupełnie inne operacje na identycznych obrazach wejściowych. Podobnie, określenie niewłaściwego typu struktury sprawiało, że model rekonstruował mylące wzorce — na przykład przekształcając siateczkową sieć w kropkowate plamki — co podkreśla zarówno elastyczność modelu, jak i znaczenie poprawnej wiedzy uprzedniej.
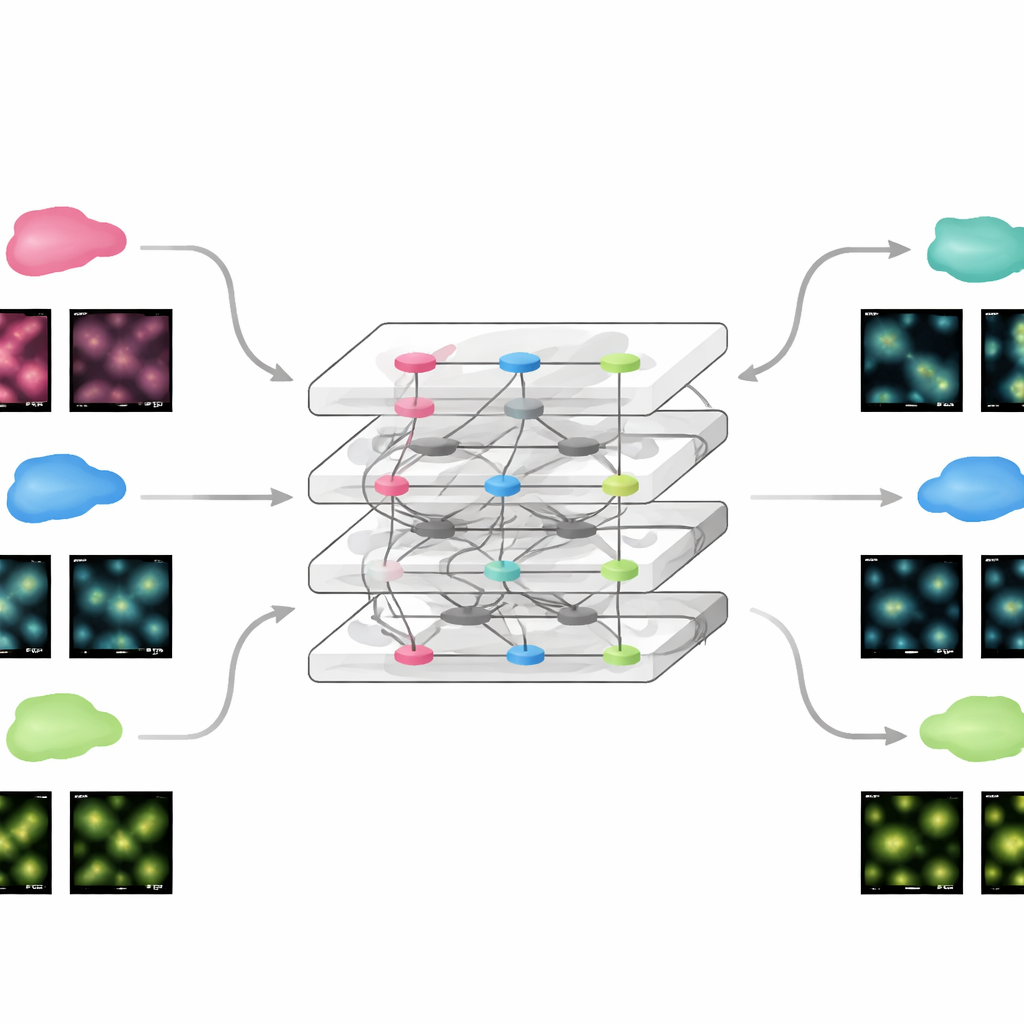
Szybkie dostosowanie do nowych eksperymentów
Dzięki temu, że FluoResFM startuje z szeroką bazą doświadczeń, można go dostroić do nowych danych używając zadziwiająco niewielu dodatkowych informacji. Zespół pokazał, że aktualizując tylko niewielką część sieci jednym przykładowym obrazem z nowego zestawu danych, model osiąga wydajność porównywalną z konwencjonalnymi sieciami głębokimi trenowanymi od podstaw na setkach obrazów. Dotyczyło to zarówno obrazów statycznych, jak i filmów czasowych przedstawiających poruszające się struktury komórkowe, gdzie dostrojony model poprawiał zarówno klarowność, jak i stabilność pomiarów w czasie. Ta sama strategia pozwoliła rozszerzyć FluoResFM poza pierwotne zadania treningowe na nowe, takie jak rekonstrukcja wolumenów 3D, projekcje powierzchni z 3D do 2D, wyrównywanie rozdzielczości wzdłuż różnych osi oraz obsługa wyższych współczynników powiększenia. We wszystkich tych przypadkach model generował wyraźniejsze struktury i lepsze zgodności ilościowe z danymi odniesienia.
Wzmacnianie innych narzędzi, żeby lepiej widziały komórki
FluoResFM to nie tylko sposób na estetyczne obrazy; wzmacnia też narzędzia analityczne zależne od jakości obrazów. Gdy autorzy podawali przywrócone obrazy do popularnych automatycznych programów segmentacyjnych używanych do wyznaczania konturów jąder, błon i organelli, te narzędzia wykrywały więcej obiektów, mniej ich przeoczały i generowały kształty lepiej zgodne z ekspercką prawdą jako punkt odniesienia. Poprawa była widoczna w dziesiątkach zestawów danych obejmujących wiele typów komórek i struktur. Aby obniżyć barierę codziennego użycia, zespół zapakował FluoResFM jako wtyczkę do napari — szeroko stosowanego interaktywnego przeglądarki obrazów — tak aby biologowie mogli przywracać obrazy i dostrajać model w ramach zwykłych przepływów pracy bez konieczności pisania kodu.
Co to oznacza dla przyszłości mikroskopii
Mówiąc prosto, ta praca pokazuje, że pojedynczy, kierowany tekstowo model AI może oczyszczać i wyostrzac szeroką gamę obrazów mikroskopii fluorescencyjnej, szybko dostosowywać się do nowych eksperymentów i zwiększać wydajność innych narzędzi analitycznych. Łącząc wiedzę o tym, co jest obrazowane, jak to zostało zarejestrowane i jaki rodzaj poprawy jest pożądany, FluoResFM generuje bardziej wiarygodne obrazy niż sieci zadaniowe trenowane w izolacji. W miarę dodawania kolejnych danych i zadań takie modele podstawowe mogą stać się standardowymi towarzyszami mikroskopów, przekształcając niedoskonałe surowe migawki w wiarygodne okna na ukrytą architekturę i dynamikę żywych komórek.
Cytowanie: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Słowa kluczowe: mikroskopia fluorescencyjna, rekonstrukcja obrazów, uczenie głębokie, modele podstawowe, obrazowanie komórek