Clear Sky Science · pt
Um modelo foundation para restauração multitarefa e entre-distribuições de imagens de microscopia de fluorescência
Visões mais nítidas do mundo celular oculto
A biologia moderna depende de microscópios para observar a vida agitada dentro das células, mas as imagens que capturamos frequentemente ficam granuladas, borradas ou sem detalhes finos. Este artigo apresenta o FluoResFM, um novo modelo de inteligência artificial (IA) projetado para limpar e aprimorar imagens de microscopia de fluorescência em muitos experimentos diferentes, tudo dentro de um único sistema. Para os cientistas, isso significa imagens mais claras com menos tentativa e erro; para pacientes e o público, aponta para descobertas biológicas e insights médicos mais rápidos e confiáveis, baseados em dados de maior qualidade.
Por que imagens de microscopia são tão difíceis de obter corretamente
Microscópios de fluorescência revelam proteínas, membranas e organelas fazendo-as brilhar, mas há uma troca: usar luz suave para proteger células vivas frequentemente produz imagens ruidosas, escuras e borradas. Pesquisadores passaram a recorrer ao aprendizado profundo para reparar essas imagens, treinando redes neurais para remover ruído, desfazer borrões ou aumentar resolução usando pares de exemplo de imagens de baixa e alta qualidade. No entanto, a maioria das ferramentas existentes é especializada e limitada. Um modelo pode funcionar apenas para denoising de uma estrutura particular, outro apenas para aprimorar um tipo específico de microscópio. Quando um modelo assim é aplicado a uma nova estrutura ou configuração de imagem, ele pode falhar gravemente, inventando detalhes falsos ou distorcendo os reais — um problema sério quando cientistas dependem dessas imagens para medições precisas.
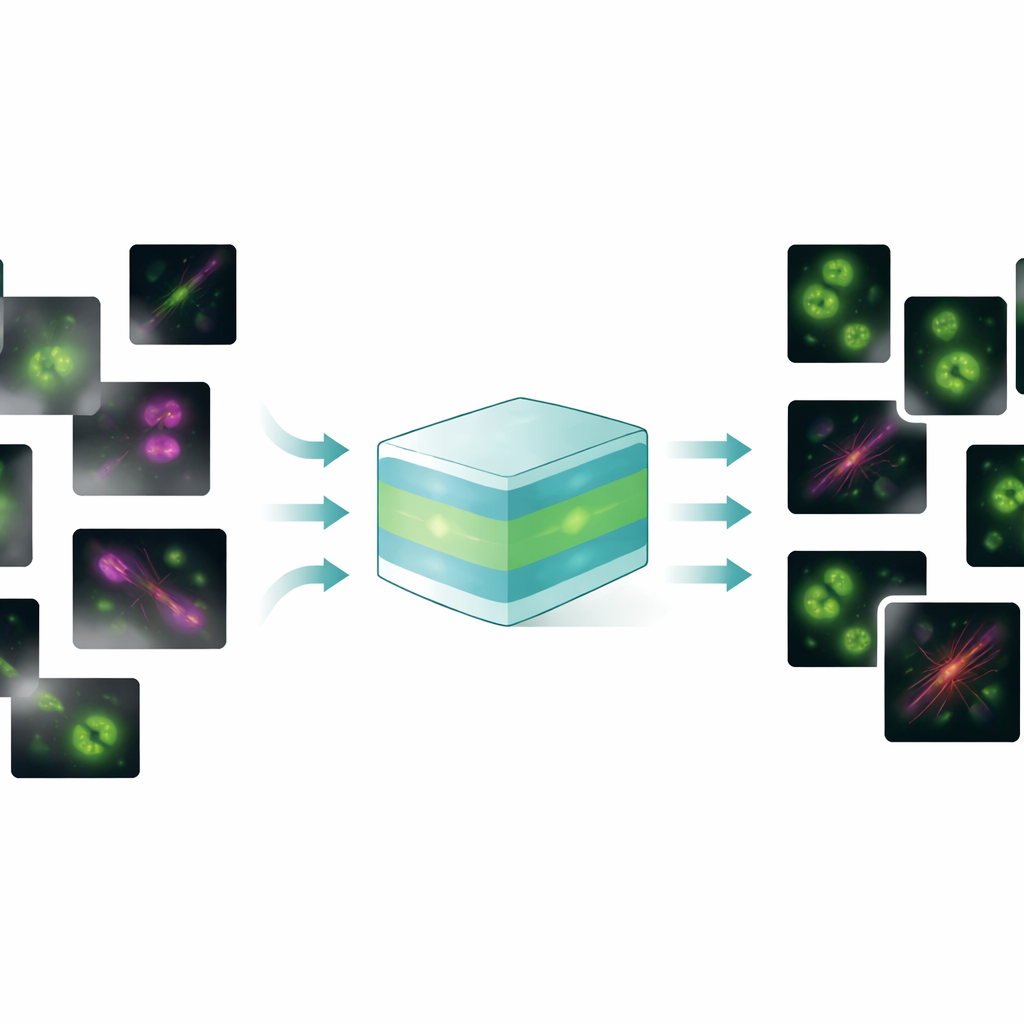
Um modelo para lidar com muitos problemas de imagem
O FluoResFM pretende ser um generalista: um modelo foundation capaz de executar várias tarefas de restauração — remoção de ruído, desborramento (deconvolução) e super-resolução — através de muitos tipos de estruturas celulares e microscópios em um único framework unificado. Os autores o treinaram com mais de 4,3 milhões de patches de imagem cobrindo mais de 20 estruturas biológicas, desde poços revestidos por clatrina e microtúbulos até núcleos, lisossomos e retículo endoplasmático, coletados em uma ampla variedade de condições de imagem. Em seu núcleo, o FluoResFM usa uma arquitetura no estilo U‑Net, um desenho comum para processamento de imagens biomédicas, mas é guiado por informação extra: descrições de texto curtas que codificam qual tarefa está sendo feita, qual estrutura está presente e como as imagens foram adquiridas. Esses prompts textuais são convertidos em features numéricas usando um modelo pré-treinado de linguagem–visão biomédica e então fundidos com features de imagem dentro da rede por camadas de atenção. Na prática, o modelo recebe não apenas “limpe esta imagem”, mas “remova ruído de uma imagem de microtúbulo deste tipo de microscópio em direção a esse tipo de referência”, o que o ajuda a escolher o tipo correto de correção.
Como a orientação por texto melhora a qualidade da imagem
Quando os autores compararam o FluoResFM com um modelo foundation líder anterior e com uma versão de si mesmo sem orientação textual, o modelo com texto mostrou claramente superioridade. Em centenas de conjuntos de dados internos e 51 conjuntos externos inéditos, o FluoResFM produziu imagens mais próximas das referências de alta qualidade por múltiplas medidas de nitidez, similaridade e erro. Foi especialmente eficaz em resolver características próximas entre si, como poros em forma de anel no envelope nuclear ou redes de microtúbulos emaranhadas, e evitou a tendência de mesclar estruturas vizinhas. Os prompts textuais também forneciam um mecanismo poderoso de direcionamento. Mudar a descrição da tarefa de “remoção de ruído” para “super-resolução” (conceitualmente) levou a mesma rede a executar operações muito diferentes sobre imagens de entrada idênticas. Do mesmo modo, especificar o tipo de estrutura errado fez o modelo reconstruir padrões enganosos, como transformar uma rede reticular em pontos, ressaltando tanto a flexibilidade do modelo quanto a importância de conhecimentos prévios corretos.
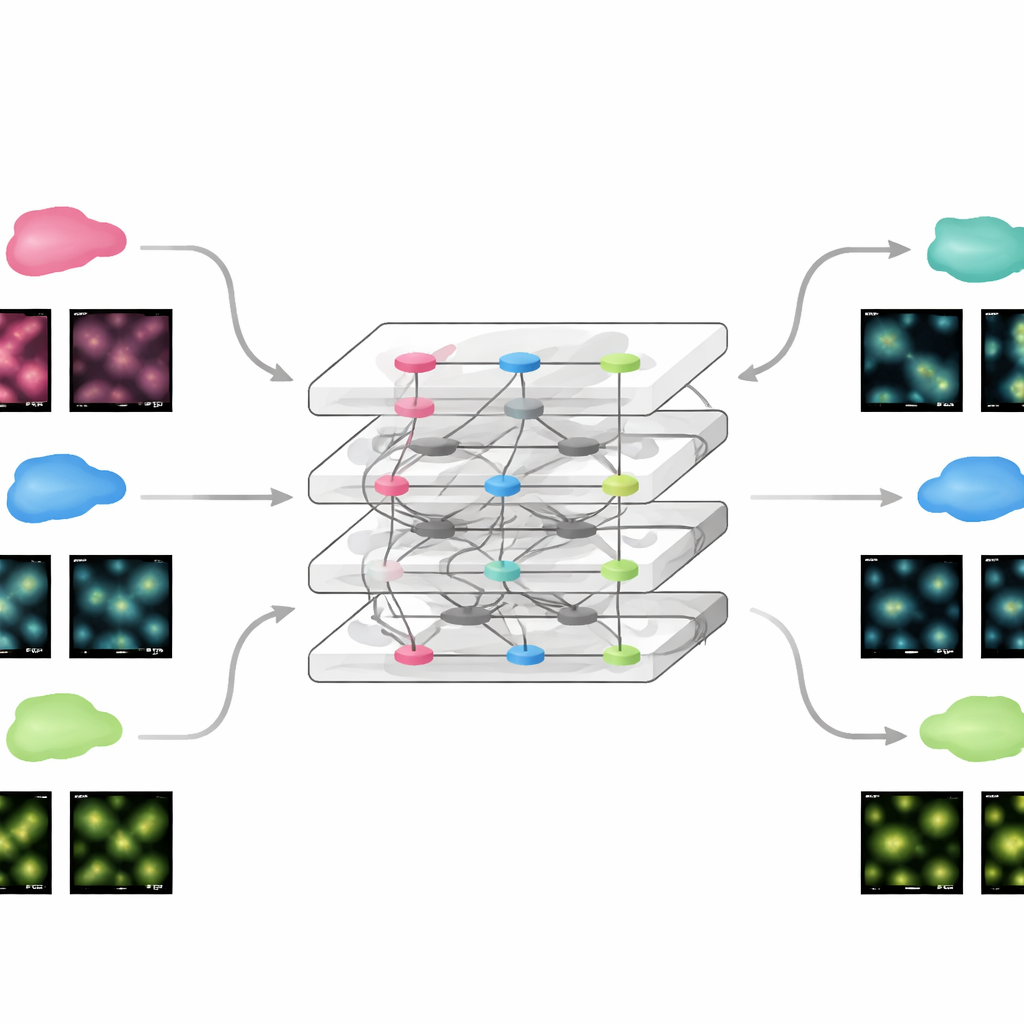
Adaptação rápida a novos experimentos
Porque o FluoResFM parte de uma base ampla de experiência, ele pode ser ajustado para novos dados usando surpreendentemente pouca informação adicional. A equipe mostrou que, ao atualizar apenas uma pequena parte da rede com uma única imagem de exemplo de um novo conjunto de dados, o modelo atingiu desempenho comparável ao de redes profundas convencionais treinadas do zero com centenas de imagens. Isso se manteve verdadeiro para imagens estáticas e para filmes time-lapse de estruturas celulares em movimento, onde o modelo fine-tunado melhorou tanto a clareza quanto a estabilidade das medições ao longo do tempo. A mesma estratégia permitiu estender o FluoResFM além das tarefas originais de treinamento para novas, como restauração volumétrica tridimensional, projeções de superfície de 3D para 2D, uniformizar resolução ao longo de diferentes eixos e lidar com fatores de aumento maiores. Em todos esses casos, o modelo produziu estruturas mais claras e melhor concordância quantitativa com os dados de referência.
Ajuda para outras ferramentas verem células com mais clareza
O FluoResFM não é apenas uma forma de gerar imagens bonitonas; ele também fortalece ferramentas de análise posteriores que dependem da qualidade da imagem. Quando os autores alimentaram imagens restauradas em programas populares de segmentação automatizada usados para delinear núcleos, membranas e organelas, essas ferramentas detectaram mais objetos, perderam menos e produziram formas que concordavam melhor com o ground truth derivado por especialistas. Essa melhora foi observada em dezenas de conjuntos de dados com muitos tipos celulares e estruturas. Para reduzir a barreira ao uso diário, a equipe empacotou o FluoResFM como um plugin para o napari, um visualizador de imagens interativo amplamente usado, para que biólogos possam restaurar imagens e ajustar o modelo dentro de seus fluxos de trabalho habituais sem precisar escrever código.
O que isso significa para a microscopia futura
Em termos simples, este trabalho mostra que um único modelo de IA guiado por texto pode limpar e aprimorar uma ampla gama de imagens de microscopia de fluorescência, adaptar-se rapidamente a novos experimentos e aumentar o desempenho de outras ferramentas de análise. Ao entrelaçar conhecimento sobre o que está sendo imageado, como foi capturado e que tipo de melhoria é desejada, o FluoResFM produz imagens mais confiáveis do que redes específicas de tarefa treinadas isoladamente. À medida que mais dados e tarefas forem adicionados, tais modelos foundation podem se tornar companheiros padrão dos microscópios, transformando instantâneos brutos imperfeitos em janelas confiáveis sobre a arquitetura oculta e a dinâmica das células vivas.
Citação: Lu, Q., Liu, X., Feng, Q. et al. A foundation model for multi-task cross-distribution restoration of fluorescence microscopy images. Nat Commun 17, 3729 (2026). https://doi.org/10.1038/s41467-026-70307-4
Palavras-chave: microscopia de fluorescência, restauração de imagens, aprendizado profundo, modelos foundation, imagem celular