Clear Sky Science · tr
Bitkisel GTR1 tarafından glukozinolat tanıma ve taşınmanın yapısal temeli
Gizli Bir Bedeli Olan Bitki Kalkanları
Tabağımızdaki hardal otu gibi sebzelerden kanola yağının kaynağı olan kolzaya kadar birçok bitki, glukozinolatlar olarak adlandırılan baharatlı, kükürtçe zengin bir bileşik ailesiyle kendini savunur. Bu bileşikler aç böcekleri uzak tutabilir ve insan sağlığı için faydaları bile olabilir; ancak hayvan yemi ve bazı mahsullerde antienerjiler (anti‑besinler) olarak kabul edilirler. Bu çalışma, bitki hücrelerinde küçük bir bekçi proteini olan GTR1’in glukozinolatları nasıl tanıdığını ve taşıdığını atomik ayrıntıda ortaya koyuyor; bu da hem daha iyi savunmalı hem de daha besleyici ürünler geliştirme yolunu açıyor.
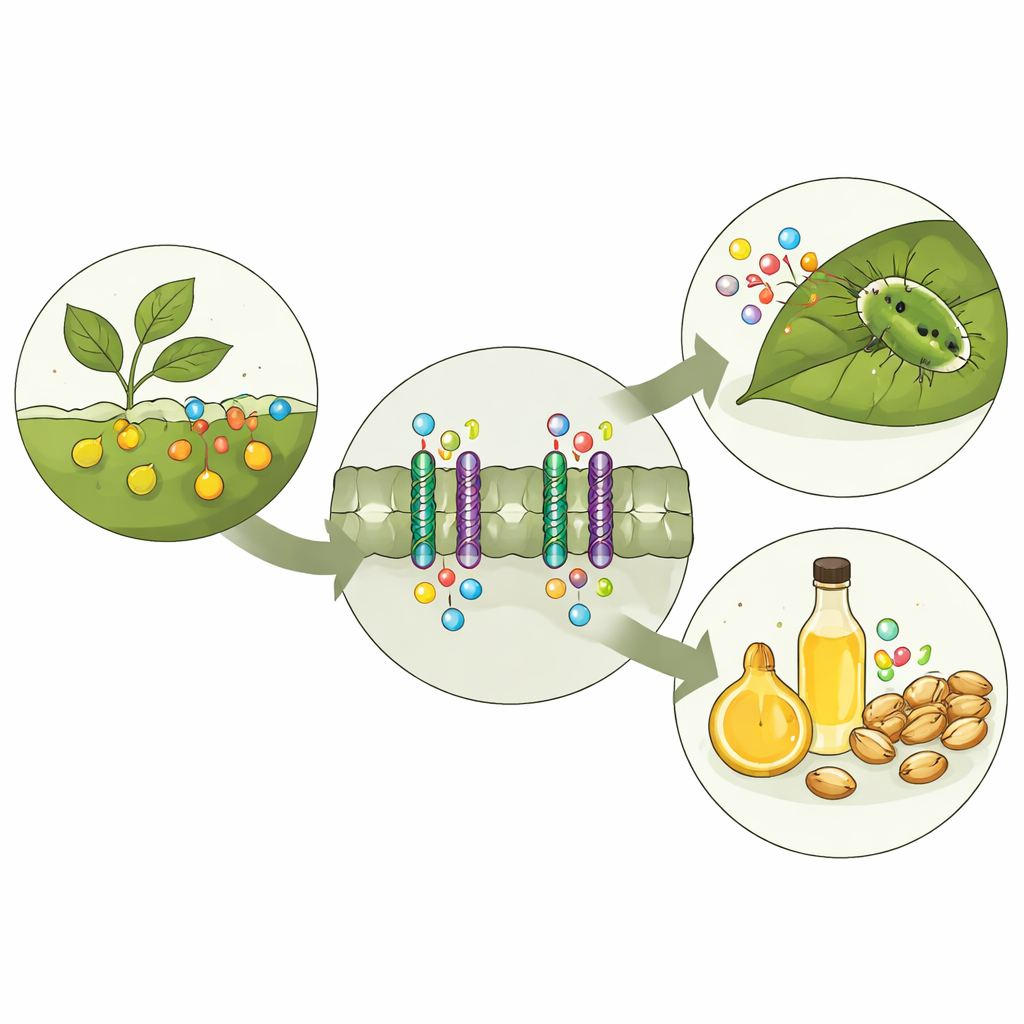
Bitkilerde Kimyasal Bir Güvenlik Sistemi
Glukozinolatlar, onları parçalayan enzimlerden ayrı saklanır. Bir böcek yaprağı çiğnediğinde, bu bölmeler yırtılır ve glukozinolatlar hızla keskin tatlı ve bazen toksik ürünlere dönüştürülerek daha fazla yemeyi caydırır. Bu savunmanın işlemesi için bitkilerin glukozinolatları üretildikleri yerden tohumlar ve özel depolama hücreleri gibi ihtiyaç duyulan yerlere göndermesi gerekir. Model bitki Arabidopsis’te, GTR1, GTR2 ve GTR3 adında üç ilişkili taşıyıcı protein bu işi üstlenir. Önceki genetik çalışmalar, bu taşıyıcılar bozulduğunda bitki içindeki glukozinolat seviyeleri ve dağılımlarının değiştiğini; bunun da hem savunmayı hem de tohum kalitesini etkilediğini göstermiştir.
Hücre Duvarındaki Kapı
GTR1 hücrenin dış zarında yer alır ve glukozinolat alımını protonların (hidrojen iyonları) zar boyunca akışıyla eşleştiren döner bir kapı gibi davranır. Kriyo‑elektron mikroskobu kullanarak yazarlar Arabidopsis GTR1’in dört üç boyutlu anlık görüntüsünü yakaladılar: kargosu olmayan iki yapı (biri dışa açık, biri içe açık) ve bağlı glukozinolatlı iki yapı. Bu görüntüler, GTR1’in merkezi bir boşluk oluşturan on iki zar geçişli segmentten oluşan bir çekirdeğe sahip olduğunu ve bu çekirdeğin bir heliksine yaslanan büyük bir “intrasellüler bölüm” tarafından çevrelendiğini gösteriyor. Bu bölümü budayarak veya ana temas noktalarını değiştirerek araştırmacılar, bunun düzgün taşıma için gerekli olduğunu; muhtemelen hareketli parçaları hizalı tutan stabilize edici bir iskelet görevi gördüğünü gösterdiler.
GTR1 Kargosunu Nasıl Tanır
Ekip, GTR1’in farklı yan zincirlere sahip iki temsilci glukozinolatı nasıl bağladığını inceledi. Her ikisi de aynı merkezi cebe yerleşmiş bulundu. Şeker ve yüklü sülfat kısımları—neredeyse tüm glukozinolatlarda ortak özellikler—boşluğun bir tarafındaki pozitif yüklü ve polar aminoasit kümesi tarafından kavranıyor. Bu kalıntıları sistematik olarak değiştirerek yazarlar, taşıma için anahtar olan iki aminoasidi, aralarında taşıyıcı ailesi boyunca ortak bir işaret dizisinin parçası olan bir lizin de dahil olmak üzere, belirlediler. Buna karşılık, değişken yan zincirlerle temas eden aminoasitlerin aktivite için daha az önemli olduğu görüldü; bu da GTR1’in birçok glukozinolatı işleyebilmesini açıklıyor. GTR1, GTR2 ve GTR3 arasındaki bu yan‑zincir‑temas noktalarındaki ince farklılıklar, her bir proteinin tercih ettiği özgül glukozinolatları ayarlıyor olabilir.
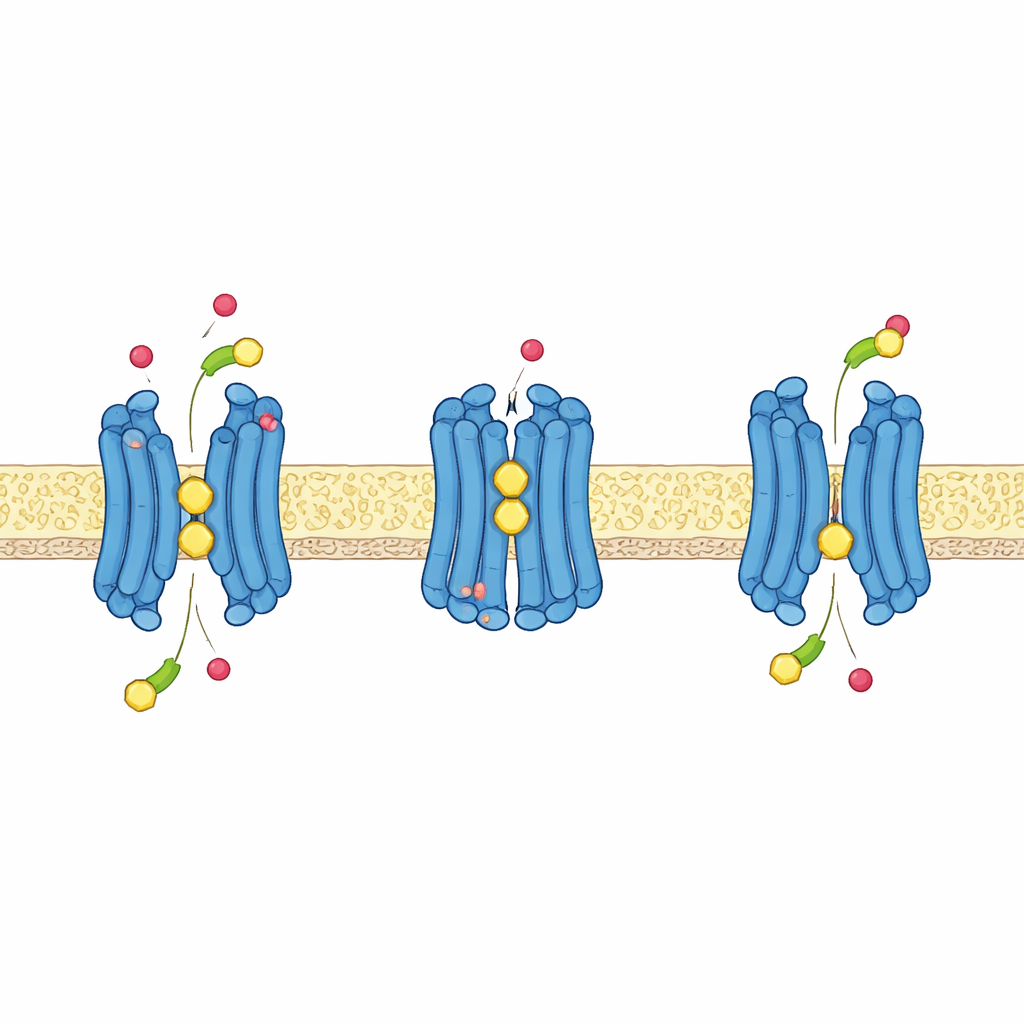
Taşımayı Güçlendirmek için Protonların Kullanılması
Birçok bitki besin taşıyıcısı gibi GTR1 de proton gradyanında depolanan eneriden—hücre dışının hücre içinden daha fazla protonuna—yararlanarak glukozinolatları aktif biçimde içeri çeker. Yapılar, bilgisayar simülasyonları ve farklı asidite düzeylerinde yapılan taşıma testleri bu işleyişi atomik düzeyde ortaya koyuyor. Merkezi boşluğun üst kısmına yakın kısa bir aminoasit dizisi, iki glutamat ve bir lizin içeriyor ve protein dışa‑açık ve içe‑açık durumları arasında geçiş yaparken yeniden düzenleniyor. Belirli glutamatlar proton aldığında lizine olan tutunmayı bırakıyor, lizini negatif yüklü sülfat grubunu bağlamaya yardımcı olmak üzere serbest bırakarak proteinin yükünü çevresine kapatmasını teşvik ediyor. Proteinin daha derininde yer alan başka bir glutamat, yakındaki bir tirozinle önemli bir ortaklık oluşturuyor; bu yer protonlandığında taşıyıcının dışa‑açık halden içe‑açık hale geçmesini destekliyor ve süreci hücrenin elektriksel voltajına duyarlı kılıyor.
Atomik Görüntülerden Daha İyi Mahsullere
Bu sonuçlar birlikte, GTR1’in protonları ve glukozinolatları birlikte taşırken dışa‑açık, kapalı (oklüde) ve içe‑açık şekiller arasında döndüğü alternatif‑erişim (alternating‑access) modelini destekliyor. Hangi protein özelliklerinin ortak glukozinolat “iskeletini” tanıdığını, hangilerinin yan‑zincir tercihlerini ayarladığını ve hangilerinin taşımayı proton akışına bağladığını netleştirerek çalışma, bitkilerde glukozinolat hareketini mühendislik etmek için ayrıntılı bir plan sunuyor. Pratik anlamda bu bilgi, tohumlarında daha az acı ve anti‑besin glukozinolat biriken; yaprak ve saplarında ise böceklere karşı güçlü kimyasal savunmayı koruyan mahsuller yetiştirmek veya tasarlamak için kullanılabilir—çiftçilere sahada daha dayanıklı ve gıda ile yem açısından daha değerli bitkiler sunar.
Atıf: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Anahtar kelimeler: glukozinolatlar, bitki taşıyıcıları, GTR1, ürün geliştirme, proton-bağlı taşıma