Clear Sky Science · it
Basi strutturali del riconoscimento e del trasporto dei glucosinolati da parte della proteina vegetale GTR1
Scudi vegetali con un costo nascosto
Molte delle verdure nei nostri piatti, dalle cime di senape alla colza da cui si ricava l’olio, si difendono con una famiglia di composti piccanti e ricchi di zolfo chiamati glucosinolati. Questi composti possono dissuadere gli insetti affamati e persino avere benefici per la salute umana, ma nell’alimentazione animale e in alcune colture sono considerati anti‑nutrienti. Questo studio svela, a livello atomico, come una piccola proteina guardiana nelle cellule vegetali, chiamata GTR1, riconosce e trasporta i glucosinolati, aprendo la strada a colture più difese e più nutrienti.
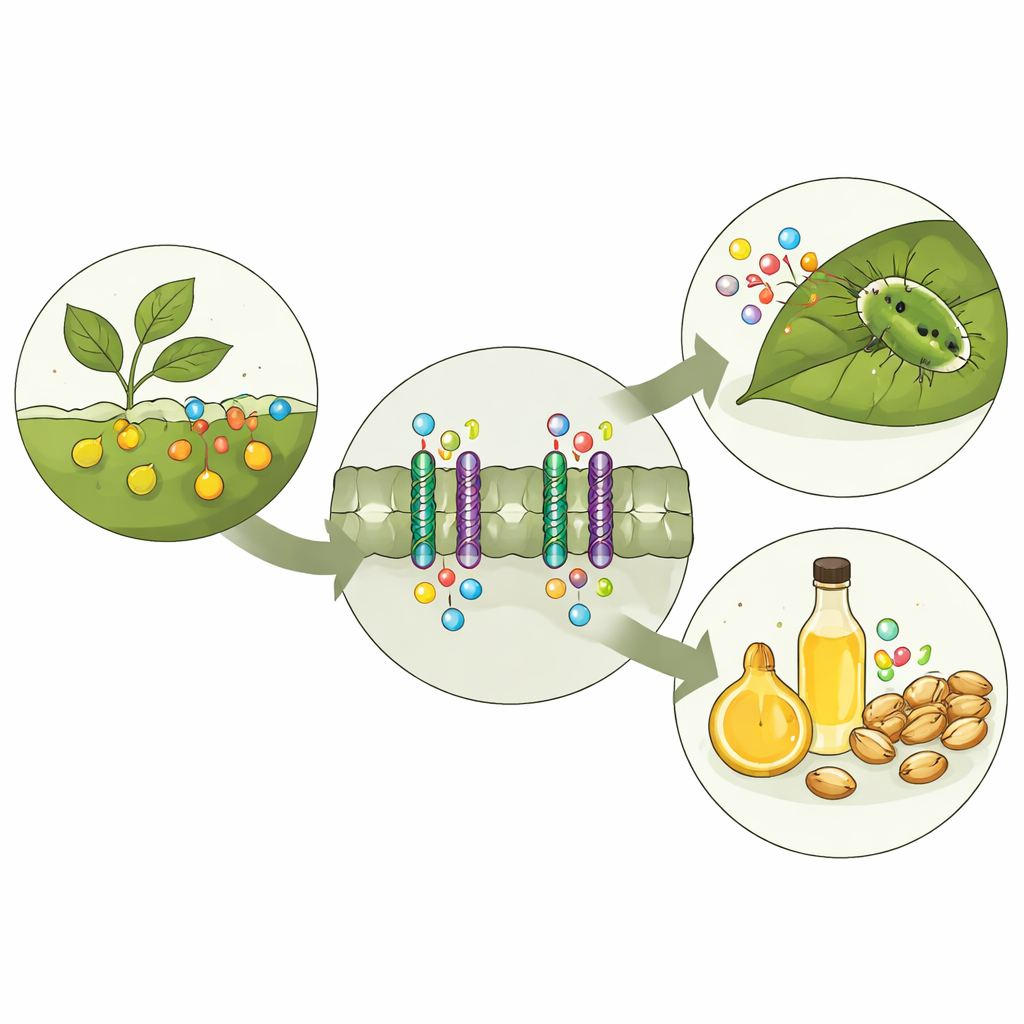
Un sistema di sicurezza chimica nelle piante
I glucosinolati sono immagazzinati separatamente dagli enzimi che li degradano. Quando un insetto morde una foglia, i compartimenti si rompono e i glucosinolati vengono rapidamente convertiti in prodotti dal sapore pungente e talvolta tossici che scoraggiano ulteriori mandibolate. Perché questa difesa funzioni, le piante devono spostare i glucosinolati dal luogo in cui vengono prodotti fino ai siti in cui servono, come i semi e le cellule di stoccaggio specializzate. Nella pianta modello Arabidopsis, tre trasportatori correlati, GTR1, GTR2 e GTR3, svolgono questo compito. Studi genetici precedenti hanno mostrato che quando questi trasportatori sono alterati, i livelli e la distribuzione dei glucosinolati nella pianta cambiano, modificando sia la difesa sia la qualità dei semi.
La porta nella parete cellulare
GTR1 si trova nella membrana esterna della cellula e agisce come una porta girevole che accoppia l’assorbimento dei glucosinolati al flusso di protoni (ioni idrogeno) attraverso la membrana. Utilizzando la crio‑microscopia elettronica, gli autori hanno ottenuto quattro istantanee tridimensionali di GTR1 di Arabidopsis: due senza carico (una aperta verso l’esterno, una verso l’interno) e due con glucosinolati legati. Queste immagini rivelano che GTR1 possiede un nucleo di dodici eliche transmembrana che formano una cavità centrale, circondata da un ampio “dominio intracellulare” che si adagia contro una delle eliche. Rimuovendo questo dominio o modificando punti di contatto chiave, i ricercatori hanno dimostrato che è essenziale per un trasporto corretto, probabilmente fungendo da impalcatura stabilizzante che mantiene allineate le parti mobili.
Come GTR1 riconosce il suo carico
Il team ha studiato come GTR1 si lega a due glucosinolati rappresentativi con catene laterali diverse. Entrambi sono risultati alloggiati nella stessa tasca centrale. Le porzioni zuccherine e il gruppo solfato carico — caratteristiche condivise da virtualmente tutti i glucosinolati — sono afferrate da un ammasso di residui aminoacidici positivi e polari su un lato della cavità. Modificando sistematicamente questi residui, gli autori hanno mostrato che due di essi, inclusa una lisina che fa parte di una sequenza caratteristica condivisa da questa famiglia di trasportatori, sono cruciali per il trasporto. Al contrario, gli amminoacidi che toccano le catene laterali variabili si sono rivelati meno importanti per l’attività, spiegando come GTR1 possa gestire molti glucosinolati diversi. Differenze sottili nelle posizioni che contattano le catene laterali tra GTR1, GTR2 e GTR3 probabilmente sintonizzano le preferenze specifiche di ciascuna proteina per determinati glucosinolati.
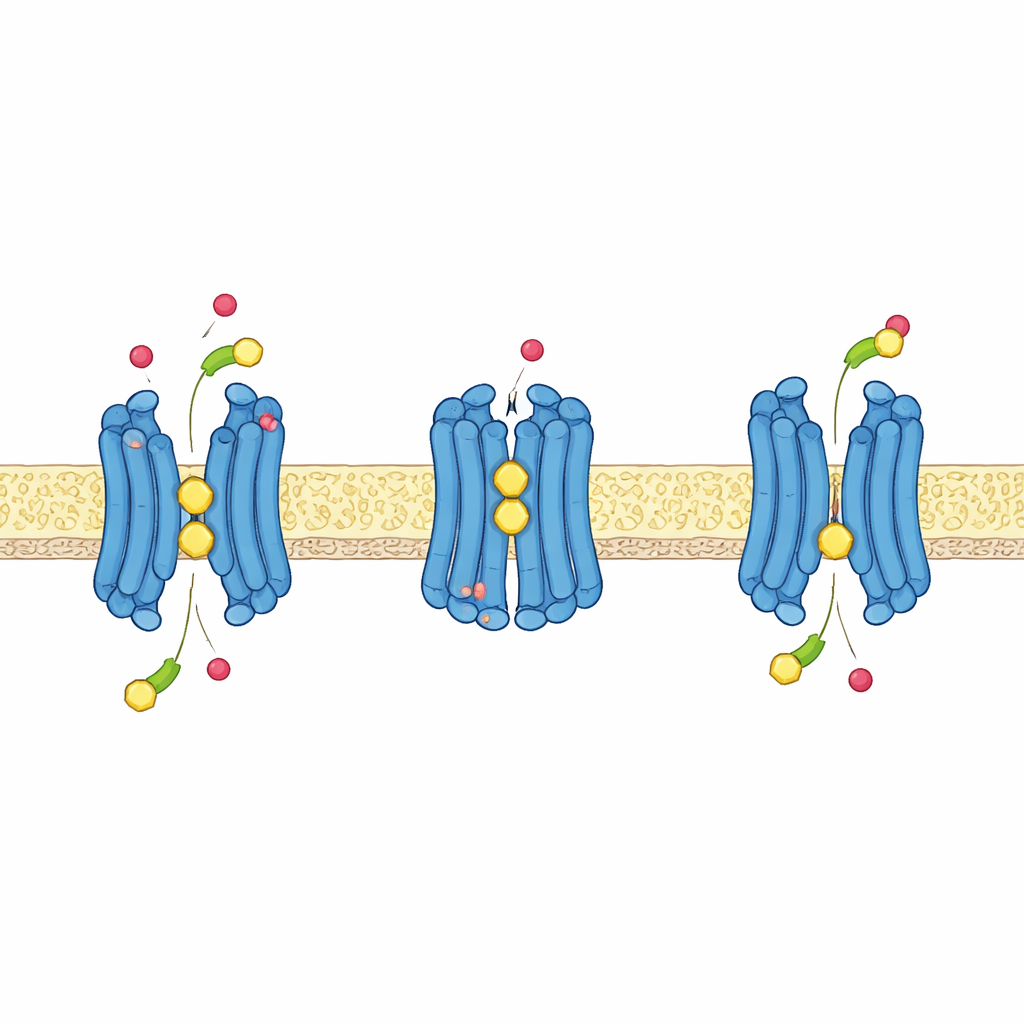
Usare i protoni per alimentare il trasporto
Come molti trasportatori di nutrienti nelle piante, GTR1 sfrutta l’energia immagazzinata in un gradiente di protoni — più protoni all’esterno della cellula che all’interno — per prelevare attivamente i glucosinolati verso l’interno. Le strutture, combinate con simulazioni al computer e test di trasporto a diversi livelli di acidità, rivelano come ciò avvenga a livello atomico. Un breve tratto di amminoacidi vicino alla sommità della cavità centrale, contenente due glutammati e una lisina, si riorganizza mentre la proteina passa tra stati rivolti verso l’esterno e verso l’interno. Quando certi glutammati catturano protoni, rilasciano la presa sulla lisina, liberandola per aiutare a legare il gruppo solfato carico negativamente dei glucosinolati e favorendo la chiusura della proteina attorno al suo carico. Un altro glutammato, più profondo nella proteina, forma una partnership chiave con una tirosina vicina; quando è protonato, questo sito contribuisce a spingere il trasportatore dallo stato rivolto verso l’esterno a quello rivolto verso l’interno e rende il processo sensibile alla tensione elettrica della cellula.
Dalle immagini atomiche a colture migliori
Nel complesso, questi risultati supportano un modello ad accesso alternato in cui GTR1 cicla attraverso forme aperte verso l’esterno, occluse e aperte verso l’interno mentre cotrasporta protoni e glucosinolati. Chiarendo esattamente quali caratteristiche della proteina riconoscono lo “scheletro” comune dei glucosinolati, quali modulano le preferenze per le catene laterali e quali accoppiano il trasporto al flusso di protoni, lo studio fornisce un progetto dettagliato per ingegnerizzare il movimento dei glucosinolati nelle piante. In termini pratici, questa conoscenza potrebbe essere usata per selezionare o progettare colture i cui semi accumulano meno glucosinolati amari e anti‑nutrizionali mentre foglie e fusti mantengono forti difese chimiche contro gli insetti — offrendo agli agricoltori piante più robuste in campo e più preziose come alimento e mangime.
Citazione: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Parole chiave: glucosinolati, trasportatori vegetali, GTR1, miglioramento delle colture, trasporto accoppiato ai protoni