Clear Sky Science · es
Base estructural del reconocimiento y transporte de glucosinolatos por la proteína vegetal GTR1
Escudos vegetales con un coste oculto
Muchas de las verduras que consumimos, desde las hojas de mostaza hasta la planta parenta del aceite de colza, el nabo forrajero, se defienden mediante una familia de compuestos picantes y ricos en azufre llamados glucosinolatos. Estos compuestos pueden disuadir a insectos voraces e incluso aportar beneficios para la salud humana, pero en piensos animales y en algunos cultivos se consideran antinutrientes. Este estudio desvela, con detalle atómico, cómo una pequeña proteína portera en las células vegetales, denominada GTR1, reconoce y transporta glucosinolatos, abriendo la vía para cultivos mejor defendidos y más nutritivos.
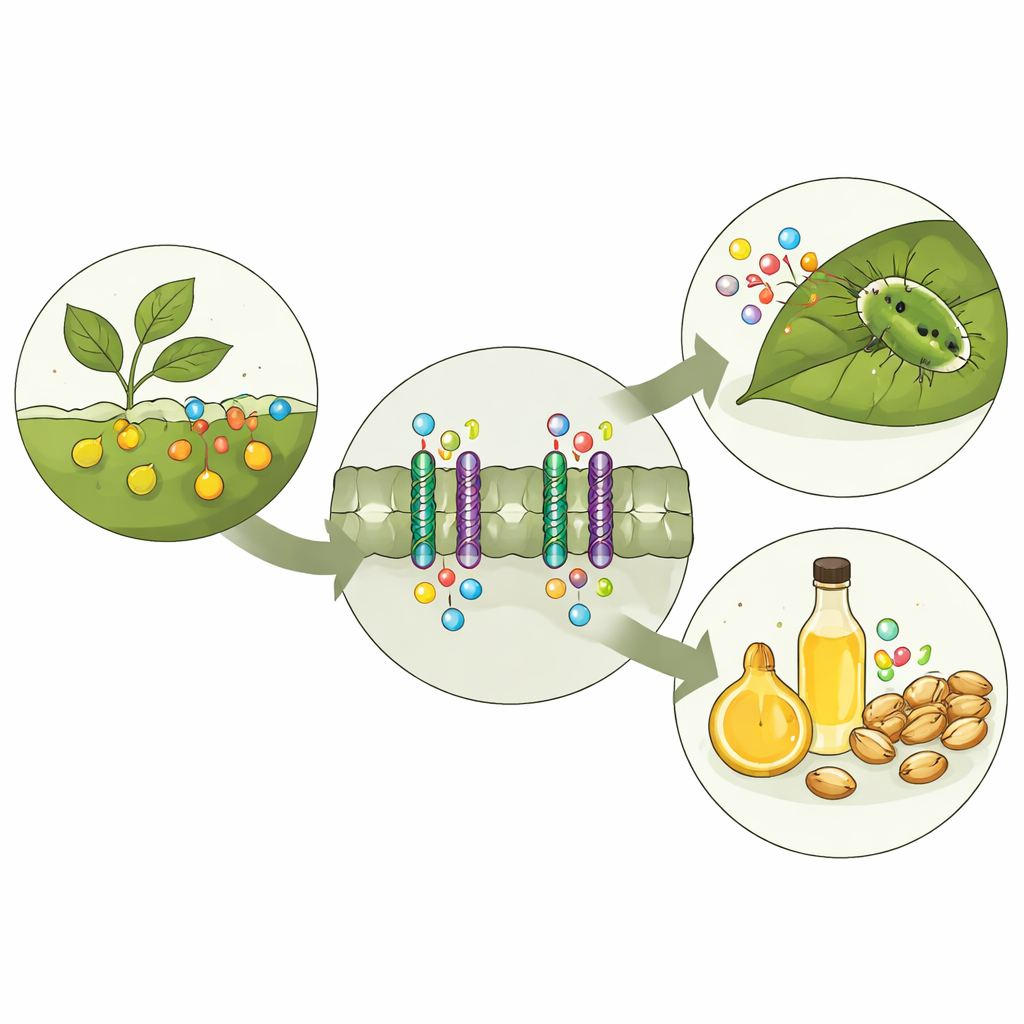
Un sistema de seguridad química en las plantas
Los glucosinolatos se almacenan por separado de las enzimas que los degradan. Cuando un insecto roe una hoja, los compartimentos se rompen y los glucosinolatos se convierten rápidamente en productos de sabor punzante y a veces tóxicos que desalientan la alimentación adicional. Para que esta defensa funcione, las plantas deben transportar los glucosinolatos desde el lugar donde se sintetizan hasta donde se necesitan, como las semillas y células de almacenamiento especializadas. En la planta modelo Arabidopsis, tres proteínas transportadoras relacionadas —GTR1, GTR2 y GTR3— se encargan de esta tarea. Trabajos genéticos previos mostraron que cuando estos transportadores se alteran, los niveles y la distribución de glucosinolatos en la planta cambian, modificando tanto la defensa como la calidad de las semillas.
La puerta en la membrana celular
GTR1 se sitúa en la membrana externa de la célula y actúa como una puerta giratoria que acopla la captación de glucosinolatos al flujo de protones (iones de hidrógeno) a través de la membrana. Mediante criomicroscopía electrónica, los autores capturaron cuatro instantáneas tridimensionales de GTR1 de Arabidopsis: dos sin carga (una abierta al exterior y otra al interior) y dos con glucosinolatos unidos. Estas imágenes revelan que GTR1 tiene un núcleo de doce segmentos transmembrana que forman una cavidad central, rodeada por un gran “dominio intracelular” que se apoya contra una de las hélices. Al recortar este dominio o modificar puntos de contacto clave, los investigadores mostraron que es esencial para el transporte correcto, probablemente actuando como un andamiaje estabilizador que mantiene alineadas las partes móviles.
Cómo GTR1 reconoce su carga
El equipo examinó cómo GTR1 se une a dos glucosinolatos representativos con cadenas laterales diferentes. Ambos se encontraron alojados en el mismo bolsillo central. Las porciones azucaradas y la parte sulfato cargada —rasgos compartidos por prácticamente todos los glucosinolatos— son sujetadas por un conjunto de aminoácidos polar y positivamente cargados en un lado de la cavidad. Al alterar sistemáticamente estos residuos, los autores demostraron que dos de ellos, incluyendo una lisina que forma parte de una secuencia característica conservada en esta familia de transportadores, son cruciales para el transporte. En contraste, los aminoácidos que contactan las cadenas laterales variables resultaron menos importantes para la actividad, lo que explica cómo GTR1 puede manejar muchos glucosinolatos. Diferencias sutiles en estas posiciones de contacto con las cadenas laterales entre GTR1, GTR2 y GTR3 probablemente afinan las preferencias específicas de cada proteína por determinados glucosinolatos.
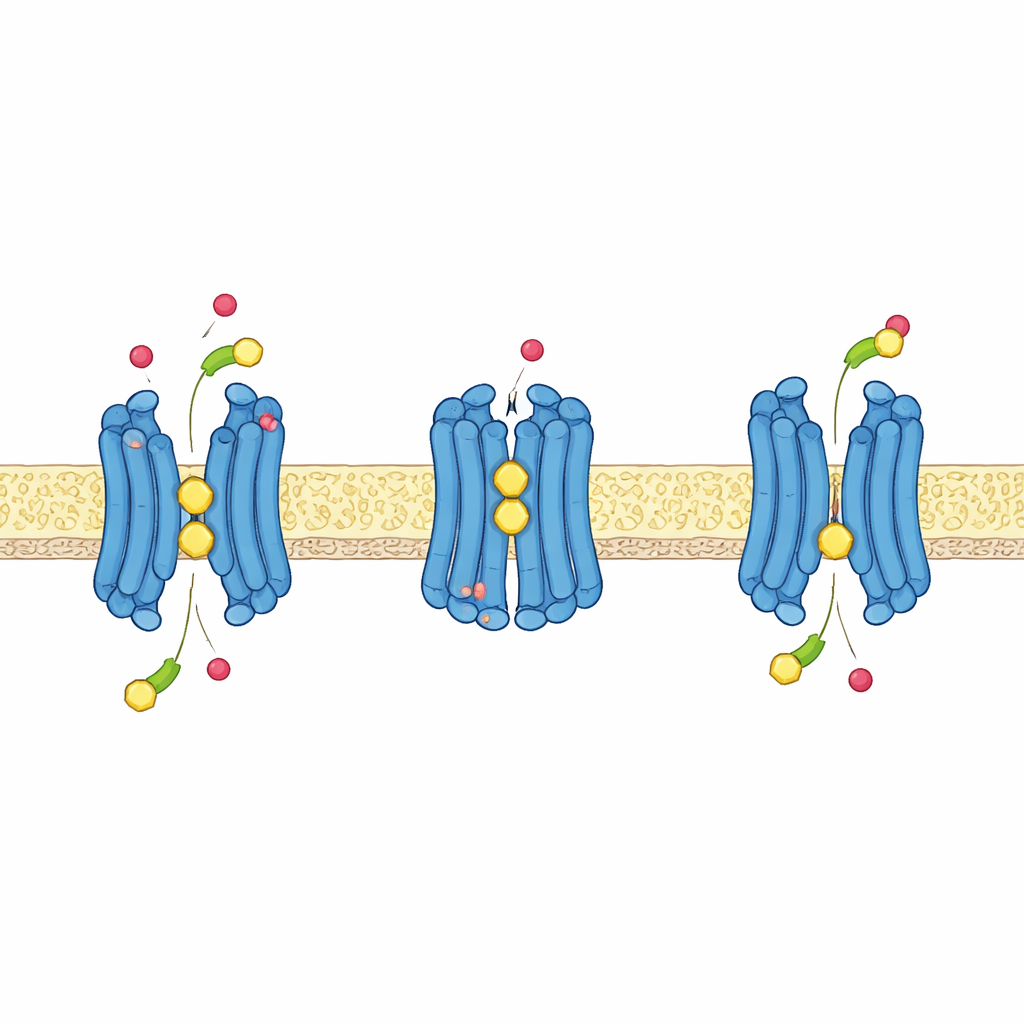
Usar protones para impulsar el transporte
Al igual que muchos transportadores de nutrientes en plantas, GTR1 aprovecha la energía almacenada en un gradiente de protones —más protones fuera de la célula que dentro— para arrastrar activamente los glucosinolatos hacia el interior. Las estructuras, combinadas con simulaciones por ordenador y ensayos de transporte a diferentes niveles de acidez, revelan cómo funciona esto a nivel atómico. Un tramo corto de aminoácidos cerca de la parte superior de la cavidad central, que contiene dos glutamatos y una lisina, se reorganiza cuando la proteína cambia entre estados orientados hacia el exterior y hacia el interior. Cuando ciertos glutamatos captan protones, aflojan su interacción con la lisina, lo que le permite ayudar a unir el grupo sulfato cargado negativamente de los glucosinolatos y favorece que la proteína se cierre alrededor de su carga. Otro glutamato, más profundo en la proteína, forma una asociación clave con una tirosina cercana; cuando se protona, este sitio ayuda a impulsar la transición del transportador desde el estado orientado hacia el exterior al orientado hacia el interior y hace que el proceso sea sensible al voltaje eléctrico de la célula.
De imágenes atómicas a cultivos mejores
En conjunto, estos resultados respaldan un modelo de acceso alterno en el que GTR1 cicla entre formas abiertas al exterior, ocluidas y abiertas al interior mientras co-transporta protones y glucosinolatos. Al clarificar exactamente qué rasgos de la proteína reconocen la “espina dorsal” común de los glucosinolatos, cuáles afinan las preferencias por las cadenas laterales y cuáles acoplan el transporte al flujo de protones, el estudio proporciona un plano detallado para diseñar el movimiento de glucosinolatos en plantas. En términos prácticos, este conocimiento podría usarse para criar o diseñar cultivos cuyas semillas acumulen menos glucosinolatos amargos y antinutricionales mientras hojas y tallos mantienen fuertes defensas químicas frente a insectos, ofreciendo a los agricultores plantas tanto más resistentes en el campo como más valiosas como alimento y pienso.
Cita: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Palabras clave: glucosinolatos, transportadores vegetales, GTR1, mejora de cultivos, transporte acoplado a protones