Clear Sky Science · de
Strukturelle Grundlage der Erkennung und des Transports von Glucosinolaten durch das Pflanzenprotein GTR1
Pflanzliche Schilde mit versteckten Kosten
Viele Gemüsesorten auf unserem Teller, von Senfblättern bis zur Raps‑Pflanze, der Ausgangsquelle für Rapsöl, verteidigen sich mit einer Familie scharfer, schwefelreicher Verbindungen, den Glucosinolaten. Diese Verbindungen können fressfeindliche Insekten abschrecken und haben möglicherweise auch gesundheitliche Vorteile für den Menschen, gelten in Tierfutter und einigen Nutzpflanzen jedoch als Anti‑Nährstoffe. Die vorliegende Studie enthüllt auf atomarer Ebene, wie ein kleiner Torwächterprotein in Pflanzenzellen, GTR1, Glucosinolate erkennt und transportiert und ebnet so den Weg zu Pflanzen, die zugleich besser geschützt und nahrhafter sind.
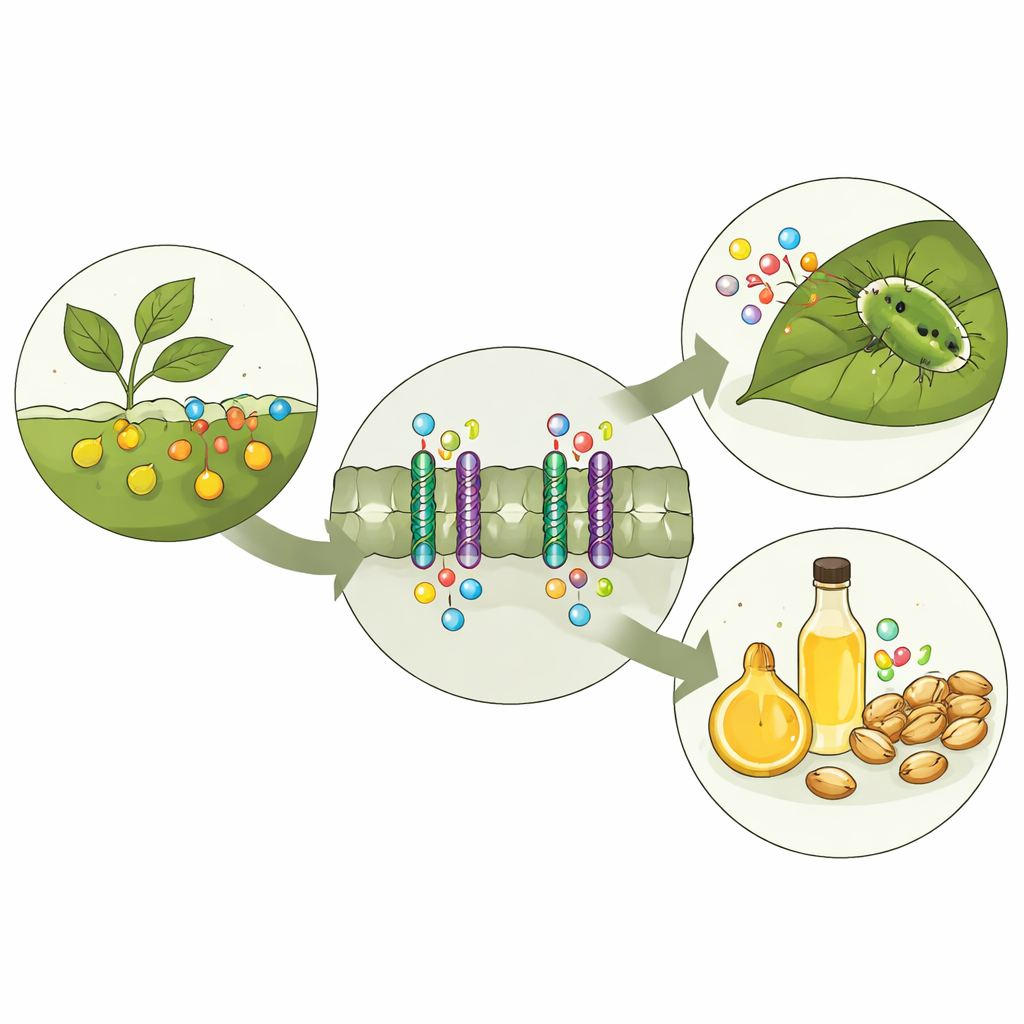
Ein chemisches Sicherheitssystem in Pflanzen
Glucosinolate werden getrennt von den Enzymen gespeichert, die sie abbauen. Wenn ein Insekt ein Blatt zerkaut, reißen die Kompartimente auf, und Glucosinolate werden schnell in scharf schmeckende und mitunter toxische Produkte umgewandelt, die weiteres Fressen unattraktiv machen. Damit diese Verteidigung funktioniert, müssen Pflanzen Glucosinolate dorthin transportieren, wo sie gebraucht werden, etwa in Samen oder spezialisierte Speicherzellen. In der Modellpflanze Arabidopsis übernehmen drei verwandte Transporterproteine, GTR1, GTR2 und GTR3, diese Aufgabe. Frühere genetische Arbeiten zeigten, dass bei Störungen dieser Transporter die Gehalte und Verteilung von Glucosinolaten in der Pflanze verändert sind, was sowohl die Abwehr als auch die Samenqualität beeinflusst.
Das Tor in der Zellwand
GTR1 sitzt in der äußeren Zellmembran und fungiert wie eine Drehtür, die die Aufnahme von Glucosinolaten an den Fluss von Protonen (Wasserstoffionen) über die Membran koppelt. Mithilfe der Kryo‑Elektronenmikroskopie hielten die Autoren vier dreidimensionale Schnappschüsse von Arabidopsis‑GTR1 fest: zwei ohne Fracht (jeweils nach außen und nach innen geöffnet) und zwei mit gebundenen Glucosinolaten. Diese Bilder zeigen, dass GTR1 einen Kern aus zwölf membranüberspannenden Segmenten besitzt, die eine zentrale Kavität bilden, umgeben von einer großen „intrazellulären Domäne“, die an einer der Helices anliegt. Durch Das Entfernen dieser Domäne oder das Verändern zentraler Kontaktstellen zeigten die Forscher, dass sie für den korrekten Transport unerlässlich ist und wahrscheinlich als stabilisierendes Gerüst wirkt, das die beweglichen Teile ausrichtet.
Wie GTR1 seine Fracht erkennt
Das Team untersuchte, wie GTR1 zwei repräsentative Glucosinolate mit unterschiedlichen Seitenketten bindet. Beide wurden in derselben zentralen Tasche lokalisiert. Die Zucker‑ und die negativ geladene Sulfatgruppe — Merkmale, die nahezu alle Glucosinolate teilen — werden von einem Cluster positiv geladener und polarer Aminosäuren an einer Seite der Kavität gehalten. Durch systematische Veränderung dieser Reste zeigten die Autoren, dass zwei davon, darunter ein Lysin, das Teil einer charakteristischen Sequenz dieser Transporterfamilie ist, für den Transport entscheidend sind. Dagegen erwiesen sich Aminosäuren, die die variablen Seitenketten berühren, als weniger wichtig für die Aktivität, was erklärt, wie GTR1 viele Glucosinolate verarbeiten kann. Subtile Unterschiede an den Seitenketten‑kontaktierenden Positionen zwischen GTR1, GTR2 und GTR3 dürften einstellen, welche spezifischen Glucosinolate jeder Transporter bevorzugt.
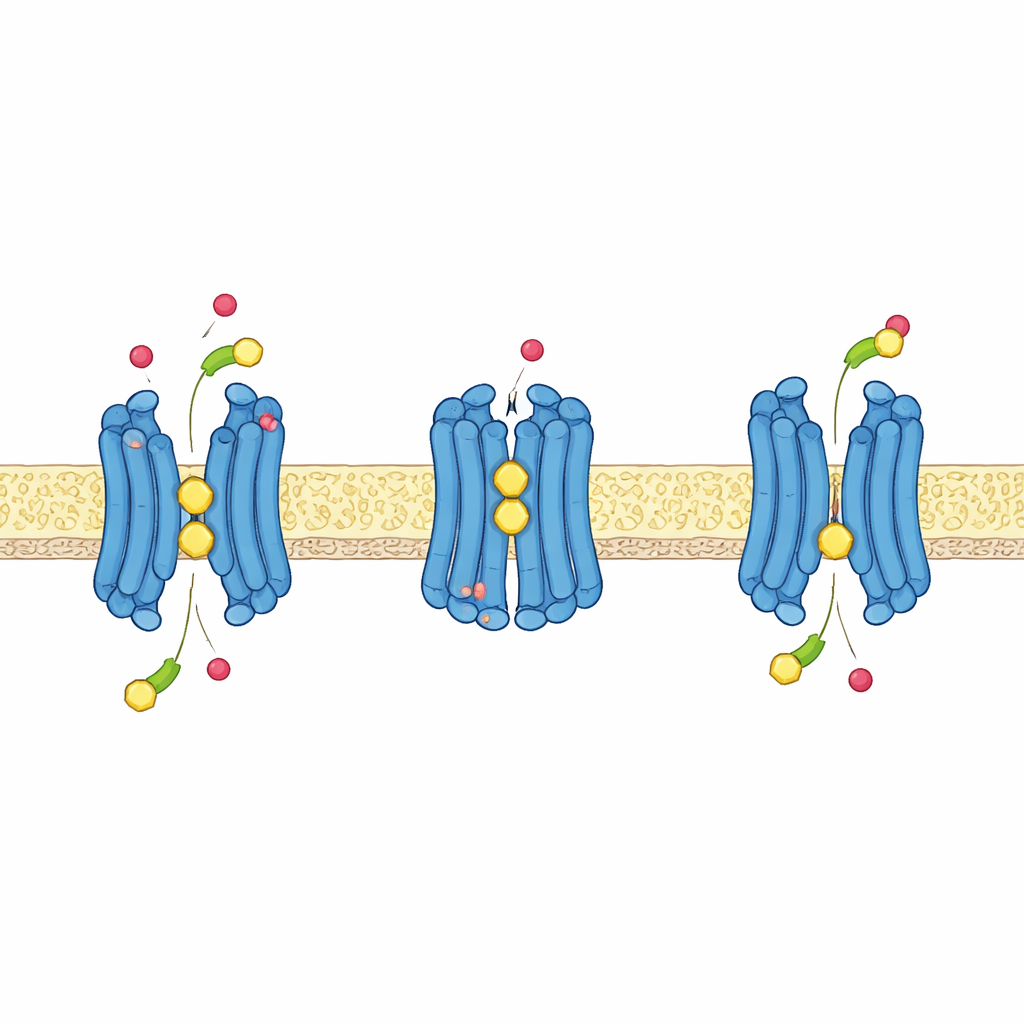
Protonen als Antriebsquelle für den Transport
Wie viele Nährstofftransporter in Pflanzen nutzt GTR1 die in einem Protonengradienten gespeicherte Energie — mehr Protonen außerhalb als innerhalb der Zelle — um Glucosinolate aktiv nach innen zu ziehen. Die Strukturen, kombiniert mit Computersimulationen und Transporttests bei unterschiedlichen pH‑Werten, zeigen, wie dies auf atomarer Ebene funktioniert. Ein kurzer Abschnitt von Aminosäuren nahe der Oberseite der zentralen Kavität, der zwei Glutamate und ein Lysin enthält, ordnet sich um, wenn das Protein zwischen nach außen‑ und nach innen‑geöffneter Konformation wechselt. Wenn bestimmte Glutamate Protonen aufnehmen, lösen sie ihre Wechselwirkung mit dem Lysin, wodurch dieses frei wird, die negativ geladene Sulfatgruppe der Glucosinolate mitzuhelfen zu binden und das Schließen des Proteins um seine Fracht zu fördern. Ein weiteres Glutamat, tiefer im Protein, bildet eine Schlüsselpartnerschaft mit einer benachbarten Tyrosin‑Seitenkette; wenn diese Stelle protoniert ist, unterstützt sie den Übergang vom nach außen‑gerichteten zum nach innen‑gerichteten Zustand und macht den Prozess empfindlich gegenüber dem elektrischen Membranpotenzial der Zelle.
Von atomaren Bildern zu besseren Nutzpflanzen
Zusammen stützen diese Ergebnisse ein Alternating‑Access‑Modell, in dem GTR1 zyklisch zwischen nach außen geöffneten, verschlossenen und nach innen geöffneten Formen wechselt, während Protonen und Glucosinolate mittransportiert werden. Indem die Studie genau herausarbeitet, welche Proteinmerkmale das gemeinsame Glucosinolat‑„Rückgrat“ erkennen, welche die Seitenkettenpräferenzen einstellen und welche den Transport an den Protonenfluss koppeln, liefert sie einen detaillierten Bauplan für die gezielte Steuerung des Glucosinolattransports in Pflanzen. Praktisch könnte dieses Wissen genutzt werden, um Pflanzen zu züchten oder zu entwerfen, deren Samen weniger bittere, anti‑nährstoffliche Glucosinolate anreichern, während Blätter und Stängel starke chemische Abwehr gegen Insekten behalten — was Landwirten robuste Pflanzen bringt, die zugleich als Lebensmittel und Futtermittel wertvoller sind.
Zitation: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Schlüsselwörter: Glucosinolate, Pflanzentransporter, GTR1, Pflanzenverbesserung, protonenkopplter Transport