Clear Sky Science · pl
Strukturalne podstawy rozpoznawania i transportu glukozynolanów przez roślinny białkowy GTR1
Roślinne tarcze z ukrytym kosztem
Wiele warzyw na naszych talerzach — od musztardowych liści po roślinę macierzystą oleju rzepakowego — broni się przy pomocy rodziny pikantnych, zawierających siarkę związków zwanych glukozynolanami. Związki te mogą odstraszać owady i mieć nawet korzystne działanie dla zdrowia ludzi, ale w paszach dla zwierząt i niektórych uprawach bywają uznawane za antyodżywcze. W badaniu tym ujawniono w atomowych detalach, jak maleńkie białko‑strażnik w komórkach roślinnych, zwane GTR1, rozpoznaje i transportuje glukozynolany, otwierając drogę do upraw lepiej chronionych, a jednocześnie bardziej pożywnych.
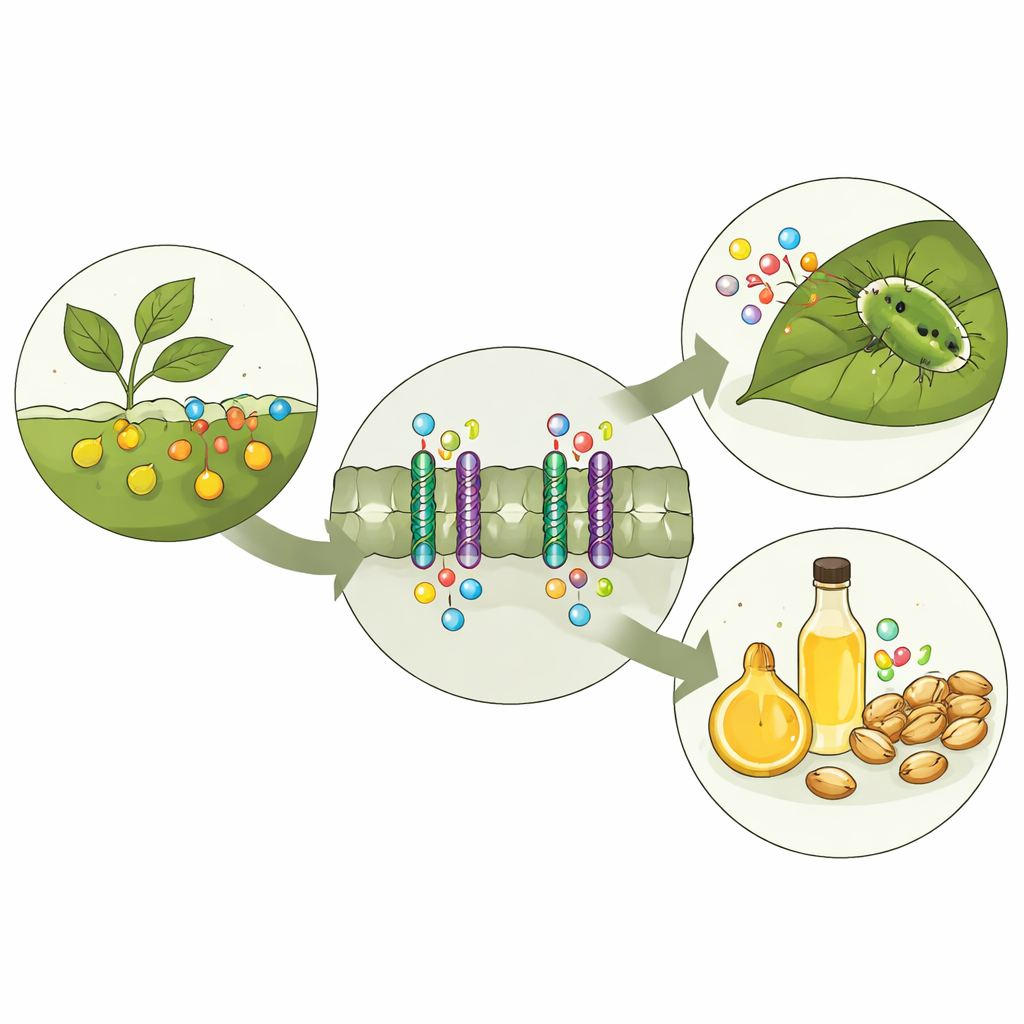
Chemiczny system ochronny w roślinach
Glukozynolany przechowywane są oddzielnie od enzymów, które je rozkładają. Gdy owad przegryzie liść, przegrody ulegają naruszeniu, a glukozynolany są szybko przekształcane w ostro‑smakowe, czasem toksyczne produkty, które zniechęcają dalsze żerowanie. Aby ta obrona działała, rośliny muszą przemieszczać glukozynolany z miejsca ich syntezy do miejsc, gdzie są potrzebne, takich jak nasiona czy wyspecjalizowane komórki magazynujące. W modelowej roślinie Arabidopsis za ten transport odpowiadają trzy spokrewnione białka‑transportery: GTR1, GTR2 i GTR3. Wcześniejsze badania genetyczne wykazały, że gdy te transportery są zaburzone, zmieniają się poziomy i rozmieszczenie glukozynolanów w roślinie, co wpływa zarówno na obronę, jak i na jakość nasion.
Bramka w ścianie komórkowej
GTR1 znajduje się w błonie komórkowej i działa jak obrotowe drzwi, sprzęgając pobieranie glukozynolanów z przepływem protonów (jonów wodoru) przez błonę. Dzięki krio‑elektronowej mikroskopii autorzy uzyskali cztery trójwymiarowe migawki Arabidopsis GTR1: dwie bez ładunku (jedną otwartą na zewnątrz, drugą otwartą do wnętrza) oraz dwie z związanymi glukozynolanami. Obrazy te ujawniają, że GTR1 ma rdzeń złożony z dwunastu segmentów przecinających błonę tworzących centralną jamę, otoczoną dużą „domeną wewnątrzkomórkową”, która przylega do jednej z helis. Poprzez obcinanie tej domeny lub zmianę kluczowych punktów kontaktu badacze wykazali, że jest ona niezbędna dla prawidłowego transportu, prawdopodobnie działając jako stabilizujący stelaż utrzymujący ruchome części we właściwym układzie.
Jak GTR1 rozpoznaje swój ładunek
Zespół badał, jak GTR1 wiąże dwa reprezentatywne glukozynolany o różnych łańcuchach bocznych. Oba znaleziono umieszczone w tej samej centralnej kieszeni. Cukrowa i naładowana część siarczynowa — cechy wspólne niemal wszystkich glukozynolanów — są chwytane przez skupisko dodatnio naładowanych i polarnego charakteru aminokwasów po jednej stronie jamy. Poprzez systematyczną zmianę tych reszt autorzy pokazali, że dwa z nich, w tym lizyna będąca częścią charakterystycznej sekwencji wspólnej dla tej rodziny transporterów, są kluczowe dla transportu. Natomiast aminokwasy stykające się ze zmiennymi łańcuchami bocznymi okazały się mniej istotne dla aktywności, co wyjaśnia, jak GTR1 może obsługiwać wiele glukozynolanów. Subtelne różnice w pozycjach kontaktujących łańcuchy boczne między GTR1, GTR2 i GTR3 prawdopodobnie dostrajają preferencje poszczególnych białek względem konkretnych glukozynolanów.
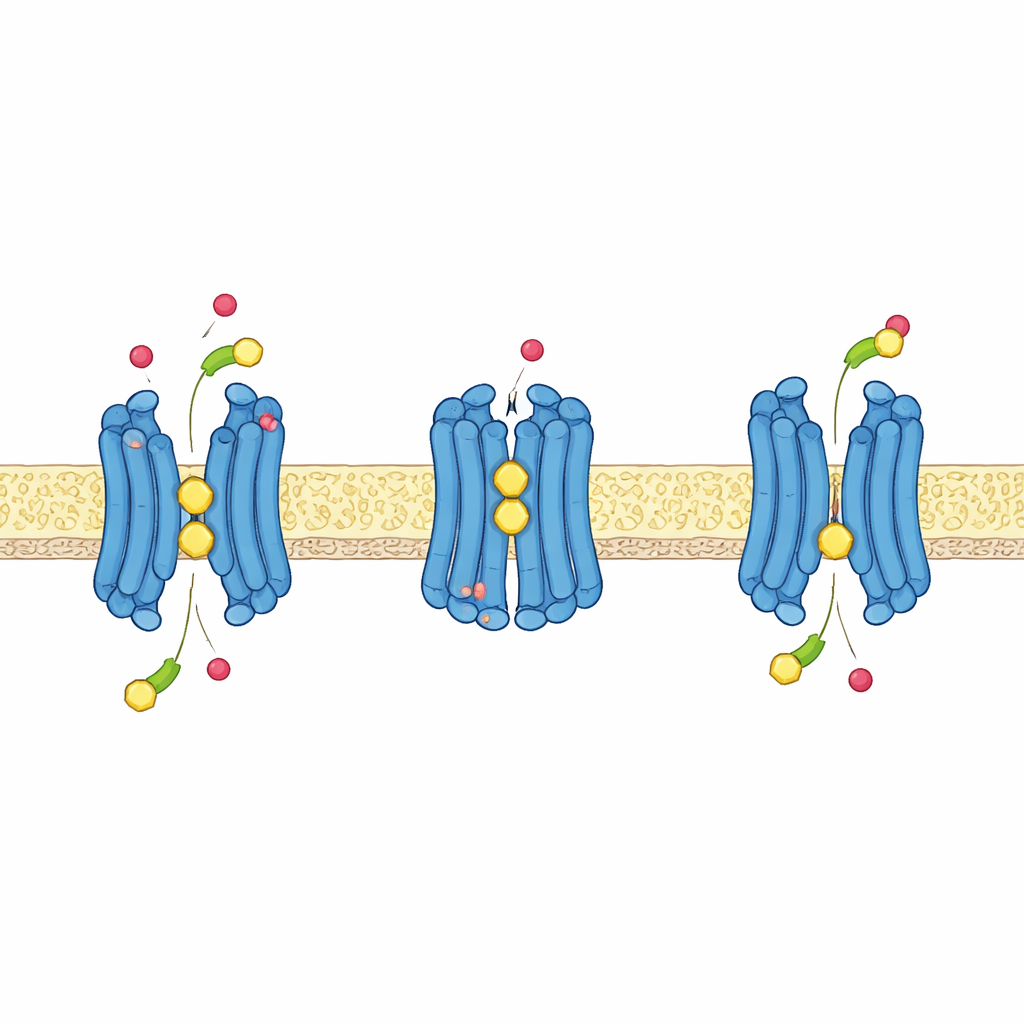
Wykorzystywanie protonów jako napędu transportu
Podobnie jak wiele transporterów składników odżywczych w roślinach, GTR1 wykorzystuje energię zgromadzoną w gradiencie protonowym — większe stężenie protonów na zewnątrz niż wewnątrz komórki — aby aktywnie pobierać glukozynolany do wnętrza. Struktury, połączone z symulacjami komputerowymi i testami transportu przy różnych poziomach kwasowości, pokazują, jak to działa na poziomie atomowym. Krótki fragment aminokwasów blisko wierzchu centralnej jamy, zawierający dwie glutaminy i lizynę, przeorganizowuje się, gdy białko przełącza się między stanami otwartymi na zewnątrz i do wnętrza. Gdy niektóre z glutamin przyjmują protony, tracą swoje wiązanie z lizyną, co uwalnia ją do pomocy w wiązaniu ujemnie naładowanej grupy siarczanowej glukozynolanów i sprzyja zamknięciu białka wokół ładunku. Inna glutamina, położona głębiej w białku, tworzy kluczowe partnerstwo z pobliską tyrozyną; po uwzględnieniu protonu to miejsce pomaga napędzać przejście transportera ze stanu otwartego na zewnątrz do stanu otwartego do wnętrza i czyni proces wrażliwym na potencjał elektryczny komórki.
Od obrazów atomowych do lepszych upraw
Razem te wyniki wspierają model alternującego dostępu, w którym GTR1 cykluje przez stany otwarte na zewnątrz, zablokowane i otwarte do wnętrza, współtransportując protony i glukozynolany. Wyjaśniając dokładnie, które cechy białka rozpoznają wspólny „kręgosłup” glukozynolanów, które regulują preferencje względem łańcuchów bocznych oraz które sprzęgają transport z przepływem protonów, badanie dostarcza szczegółowego planu inżynieryjnego dla modulacji ruchu glukozynolanów w roślinach. W praktyce tę wiedzę można wykorzystać do hodowli lub projektowania upraw, których nasiona akumulują mniej gorzkich, antyodżywczych glukozynolanów, podczas gdy liście i łodygi zachowują silne chemiczne zabezpieczenia przed owadami — oferując rolnikom rośliny jednocześnie bardziej wytrzymałe w polu i cenniejsze jako żywność i pasza.
Cytowanie: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Słowa kluczowe: glukozynolany, transportery roślinne, GTR1, poprawa roślin uprawnych, transport sprzężony z protonami