Clear Sky Science · ru
Структурные основания распознавания и транспорта глюкозинолатов белком GTR1 растений
Растительные щиты с скрытой ценой
Многие овощи на нашем столе — от листовой горчицы до исходного растения для производства рапсового масла — защищают себя семейством острых, бедных серой соединений, называемых глюкозинолатами. Эти вещества отпугивают голодных насекомых и даже могут приносить пользу человеку, но в корме для животных и в некоторых культурах их считают анти‑питательными факторами. В этом исследовании раскрывается в атомных деталях, как крошечный «привратник» в клетках растений, белок GTR1, распознаёт и перемещает глюкозинолаты, что открывает путь к культурам, одновременно лучше защищённым и более питательным.
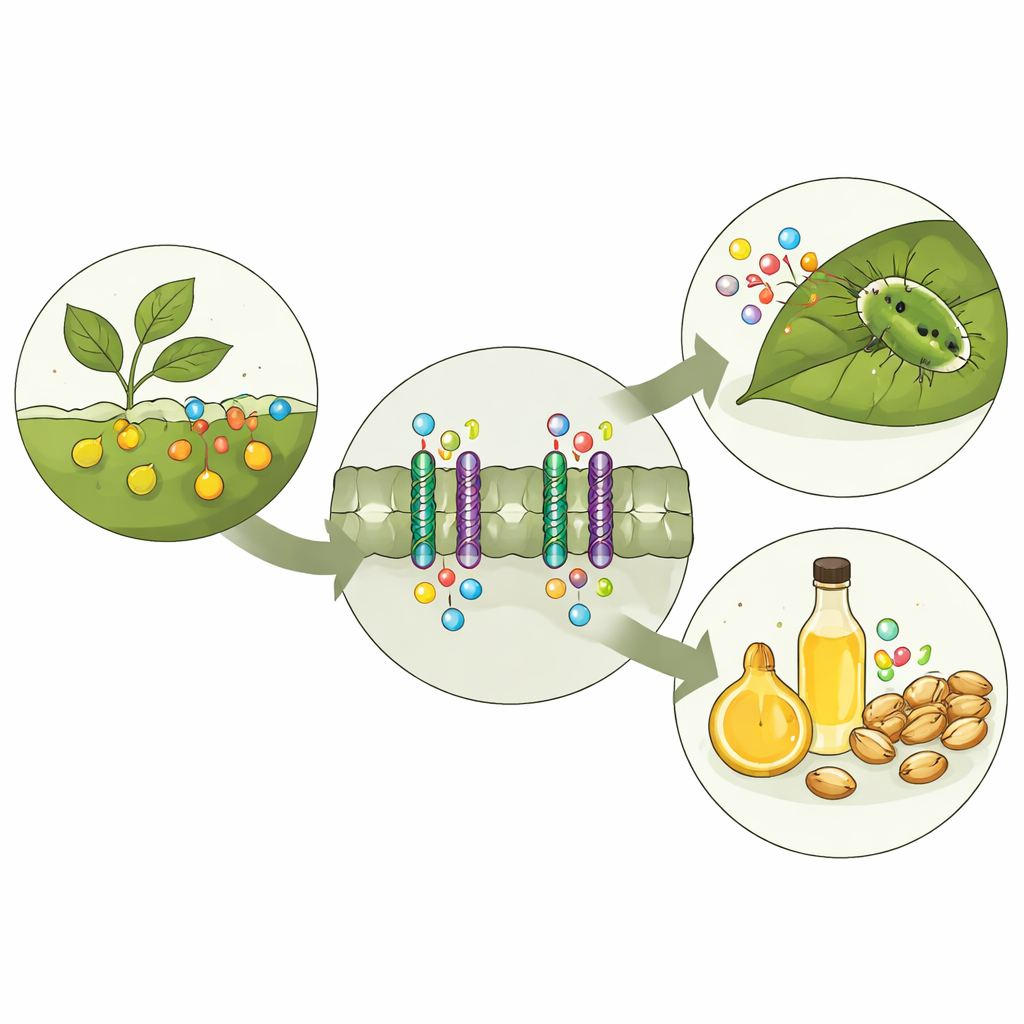
Химическая система безопасности в растениях
Глюкозинолаты хранятся отдельно от ферментов, которые их разрушают. Когда насекомое перекусывает лист, отсеки разрываются, и глюкозинолаты быстро превращаются в острые на вкус и иногда токсичные продукты, что отпугивает дальнейшее поедание. Чтобы эта защита работала, растения должны транспортировать глюкозинолаты от места синтеза к месту потребления — например, в семена и специализированные клетки‑депо. В модельном растении Arabidopsis эту задачу выполняют три родственных транспортёра GTR1, GTR2 и GTR3. Ранние генетические исследования показали, что при нарушении работы этих белков уровни и распределение глюкозинолатов по растению меняются, что влияет и на защиту, и на качество семян.
Врата в клеточной стенке
GTR1 располагается в плазматической мембране клетки и работает как вращающаяся дверь, связывая захват глюкозинолатов с потоком протонов (ионов водорода) через мембрану. С помощью крио‑электронной микроскопии авторы получили четыре трёхмерных «моментальных снимка» GTR1 из Arabidopsis: два без груза (одно обращено наружу, другое внутрь) и два с связанными глюкозинолатами. Эти изображения показывают, что у GTR1 есть сердцевина из двенадцати спиралей, пересекающих мембрану, формирующих центральную полость, окружённую большой «внутриклеточной доменом», прижатым к одной из спиралей. Укорачивание этого домена или изменение ключевых контактных точек продемонстрировало, что он необходим для корректного транспорта, вероятно выполняя роль стабилизирующего каркаса, который удерживает подвижные части в нужной ориентации.
Как GTR1 распознаёт свой груз
Группа изучила, как GTR1 связывает два представительных глюкозинолата с разными боковыми цепями. Оба оказались расположенными в одной и той же центральной кармане. Сахарная и заряженная сульфатная части — признаки, общие почти для всех глюкозинолатов — захватываются кластером положительно заряженных и полярных аминокислот с одной стороны полости. Путём систематического изменения этих остатков авторы показали, что два из них, включая лизин, входящий в характерную для этого семейства транспортёров последовательность, критически важны для транспорта. Напротив, аминокислоты, контактирующие с переменными боковыми цепями, оказались менее значимы для активности, что объясняет способность GTR1 работать с множеством различных глюкозинолатов. Тонкие различия в положениях, контактирующих с боковыми цепями, между GTR1, GTR2 и GTR3, вероятно, определяют предпочтения каждого из белков по конкретным глюкозинолатам.
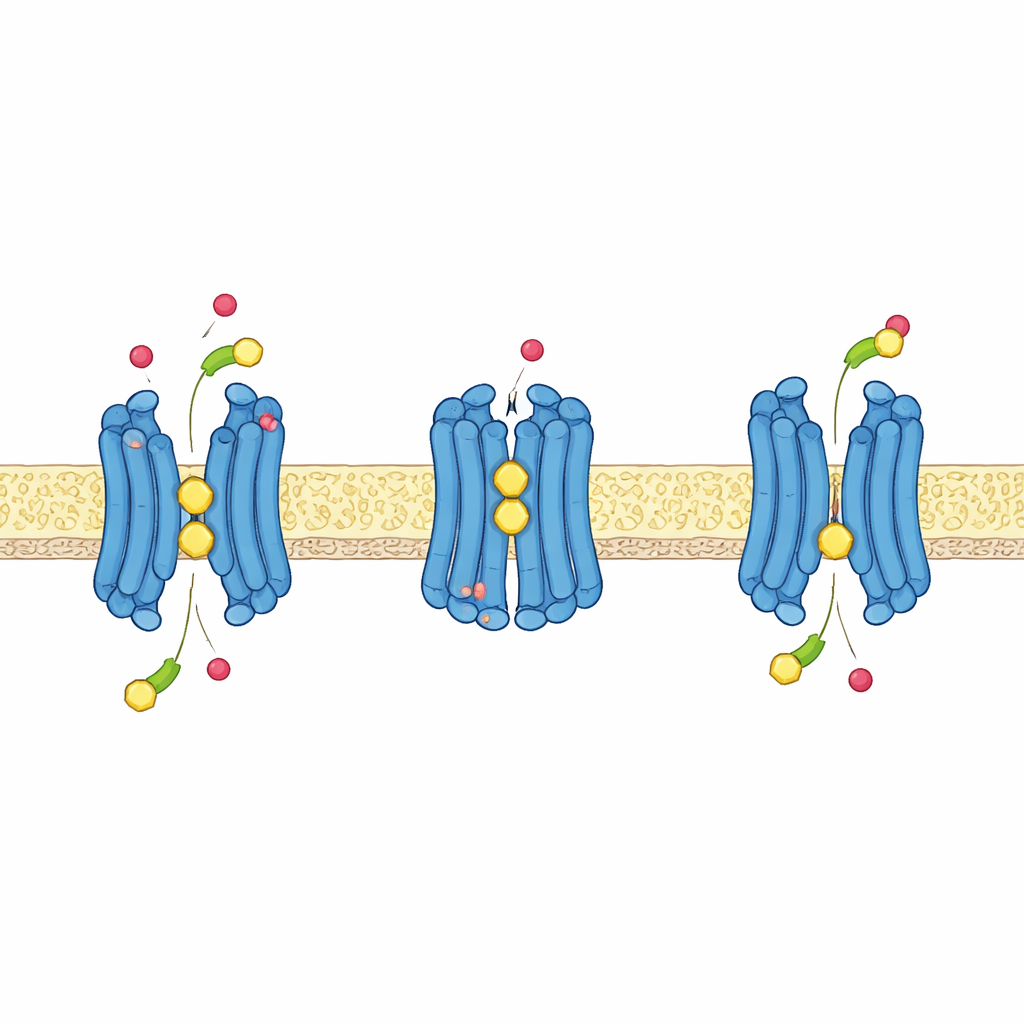
Использование протонов для приведения транспорта в действие
Как и многие питательные транспортёры в растениях, GTR1 использует энергию, заключённую в протонном градиенте — когда снаружи клетки больше протонов, чем внутри — чтобы активно втягивать глюкозинолаты внутрь. Структуры в сочетании с компьютерными моделями и тестами транспорта при разных уровнях кислотности раскрывают, как это работает на атомном уровне. Короткий участок аминокислот у вершины центральной полости, включающий два глутамата и лизин, перестраивается при переключении белка между наружным и внутренним состояниями. Когда некоторые глутаматы присоединяют протоны, они ослабевают свою связь с лизином, освобождая его для помощи в связывании отрицательно заряженной сульфатной группы глюкозинолатов и способствуя «запиранию» белка вокруг груза. Другой глутамат, расположенный глубже в белке, формирует ключевое партнёрство с соседним тирозином; при протонировании этот сайт помогает приводить транспортёр из наружно‑открытого в внутрь‑открытое состояние и делает процесс чувствительным к мембранному потенциалу клетки.
От атомных снимков к лучшим культурам
В совокупности эти результаты поддерживают модель чередующегося доступа, при которой GTR1 проходит циклы наружно‑открытого, окклюдированного и внутрь‑открытого состояний, ко‑транспортируя протоны и глюкозинолаты. Проясняя, какие именно элементы белка распознают общий «скелет» глюкозинолатов, какие настраивают предпочтения к боковым цепям и какие связывают транспорт с потоком протонов, исследование даёт детальную схему для инженерии перемещения глюкозинолатов в растениях. В практическом плане эти знания можно использовать при селекции или дизайне культур, семена которых накапливают меньше горьких, анти‑питательных глюкозинолатов, тогда как листья и стебли сохраняют сильную химическую защиту от насекомых — что даёт фермерам растения, более стойкие в поле и более ценны как пища и корм.
Цитирование: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Ключевые слова: глюкозинолаты, транспортёры растений, GTR1, улучшение сельхозкультур, протоно‑зависимый транспорт