Clear Sky Science · pt
Base estrutural do reconhecimento e transporte de glucosinolatos pela GTR1 vegetal
Escudos vegetais com um custo oculto
Muitas das hortaliças no nosso prato, desde folhas de mostarda até a planta‑pai do óleo de canola, a colza, defendem‑se com uma família de compostos picantes e ricos em enxofre chamados glucosinolatos. Essas substâncias podem deter insetos famintos e até apresentar benefícios à saúde humana, mas em rações animais e em algumas culturas são consideradas antinutrientes. Este estudo revela, em detalhe atômico, como uma pequena proteína porteira nas células vegetais, chamada GTR1, reconhece e movimenta glucosinolatos, abrindo caminho para plantas cultivadas que sejam ao mesmo tempo melhor defendidas e mais nutritivas.
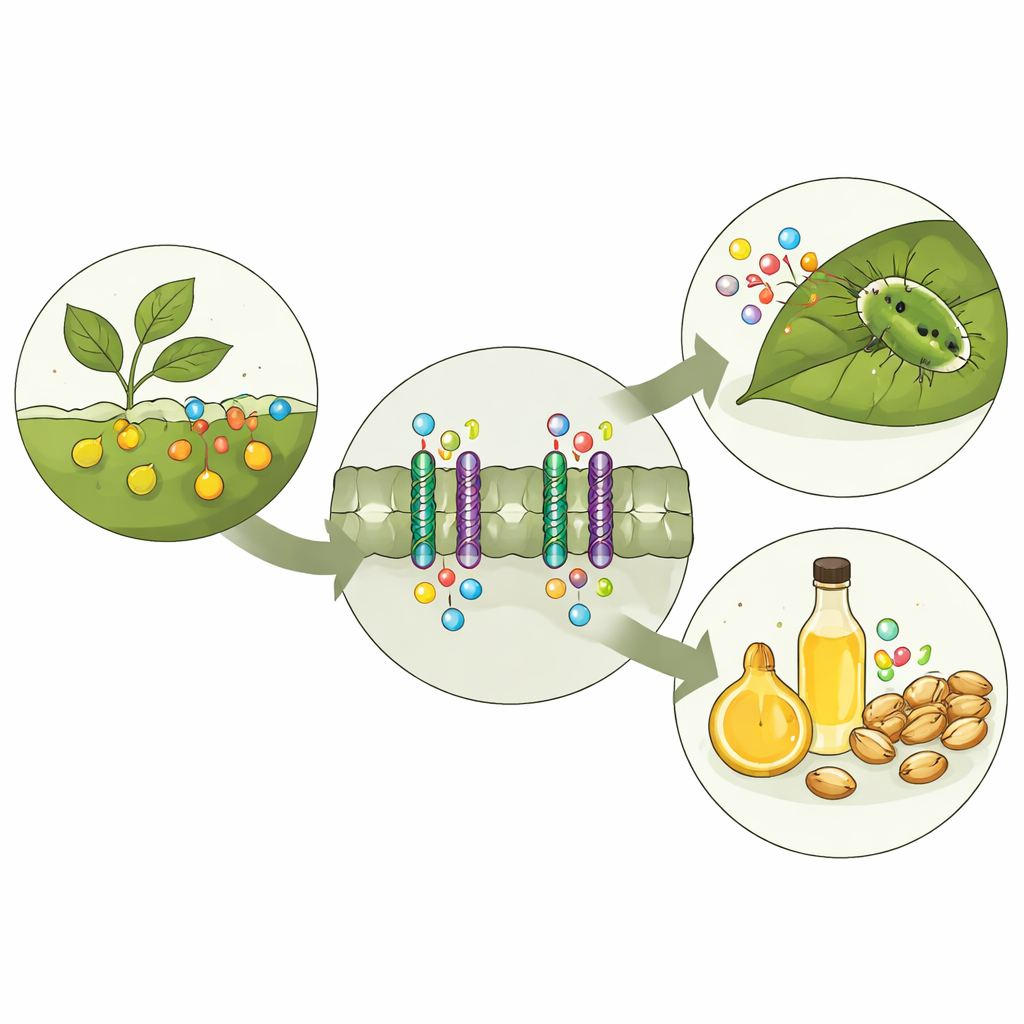
Um sistema químico de segurança nas plantas
Os glucosinolatos são armazenados separadamente das enzimas que os degradam. Quando um inseto mastiga uma folha, os compartimentos se rompem e os glucosinolatos são rapidamente convertidos em produtos de sabor cortante e às vezes tóxicos que desencorajam a continuação da alimentação. Para que essa defesa funcione, as plantas precisam transportar glucosinolatos de onde são sintetizados até onde são necessários, como sementes e células de armazenamento especializadas. Na planta modelo Arabidopsis, três transportadores relacionados — GTR1, GTR2 e GTR3 — cumprem essa função. Trabalhos genéticos anteriores mostraram que, quando esses transportadores são perturbados, os níveis e os padrões de glucosinolatos na planta mudam, alterando tanto a defesa quanto a qualidade das sementes.
A porta na parede celular
A GTR1 localiza‑se na membrana externa da célula e atua como uma porta giratória que acopla a captação de glucosinolatos ao fluxo de prótons (íons de hidrogênio) através da membrana. Usando crio‑microscopia eletrônica, os autores capturaram quatro instantâneos tridimensionais da GTR1 de Arabidopsis: dois sem carga (um aberto para o lado externo, outro aberto para o lado interno) e dois com glucosinolatos ligados. Essas imagens revelam que a GTR1 tem um núcleo de doze segmentos transmembranares que formam uma cavidade central, rodeada por um grande “domínio intracelular” que se apoia contra uma das hélices. Ao aparar esse domínio ou alterar pontos de contato chave, os pesquisadores mostraram que ele é essencial para o transporte adequado, provavelmente atuando como um andaime estabilizador que mantém as partes móveis alinhadas.
Como a GTR1 reconhece sua carga
A equipe examinou como a GTR1 se liga a dois glucosinolatos representativos com cadeias laterais diferentes. Ambos foram encontrados alojados na mesma bolsa central. As porções de açúcar e o grupo sulfato carregado — características compartilhadas por praticamente todos os glucosinolatos — são seguradas por um aglomerado de aminoácidos positivamente carregados e polares em um lado da cavidade. Ao alterar sistematicamente esses resíduos, os autores demonstraram que dois deles, incluindo uma lisina que faz parte de uma sequência marcante compartilhada por essa família de transportadores, são cruciais para o transporte. Em contraste, aminoácidos que tocam as cadeias laterais variáveis mostraram‑se menos importantes para a atividade, explicando como a GTR1 pode lidar com muitos glucosinolatos. Diferenças sutis nas posições que contatam as cadeias laterais entre GTR1, GTR2 e GTR3 provavelmente ajustam quais glucosinolatos específicos cada proteína prefere.
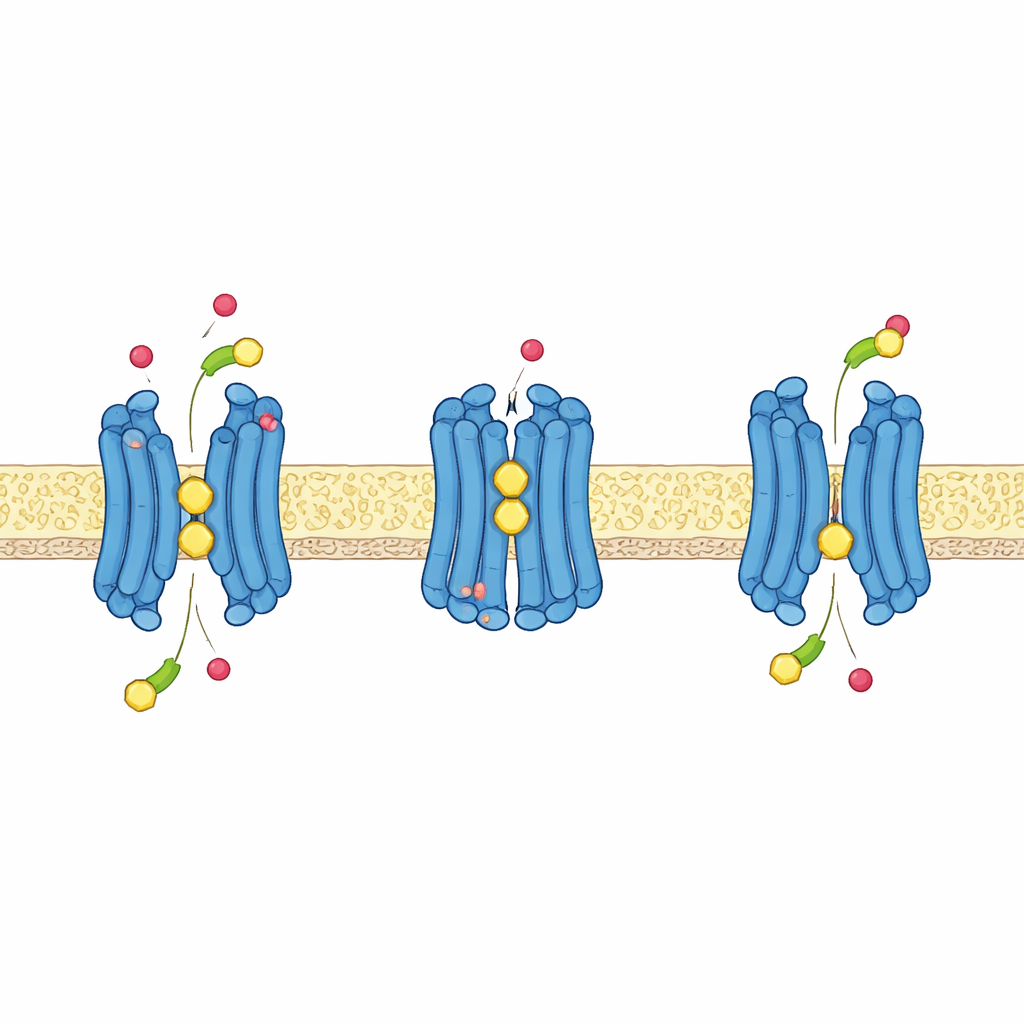
Usando prótons para impulsionar o transporte
Como muitos transportadores de nutrientes em plantas, a GTR1 aproveita a energia armazenada em um gradiente de prótons — mais prótons fora da célula do que dentro — para puxar ativamente glucosinolatos para o interior. As estruturas, combinadas com simulações computacionais e testes de transporte em diferentes níveis de acidez, revelam como isso funciona em nível atômico. Um trecho curto de aminoácidos próximo ao topo da cavidade central, contendo dois glutamatos e uma lisina, reorganiza‑se conforme a proteína alterna entre estados voltados para fora e para dentro. Quando certos glutamatos capturam prótons, eles relaxam sua interação com a lisina, liberando‑a para ajudar a ligar o grupo sulfato negativamente carregado dos glucosinolatos e encorajando a proteína a fechar‑se em torno de sua carga. Outro glutamato, mais profundo na proteína, forma uma parceria chave com uma tirosina próxima; quando protonado, esse sítio ajuda a impulsionar o transportador do estado voltado para fora para o estado voltado para dentro e torna o processo sensível à voltagem elétrica da célula.
Das imagens atômicas a culturas melhores
Em conjunto, esses resultados apoiam um modelo de acesso alternado em que a GTR1 cicla por formas abertas para fora, ocluídas e abertas para dentro enquanto cotransporta prótons e glucosinolatos. Ao esclarecer exatamente quais características da proteína reconhecem o “esqueleto” comum dos glucosinolatos, quais ajustam as preferências por cadeias laterais e quais acoplam o transporte ao fluxo de prótons, o estudo fornece um roteiro detalhado para a engenharia do movimento de glucosinolatos nas plantas. Em termos práticos, esse conhecimento poderia ser usado para cultivar ou projetar plantas cujas sementes acumulem menos glucosinolatos amargos e antinutricionais, enquanto folhas e caules mantêm defesas químicas fortes contra insetos — oferecendo aos agricultores plantas mais resistentes no campo e mais valiosas como alimento e ração.
Citação: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Palavras-chave: glucosinolatos, transportadores vegetais, GTR1, melhoria de culturas, transporte acoplado a prótons