Clear Sky Science · nl
Structurele basis van herkenning en transport van glucosinolaten door plant GTR1
Plantaardige schilden met een verborgen prijs
Veel van de groenten op ons bord, van mosterdblad tot de koolzaadplant waaruit raapzaadolie wordt gewonnen, verdedigen zich met een familie pittige, zwavelrijke verbindingen die glucosinolaten worden genoemd. Deze stoffen kunnen hongerige insecten afschrikken en hebben mogelijk zelfs gezondheidsvoordelen voor mensen, maar in diervoeders en sommige gewassen gelden ze als anti‑nutriënten. Deze studie onthult op atomaire schaal hoe een klein poortwachtereiwit in plantencellen, genaamd GTR1, glucosinolaten herkent en transporteert, en biedt zo aanknopingspunten voor gewassen die zowel beter verdedigd als voedzamer zijn.
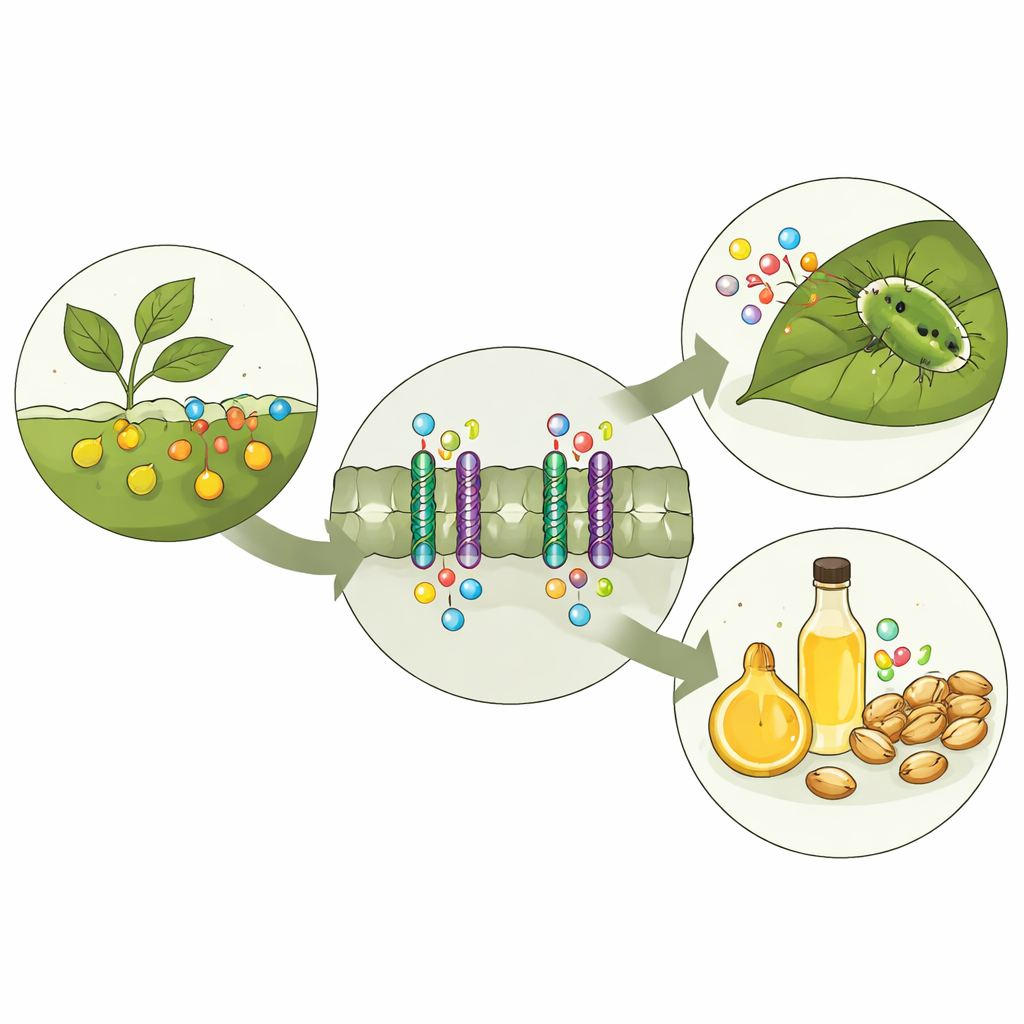
Een chemisch beveiligingssysteem in planten
Glucosinolaten worden apart opgeslagen van de enzymen die ze afbreken. Wanneer een insect op een blad kauwt, scheuren de compartimenten open en worden glucosinolaten snel omgezet in scherp smakende en soms toxische producten die verder vraat ontmoedigen. Om deze verdediging te laten werken moeten planten glucosinolaten verplaatsen van de plek waar ze zijn gemaakt naar de plekken waar ze nodig zijn, zoals zaden en gespecialiseerde opslagcellen. In de modelplant Arabidopsis verzorgen drie verwante transportereiwitten, GTR1, GTR2 en GTR3, deze taak. Eerder genetisch werk toonde aan dat wanneer deze transporters worden verstoord, de niveaus en verdeling van glucosinolaten in de plant veranderen, wat zowel de verdediging als de zaadkwaliteit beïnvloedt.
De poort in het celmembraan
GTR1 zit in het buitenste membraan van de cel en werkt als een draaitocht die de opname van glucosinolaten koppelt aan de stroom van protonen (waterstofionen) over het membraan. Met cryo‑elektronenmicroscopie vingen de auteurs vier driedimensionale momentopnamen van Arabidopsis GTR1: twee zonder lading (één naar buiten open, één naar binnen open) en twee met gebonden glucosinolaten. Deze beelden laten zien dat GTR1 een kern van twaalf membraan‑overspannende segmenten heeft die een centrale holte vormen, omgeven door een grote “intracellulaire domein” die tegen een van de helices aan ligt. Door dit domein te verkleinen of cruciale contactpunten te veranderen, toonden de onderzoekers aan dat het essentieel is voor goed transport en waarschijnlijk functioneert als een stabiliserend geraamte dat de bewegende onderdelen op hun plaats houdt.
Hoe GTR1 zijn lading herkent
Het team onderzocht hoe GTR1 twee representatieve glucosinolaten met verschillende zijketens bindt. Beide bleken in dezelfde centrale pocket te liggen. Het suikerdeel en het geladen sulfaatdeel — kenmerken die vrijwel alle glucosinolaten gemeen hebben — worden vastgegrepen door een cluster van positief geladen en polaire aminozuren aan één kant van de holte. Door deze residuen systematisch te veranderen, lieten de auteurs zien dat twee van hen, waaronder een lysine die deel uitmaakt van een kenmerkende sequentie in deze transporterfamilie, cruciaal zijn voor transport. Daarentegen bleken aminozuren die contact maken met de variabele zijketens minder belangrijk voor activiteit, wat verklaart hoe GTR1 veel verschillende glucosinolaten kan verwerken. Subtiele verschillen in deze zijketen‑contactpunten tussen GTR1, GTR2 en GTR3 stemmen waarschijnlijk af welke specifieke glucosinolaten elk eiwit prefereert.
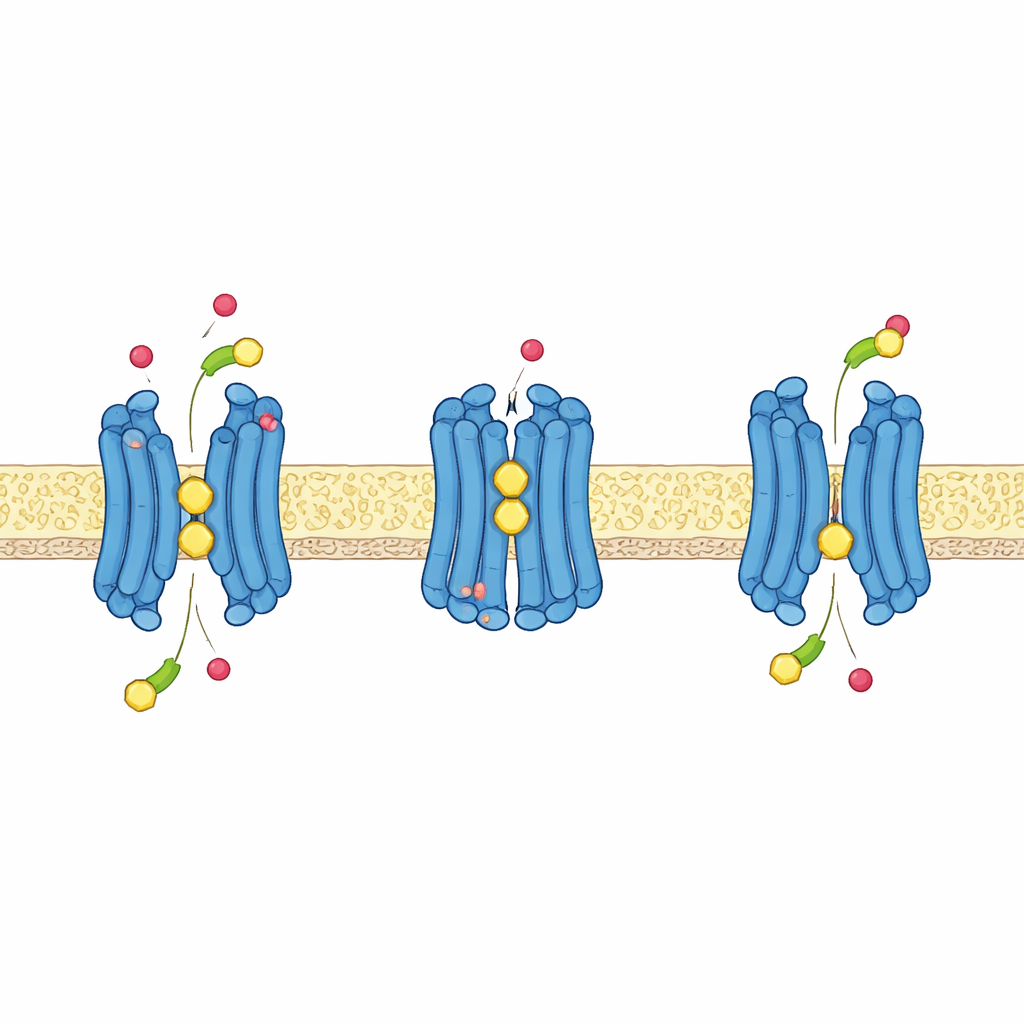
Protonen gebruiken om transport aan te drijven
Net als veel nutriëntentransporters in planten gebruikt GTR1 de energie die opgeslagen is in een protongraadient — meer protonen buiten de cel dan binnen — om actief glucosinolaten naar binnen te trekken. De structuren, gecombineerd met computatiesimulaties en transporteproeven bij verschillende zuurgraad, laten zien hoe dit op atomaire schaal werkt. Een korte keten aminozuren nabij de bovenkant van de centrale holte, met twee glutamaten en een lysine, herschikt zich wanneer het eiwit wisselt tussen naar‑buiten en naar‑binnen gerichte toestanden. Wanneer bepaalde glutamaten protonen opnemen, laten zij hun greep op de lysine los, waardoor deze vrij is om de negatief geladen sulfaatgroep van glucosinolaten te helpen binden en het eiwit aanmoedigt zich om zijn lading te sluiten. Een andere glutamaat, dieper in het eiwit, vormt een belangrijke partnerrelatie met een naburige tyrosine; wanneer deze wordt geprotoneerd helpt deze site het transporteerproces van naar‑buiten naar naar‑binnen te sturen en maakt het proces gevoelig voor de elektrische spanning van de cel.
Van atomische beelden naar betere gewassen
Gezamenlijk ondersteunen deze resultaten een alternerend‑toegangsmodel waarin GTR1 cycli door naar‑buiten open, geoccludeerd en naar‑binnen open vormen terwijl het protonen en glucosinolaten cotransporteert. Door precies te verduidelijken welke proteïnekenmerken de gemeenschappelijke glucosinolaath“ruggenwervel” herkennen, welke de voorkeur voor zijketens afstemmen en welke het transport koppelen aan protonstroom, levert de studie een gedetailleerd stappenplan voor het ontwerpen van glucosinolaattransport in planten. In praktische zin kan deze kennis worden gebruikt om gewassen te kruisen of te ontwerpen waarvan de zaden minder bittere, antinutritionele glucosinolaten ophopen terwijl bladeren en stengels sterke chemische afweer tegen insecten behouden — wat boeren planten biedt die zowel robuuster in het veld als waardevoller als voedsel en voer zijn.
Bronvermelding: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Trefwoorden: glucosinolaten, planttransporters, GTR1, gewasonwikkeling, protongekoppeld transport