Clear Sky Science · sv
Strukturell grund för igenkänning och transport av glukosinolater av växtproteinet GTR1
Växternas skydd med en dold kostnad
Många av grönsakerna på våra tallrikar, från senapsgröna blad till rapsplantan som ger rapsolja, försvarar sig med en familj av skarpa, svavelrika föreningar kallade glukosinolater. Dessa ämnen kan avskräcka hungriga insekter och kan även ge hälsofördelar för människor, men i djurfoder och vissa grödor betraktas de som antinutrienter. Denna studie avslöjar i atomär detalj hur ett litet grindvaktprotein i växtceller, kallat GTR1, känner igen och förflyttar glukosinolater, vilket öppnar vägen för grödor som både är bättre försvarade och mer näringsrika.
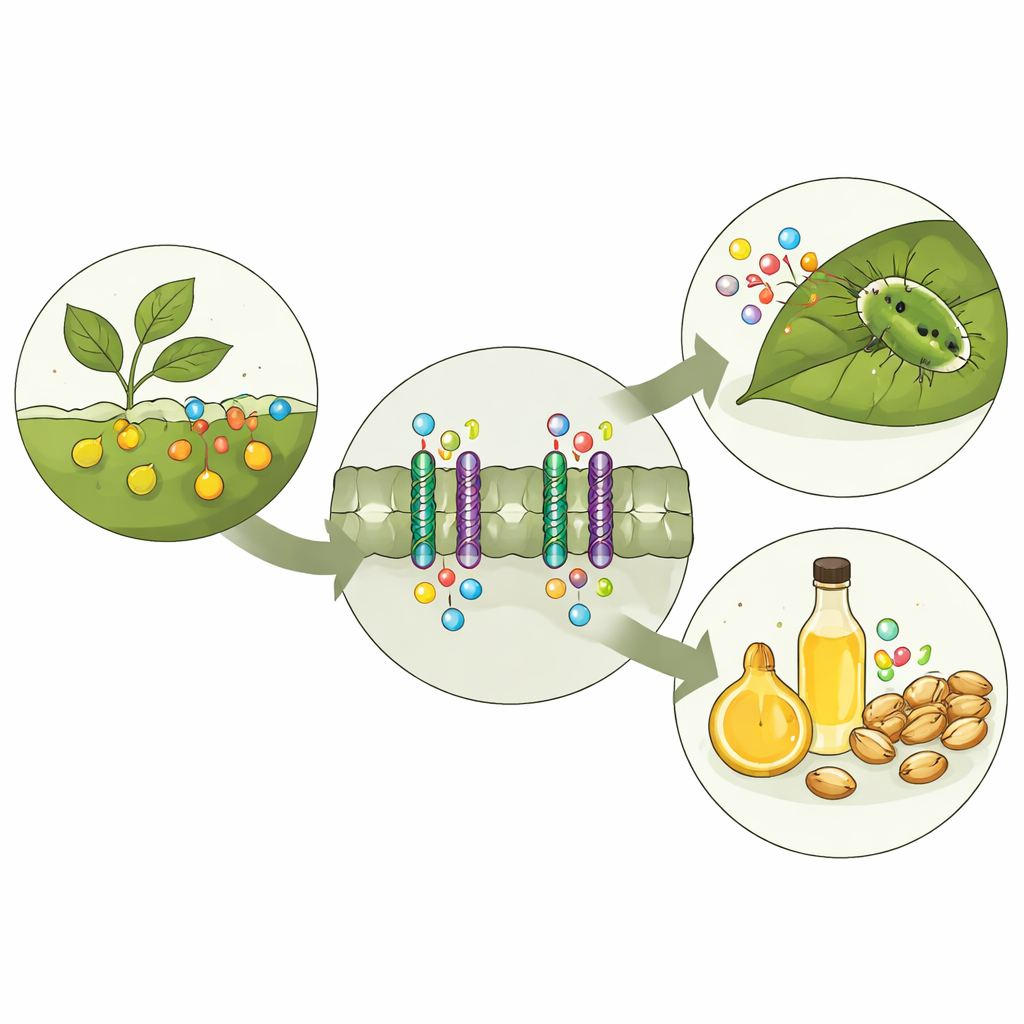
Ett kemiskt säkerhetssystem i växter
Glukosinolater lagras åtskilda från de enzymer som bryter ned dem. När en insekt gnager i ett blad rupturerar facken och glukosinolater omvandlas snabbt till skarpa och ibland giftiga produkter som avskräcker fortsatt betning. För att detta försvar ska fungera måste växter förflytta glukosinolater från där de bildas till där de behövs, såsom frön och specialiserade lagringsceller. I modellväxten Arabidopsis sköter tre besläktade transportproteiner, GTR1, GTR2 och GTR3, detta jobb. Tidigare genetiska studier visade att när dessa transportörer störs förändras mängden och fördelningen av glukosinolater i växten, vilket påverkar både försvar och frökvalitet.
Grinden i cellmembranet
GTR1 sitter i cellens yttre membran och fungerar som en snurrdörr som kopplar upptaget av glukosinolater till flödet av protoner (vätejoner) över membranet. Med hjälp av kryo-elektronmikroskopi fångade författarna fyra tredimensionella ögonblicksbilder av Arabidopsis GTR1: två utan last (en öppen mot utsidan, en öppen mot insidan) och två med bundna glukosinolater. Dessa bilder visar att GTR1 har en kärna av tolv membrangenomträngande segment som bildar ett centralt hålrum, omslutet av en stor ”intracellulär domän” som ligger an mot en av helixarna. Genom att trimma denna domän eller förändra viktiga kontaktpunkter visade forskarna att den är nödvändig för korrekt transport, sannolikt som ett stabiliserande skelett som håller de rörliga delarna i rätt läge.
Hur GTR1 känner igen sin last
Gruppen undersökte hur GTR1 binder två representativa glukosinolater med olika sidokedjor. Båda hittades inpassade i samma centrala ficka. Sockerdelen och den laddade sulfatdelen—egenskaper som delas av i princip alla glukosinolater—hålls fast av en klunga positivt laddade och polära aminosyror på ena sidan av hålrummet. Genom att systematiskt ändra dessa rester visade författarna att två av dem, inklusive en lysin som ingår i en typisk sekvens som delas av denna transportörfamilj, är avgörande för transporten. I kontrast var aminosyror som rör de varierande sidokedjorna mindre viktiga för aktiviteten, vilket förklarar hur GTR1 kan hantera många olika glukosinolater. Subtila skillnader i dessa positioner som kontaktar sidokedjor mellan GTR1, GTR2 och GTR3 troligen finjusterar vilka specifika glukosinolater varje protein föredrar.
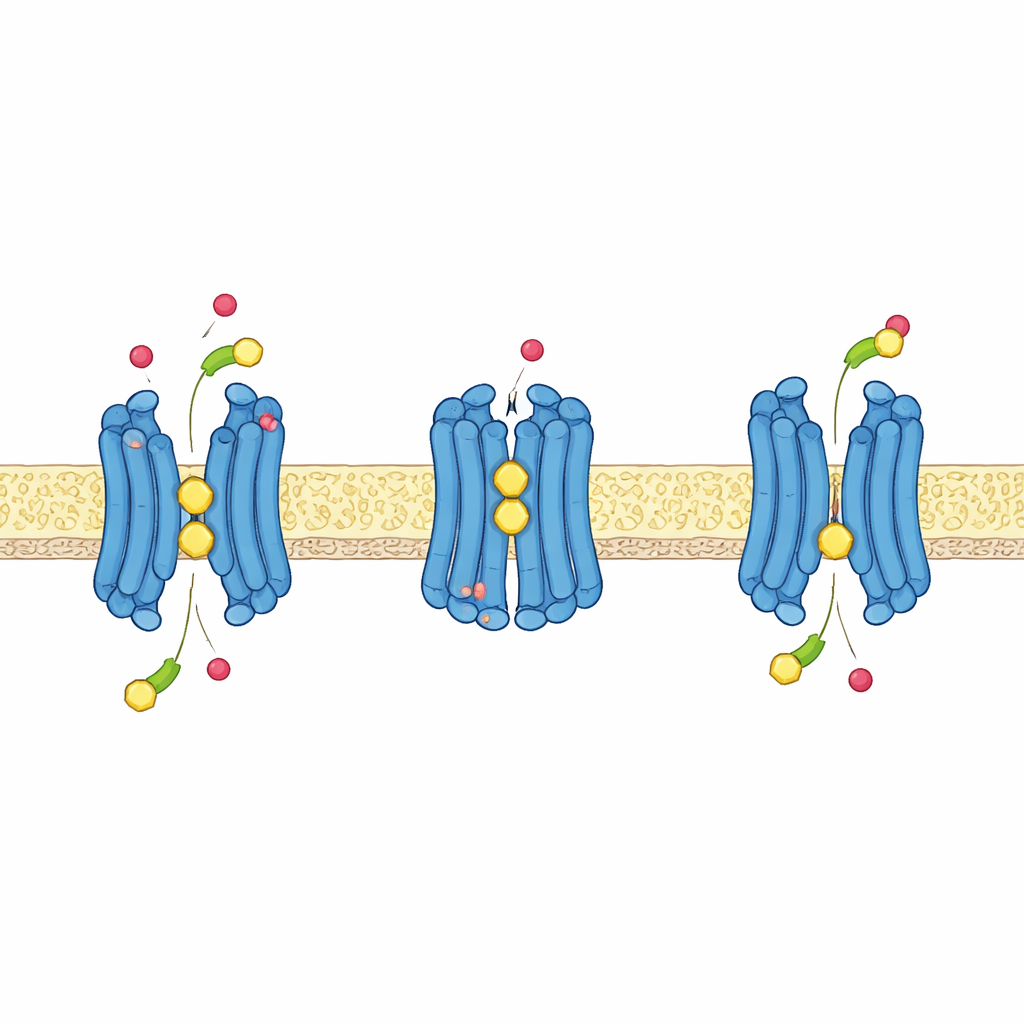
Använder protoner för att driva transporten
Liksom många näringstransportörer i växter utnyttjar GTR1 den energi som lagras i en protongradient—fler protoner utanför cellen än innanför—för att aktivt dra in glukosinolater. Strukturerna, kombinerade med datorsimuleringar och transporttester vid olika surhetsnivåer, visar hur detta fungerar på atomnivå. Ett kort streck av aminosyror nära toppen av det centrala hålrummet, som innehåller två glutamater och en lysin, omarrangeras när proteinet växlar mellan utåt- och inåtriktade tillstånd. När vissa glutamater tar upp protoner släpper de sitt grepp om lysinet, vilket frigör det att hjälpa till att binda den negativt laddade sulfatgruppen hos glukosinolater och uppmuntrar proteinet att sluta sig kring sin last. En annan glutamat längre in i proteinet bildar ett viktigt partnerskap med en närliggande tyrosin; när denna plats protoneras hjälper den till att driva transportören från det utåtvända till det inåtvända tillståndet och gör processen känslig för cellens elektriska spänning.
Från atomära bilder till bättre grödor
Tillsammans stöder dessa resultat en växelvis åtkomstmodell där GTR1 cyklar genom utåt-öppet, ockluderat och inåt-öppet former samtidigt som den samtransportera protoner och glukosinolater. Genom att klargöra exakt vilka proteinfunktioner som känner igen den gemensamma glukosinolat-”ryggraden”, vilka som ställer in sidokedjepreferenser och vilka som kopplar transporten till protonflödet, ger studien en detaljerad ritning för att designa glukosinolatförflyttning i växter. I praktiska termer skulle denna kunskap kunna användas för att avla eller designa grödor vars frön ackumulerar färre bittra, antinutritiva glukosinolater samtidigt som blad och stjälkar behåller starka kemiska försvar mot insekter—vilket ger jordbrukare växter som både är tåligare på fältet och mer värdefulla som livsmedel och foder.
Citering: Yan, R., Fan, J., Chi, C. et al. Structural basis of glucosinolate recognition and transport by plant GTR1. Cell Discov 12, 26 (2026). https://doi.org/10.1038/s41421-026-00884-7
Nyckelord: glukosinolater, växttransportörer, GTR1, grödförbättring, protonkopplad transport