Clear Sky Science · tr
Hastalıklarda NINJ1’in rolü
Hücrelerin Patlamayı Seçtiği An
Hücrelerimiz, yaşamın içini dış dünyadan ayrı tutan ince dış zarlarla sarılıdır. On yıllar boyunca bilim insanları, bu zarlar hücre ölümü sırasında nihayet yırtıldığında bunun şanssız bir patlama—balonun patlaması gibi—olduğunu varsaydılar. Bu derleme makalesi ise küçük bir zar proteini olan NINJ1’in yerleşik bir yıkım anahtarı gibi davrandığını gösteriyor. Hücrelerin ne zaman ve nasıl patlayacağını belirleyerek NINJ1, inflamasyon, sinir onarımı, damar büyümesi, enfeksiyon kontrolü ve hatta kanser üzerinde şekillendirici etkilere sahip—bu da onu gelecekteki ilaçlar için çekici ama karmaşık bir hedef yapıyor.
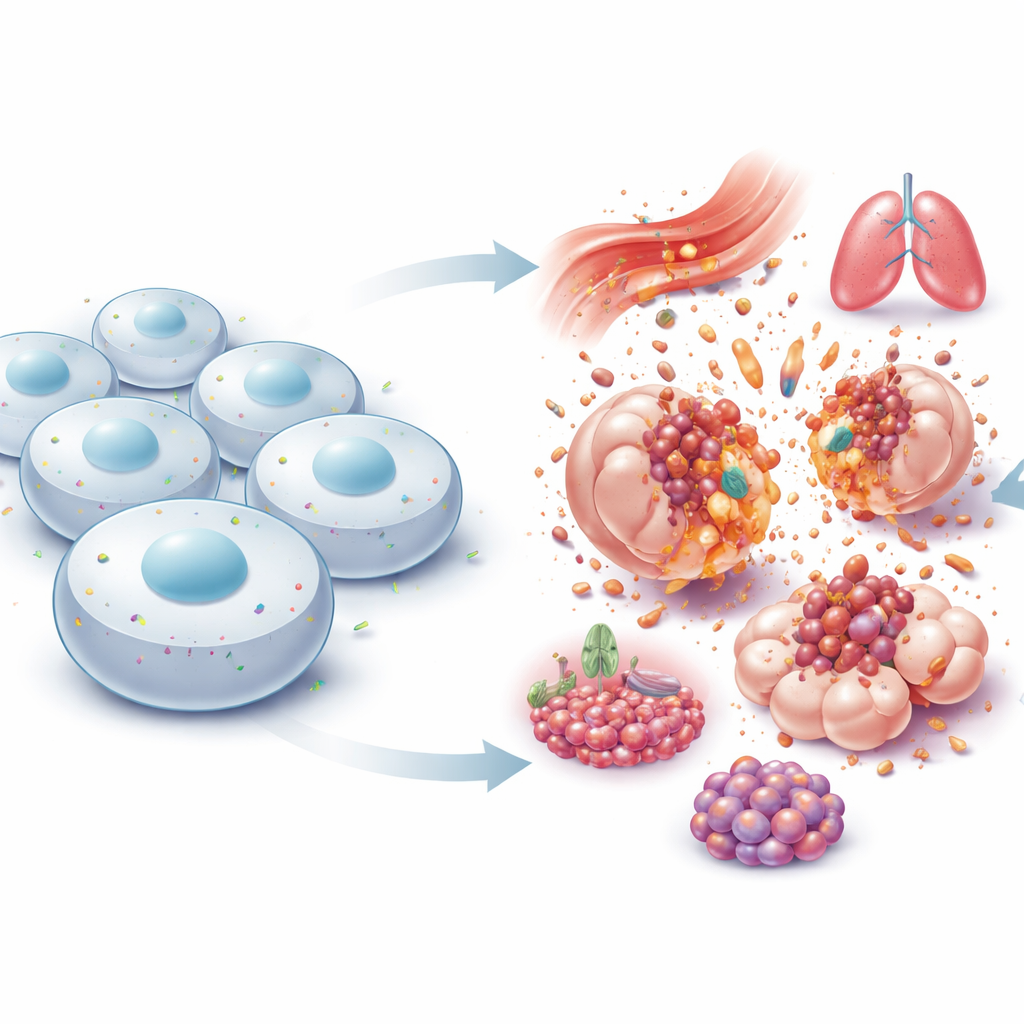
Hücrenin Kenarındaki Küçük Bir Kapıcı
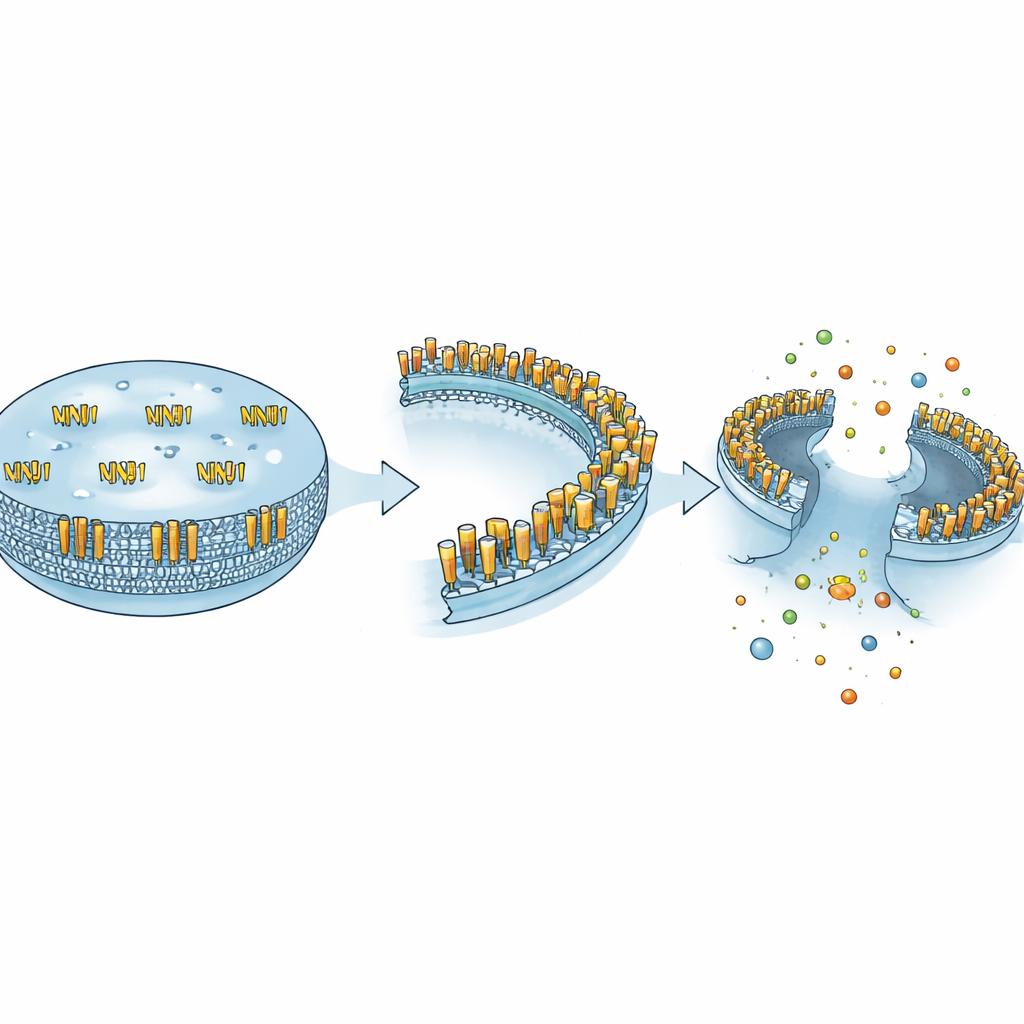
NINJ1 hücrelerin dış zarında bulunur ve ilk olarak yaralanmış sinirlerde keşfedilmiş; burada hasarlı liflerin yeniden uzamasına yardımcı oluyor gibi görünmüştür. Yıllarca hücrelerin birbirine tutunmasına izin veren basit bir “yapışkan” protein olarak ele alındı. Bu görüş 2021’de değişti; araştırmacılar NINJ1’in patlayıcı hücre ölümünün son yırtılmasının aktif uygulayıcısı olduğunu gösterdiler. Zar pasif olarak bozulmak yerine, NINJ1 molekülleri şekil değiştirir, büyük halka benzeri yapılar oluşturur ve zar parçalarını kesip çıkararak hücre içeriğinin çevre dokuya boşalmasına izin verir. Bu, tamamen tesadüfi bir yırtılma fikrini altüst eder ve lizitik hücre ölümünün son basamağının kendi içinde dikkatle düzenlendiğini ortaya koyar.
Tek Protein, Üç Yüz
Yazarlar, NINJ1’in görünüşte çelişkili davranışlarının onun farklı fiziksel formları benimseme yeteneğiyle açıklanabileceğini savunuyor. Sessiz durumunda NINJ1 çoğunlukla hücrelerin birbirine tutunmasına yardımcı olan dimer çiftleri halinde tek birimler olarak bulunur. MMP-9 gibi kesici bir enzim dış segmentini kopardığında, bu fragman çevre sıvıya salınır ve bağışıklık hücrelerini çeken ve yönlendiren küçük bir sinyal olan kemokin gibi davranır. Güçlü stres sinyalleri altında ise NINJ1 birimleri zar içinde yerleşik büyük oligomerik halkalara yeniden düzenlenir; bunlar zar yamalarını oyarak tam yırtılmaya neden olur. Yapışkan, çözünür haberci ve zar “kesici” olmak üzere bu üç form, tek bir proteine bağlama, hücre hareketi ve hücre yıkımını bağlama yeteneği verir; hangi görevin yerine getirileceği bağlama bağlıdır.
Hücre Patlamasının Sağlık ve Hastalık Üzerindeki Etkileri
NINJ1 hücrelerin nazikçe yok olup olmayacağı ya da patlayarak parçalanıp parçalanmayacağını yönettiği için birçok hastalığın kesişme noktasında yer alır. Şiddetli pankreatit veya gut gibi inflamatuvar durumlarda NINJ1 kaynaklı yırtılma, ölen hücrelerden tehlike sinyalleri salınarak ağrı ve şişliği artırır; hayvan modellerinde NINJ1’in engellenmesi doku hasarını hafifletebilir. Kan damarlarında NINJ1’in çift yönlü bir yaşamı vardır: belirli formları diyabetik damar hasarını kötüleştirirken, çözünür fragmanı arter plaklarında inflamasyonu yatıştırabilir. Enfeksiyonlar sırasında NINJ1 aracılı patlama vücudun mikropları açığa çıkarmasına ve bağışıklık savunmalarını seferber etmesine yardımcı olur; ancak sepsis ve şiddetli viral hastalıklarda aynı süreç aşırı, vücut çapında inflamasyon ve pıhtılaşmayı körükleyebilir. Beyinde ve sinirlerde NINJ1 bazı durumlarda sinir yeniden büyümesini ve damar onarımını destekler, ancak felç veya travma sonrası zararlı inflamasyona da katkıda bulunur.
Kanserde NINJ1 ve Gelecekteki Tedaviler
Kansere gelince, NINJ1 yine iki yüz gösterir. Tümör baskılayıcı p53’ün durumu ve çevre doku sinyallerine bağlı olarak, tümör büyümesini ve yayılmasını destekleyebilir veya inflamatuvar, tedaviye bağlı hücre ölümünü tetiklemeye yardımcı olabilir. Bu karmaşıklık NINJ1’i cazip ama tehlikeli bir ilaç hedefi yapar. Derleme mevcut deneysel stratejileri haritalandırır: NINJ1 düzeylerini düşüren doğal bileşikler ve vitaminler, halka benzeri montajlarını önleyen amino asitler ve küçük moleküller ve yapışkan veya kemotaktik rollerini engelleyen tasarım peptitler veya antikorlar. Yazarlar, gerçekten güvenli terapilerin “form-spesifik” olması gerektiğini; akut doku hasarında gözenek oluşturan halkalara, kronik inflamasyonda çözünür fragmana veya zararlı bağışıklık hücresi hareketiyle ilişkili hastalıklarda yapışkan forma yönelik olması gerektiğini savunuyorlar.
Hücresel Bir Devre Kesiciyi İlaç Hedefine Çevirmek
Genel olarak makale, NINJ1’in hücre ölümü için basit bir açma–kapama düğmesi olmadığını, yapısının görevini belirleyen çok yönlü bir kontrol merkezi olduğunu sonucuna varıyor. Bir hücrenin tutunup tutunmayacağına, yardım sinyali gönderip göndermeyeceğine veya parçalanıp parçalanmayacağına karar vererek NINJ1 sinir onarımı, bağışıklık, damar sağlığı, enfeksiyon sonuçları ve kanser davranışını birbirine bağlıyor. Bu devre kesiciyi terapi için kullanmak, zararlı formu doğru hücrelerde doğru zamanda hedeflerken konak savunması ve doku onarımındaki koruyucu rollerini koruyacak hassas kontrol gerektirecek. Bu hassasiyet sağlanabilirse, NINJ1 bazlı tedaviler geniş bir hastalık yelpazesinde zararlı inflamasyon ve hücre ölümünü dizginlemenin yeni bir yolunu sunabilir.
Atıf: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Anahtar kelimeler: NINJ1, hücre ölümü, inflamasyon, zarf yırtılması, terapötik hedefler