Clear Sky Science · pl
Rola NINJ1 w chorobach
Kiedy komórki wybierają pęknięcie
Nasze komórki otoczone są delikatnymi zewnętrznymi powłokami, które oddzielają wnętrze życia od świata zewnętrznego. Przez dekady naukowcy zakładali, że gdy te powłoki w końcu pękają podczas śmierci komórki, jest to po prostu niefortunne pęknięcie — jak pęknięcie balonu. Ten artykuł przeglądowy pokazuje, że zamiast tego mały białkowy składnik błony o nazwie NINJ1 działa jak wbudowany przełącznik wyburzeniowy. Decydując, kiedy i w jaki sposób komórki rozrywają się, NINJ1 kształtuje zapalenie, naprawę nerwów, wzrost naczyń krwionośnych, kontrolę infekcji, a nawet rozwój nowotworów — co czyni go atrakcyjnym, lecz trudnym celem dla przyszłych leków.
Maleńki strażnik na krawędzi komórki
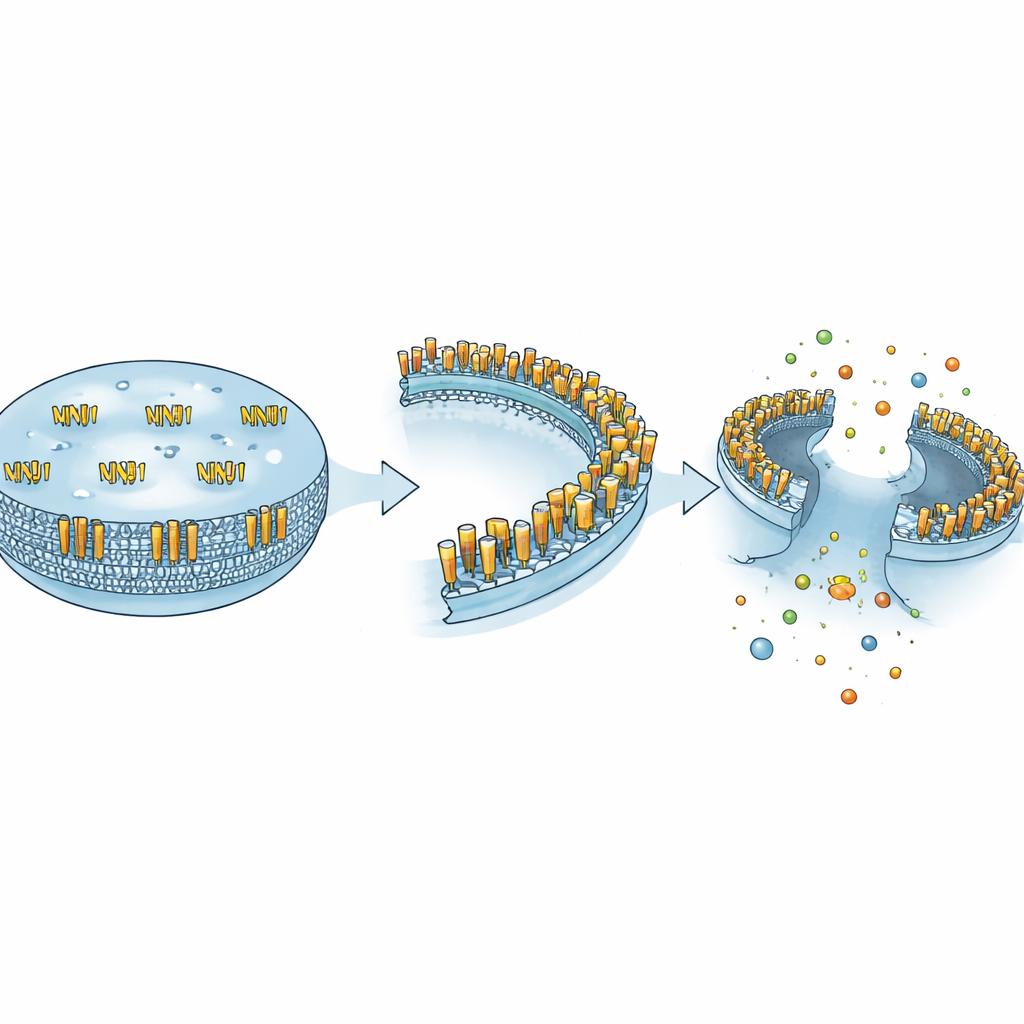
NINJ1 znajduje się w błonie zewnętrznej komórek i został pierwotnie odkryty w uszkodzonych nerwach, gdzie wydawał się pomagać w odrastaniu uszkodzonych włókien. Przez lata traktowano go jako proste „lepne” białko umożliwiające komórkom przyleganie do siebie. Ten pogląd zmienił się w 2021 roku, gdy badacze wykazali, że NINJ1 jest aktywnym wykonawcą końcowego rozdarcia w wielu formach wybuchowej śmierci komórkowej. Zamiast biernej awarii błony, cząsteczki NINJ1 zmieniają kształt, zbierają się w duże pierścieniowe struktury i wycinają fragmenty błony, pozwalając zawartości komórki wylać się do otaczającej tkanki. To obala dawny obraz czysto przypadkowego pęknięcia i ujawnia, że ostatni etap litycznej śmierci komórki jest sam w sobie starannie regulowany.
Jedno białko, trzy oblicza
Autorzy argumentują, że pozornie sprzeczne zachowania NINJ1 można zrozumieć przez jego zdolność do przyjmowania różnych form fizycznych. W stanie spoczynku NINJ1 występuje głównie jako pojedyncze jednostki złączone w dimery, które pomagają komórkom przylegać do siebie. Gdy enzym trawiący, taki jak MMP-9, obcina jego zewnętrzny fragment, ten odczepiony kawałek uwalnia się do płynu otaczającego i zachowuje się jak chemokinina — mały sygnał przyciągający i kierujący komórkami układu odpornościowego. Pod silnymi sygnałami stresowymi jednostki NINJ1 reorganizują się natomiast w duże oligomeryczne pierścienie zakotwiczone w błonie, które wycinają fragmenty błony i powodują pełne rozerwanie. Te trzy formy — adhezyjna, rozpuszczalny posłaniec i „nóż” błonowy — dają jednemu białku zdolność kontrolowania kontaktów komórkowych, ruchu komórek i ich rozbiórki, zależnie od kontekstu.
Jak pękanie komórek kształtuje zdrowie i choroby
Ponieważ NINJ1 decyduje, czy komórki gasną łagodnie, czy wybuchowo pękają, znajduje się na skrzyżowaniu wielu chorób. W stanach zapalnych, takich jak ciężkie zapalenie trzustki czy dna moczanowa, NINJ1-napędzane pęknięcia wzmacniają ból i obrzęk przez uwalnianie sygnałów niebezpieczeństwa z umierających komórek; blokada NINJ1 w modelach zwierzęcych może łagodzić uszkodzenia tkanek. W naczyniach krwionośnych NINJ1 ma dwoistą rolę: pewne formy pogarszają uszkodzenia naczyń w cukrzycy, podczas gdy jego rozpuszczalny fragment może uspokajać zapalenie w blaszkach miażdżycowych. Podczas infekcji pękanie zależne od NINJ1 pomaga organizmowi odsłonić drobnoustroje i zmobilizować obronę immunologiczną, lecz w sepsie i ciężkich chorobach wirusowych ten sam proces może napędzać przytłaczające, ogólnoustrojowe zapalenie i krzepnięcie. W mózgu i nerwach NINJ1 wspiera odrastanie nerwów i naprawę naczyń w niektórych sytuacjach, ale uczestniczy też w szkodliwym zapaleniu po udarze lub urazie.
NINJ1 w raku i przyszłe terapie
W raku NINJ1 znowu pokazuje dwie twarze. W zależności od statusu supresora nowotworowego p53 i sygnałów z otaczającej tkanki, może wspierać wzrost i rozprzestrzenianie się guza albo pomagać w wywoływaniu zapalnej, wywołanej terapią śmierci komórkowej. Ta złożoność czyni NINJ1 kuszącym, lecz ryzykownym celem lekowym. Przegląd przedstawia obecne strategie eksperymentalne: związki naturalne i witaminy obniżające poziom NINJ1, aminokwasy i małe cząsteczki zapobiegające tworzeniu się jego pierścieni, oraz zaprojektowane peptydy czy przeciwciała blokujące jego role adhezyjne lub chemotaktyczne. Autorzy twierdzą, że naprawdę bezpieczne terapie muszą być „specyficzne dla formy” — ukierunkowane na formujące pory pierścienie w ostrych uszkodzeniach tkanek, na rozpuszczalny fragment w przewlekłym zapaleniu lub na formę adhezyjną w chorobach napędzanych szkodliwym ruchem komórek odpornościowych.
Przekształcanie komórkowego przełącznika awaryjnego w cel lekarski
Podsumowując, artykuł dochodzi do wniosku, że NINJ1 nie jest prostym przełącznikiem włącz/wyłącz śmierci komórki, lecz wszechstronnym centrum sterowania, którego struktura determinuje zadanie. Decydując, czy komórka trzyma się, wysyła sygnały pomocy, czy rozpada się na kawałki, NINJ1 łączy naprawę nerwów, odporność, zdrowie naczyń krwionośnych, przebieg infekcji i zachowanie nowotworów. Wykorzystanie tego przełącznika awaryjnego w terapii będzie wymagało precyzyjnej kontroli — uderzenia w szkodliwą formę we właściwych komórkach we właściwym czasie, przy jednoczesnym zachowaniu jego ochronnych ról w obronie gospodarza i naprawie tkanek. Jeśli taka precyzja będzie możliwa, terapie oparte na NINJ1 mogą zaoferować nowy sposób ujarzmienia szkodliwych zapaleń i śmierci komórek w szerokim spektrum chorób.
Cytowanie: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Słowa kluczowe: NINJ1, śmierć komórkowa, zapalenie, pęknięcie błony, cele terapeutyczne