Clear Sky Science · fr
Le rôle de NINJ1 dans les maladies
Quand les cellules choisissent d’éclater
Nos cellules sont enveloppées d’une fine peau externe qui sépare la vie intérieure du monde extérieur. Pendant des décennies, les scientifiques ont supposé que lorsque ces membranes se déchirent enfin lors de la mort cellulaire, c’était un incident fortuit — comme un ballon qui éclate. Cet article de synthèse montre qu’au contraire, une petite protéine membranaire nommée NINJ1 fonctionne comme un commutateur interne de démolition. En décidant quand et comment les cellules se rompent, NINJ1 contribue à façonner l’inflammation, la réparation nerveuse, la croissance des vaisseaux sanguins, le contrôle des infections et même le cancer — ce qui en fait une cible attrayante mais délicate pour de futurs traitements.
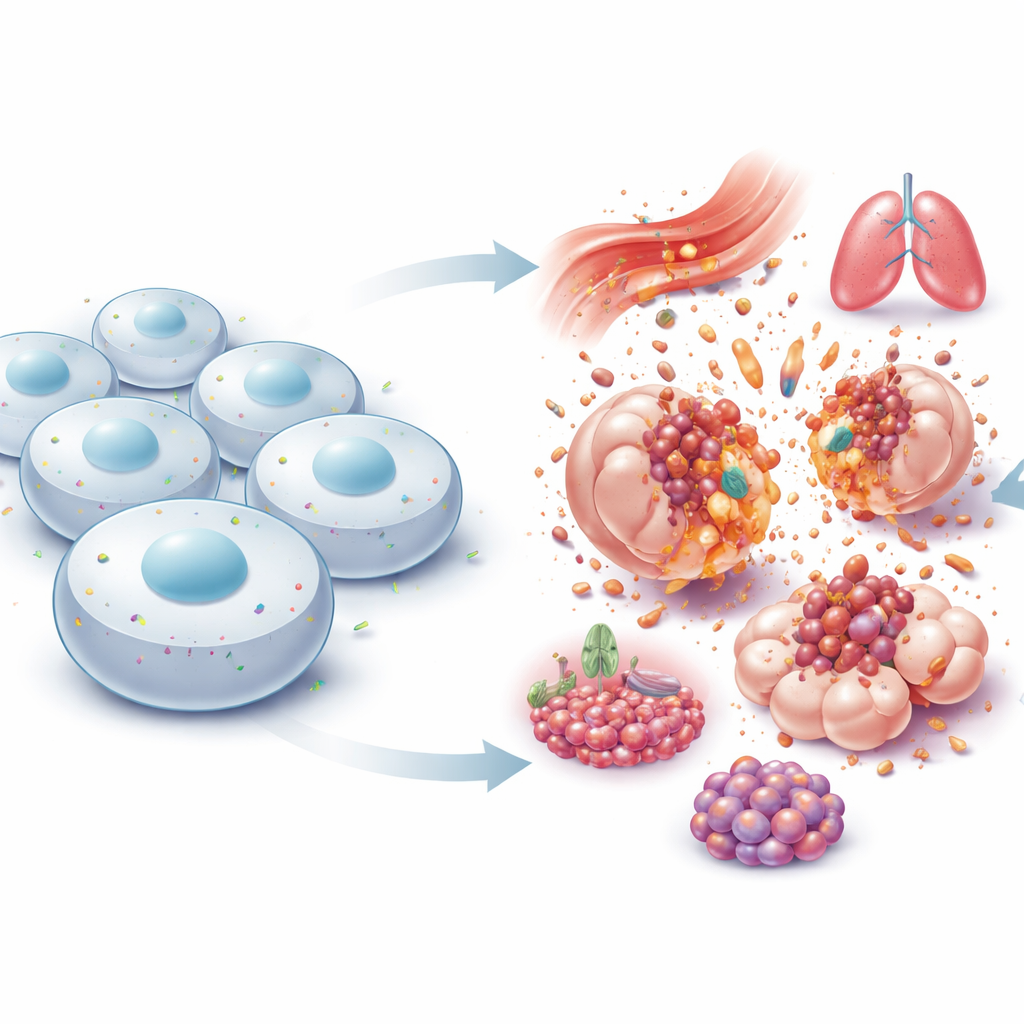
Un minuscule gardien au bord de la cellule
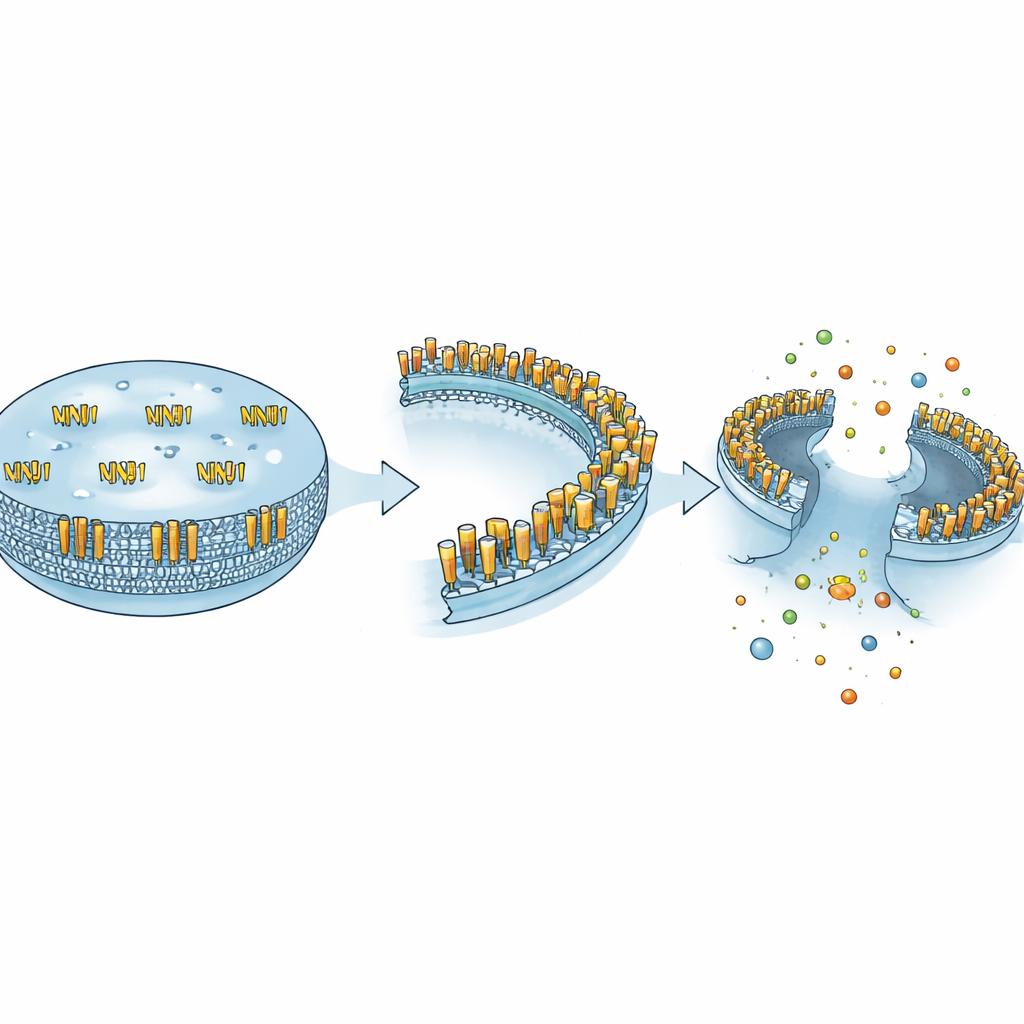
NINJ1 se situe dans la membrane externe des cellules et a été découverte à l’origine dans des nerfs lésés, où elle semblait favoriser la repousse des fibres endommagées. Pendant des années, on l’a considérée comme une simple protéine « adhésive » permettant aux cellules de rester attachées les unes aux autres. Cette vision a changé en 2021, lorsque des chercheurs ont montré que NINJ1 est l’exécutrice active de la déchirure finale dans de nombreuses formes de mort cellulaire explosive. Plutôt que de céder passivement, les molécules de NINJ1 changent de conformation, s’assemblent en grandes structures annulaires et extraient des portions de membrane, permettant au contenu cellulaire de se répandre dans les tissus environnants. Cela renverse l’ancienne idée d’une rupture purement accidentelle et révèle que la dernière étape de la mort cellulaire lytique est elle-même finement régulée.
Une protéine, trois visages
Les auteurs soutiennent que les comportements apparemment contradictoires de NINJ1 s’expliquent par sa capacité à adopter différentes formes physiques. À l’état calme, NINJ1 existe principalement comme des unités simples appariées en dimères qui aident les cellules à adhérer entre elles. Lorsqu’une enzyme clivante telle que la MMP‑9 coupe son segment extracellulaire, ce fragment est libéré dans le fluide environnant et se comporte comme une chimiokine — un petit signal qui attire et guide les cellules immunitaires. Sous de forts signaux de stress, les unités de NINJ1 se réorganisent en grands anneaux oligomériques ancrés dans la membrane, qui découpent des plaques membranaires et provoquent une rupture complète. Ces trois formes — adhésive, messagère soluble et « coupeuse » membranaire — confèrent à une même protéine la capacité de contrôler le contact cellulaire, le mouvement cellulaire et la démolition cellulaire, selon le contexte.
Comment l’éclatement des cellules façonne la santé et la maladie
Parce que NINJ1 régule si les cellules s’éteignent en douceur ou éclatent de façon explosive, elle se trouve au carrefour de nombreuses pathologies. Dans des affections inflammatoires comme une pancréatite sévère ou la goutte, la rupture induite par NINJ1 amplifie la douleur et l’oedème en libérant des signaux de danger depuis les cellules mourantes ; bloquer NINJ1 chez l’animal peut atténuer les lésions tissulaires. Dans les vaisseaux sanguins, NINJ1 a une double vie : certaines formes aggravent les lésions vasculaires liées au diabète, tandis que son fragment soluble peut calmer l’inflammation dans les plaques artérielles. Lors des infections, l’éclatement médié par NINJ1 aide l’organisme à exposer les microbes et à mobiliser les défenses immunitaires, mais dans le sepsis et les maladies virales sévères, ce même processus peut alimenter une inflammation généralisée et une coagulation excessives. Dans le cerveau et les nerfs, NINJ1 favorise la repousse nerveuse et la réparation vasculaire dans certains contextes, tout en participant à l’inflammation délétère après un AVC ou un traumatisme.
NINJ1 dans le cancer et perspectives thérapeutiques
Dans le cancer, NINJ1 montre à nouveau deux visages. Selon le statut du suppresseur de tumeur p53 et les signaux du microenvironnement, elle peut soit favoriser la croissance et la dissémination tumorales, soit aider à déclencher une mort cellulaire inflammatoire induite par les traitements. Cette complexité rend NINJ1 une cible médicamenteuse tentante mais risquée. La revue cartographie les stratégies expérimentales actuelles : composés naturels et vitamines qui abaissent les niveaux de NINJ1, acides aminés et petites molécules qui empêchent la formation de ses assemblages annulaires, et peptides conçus ou anticorps qui bloquent ses rôles adhésifs ou chimiotactiques. Les auteurs soutiennent que des thérapies vraiment sûres doivent être « spécifiques à la forme » — visant les anneaux formant des pores dans les lésions tissulaires aiguës, le fragment soluble dans l’inflammation chronique, ou la forme adhésive dans les maladies liées au trafic nuisible des cellules immunitaires.
Transformer un interrupteur de rupture cellulaire en cible médicamenteuse
Globalement, l’article conclut que NINJ1 n’est pas un simple interrupteur marche‑arrêt de la mort cellulaire, mais un centre de contrôle polyvalent dont la structure détermine la fonction. En décidant si une cellule reste attachée, envoie des signaux d’aide ou se disloque, NINJ1 relie la réparation nerveuse, l’immunité, la santé vasculaire, le devenir des infections et le comportement des tumeurs. Exploiter cet interrupteur pour la thérapie exigera un contrôle extrêmement précis — cibler la forme nuisible dans les bonnes cellules au bon moment tout en préservant ses rôles protecteurs dans la défense de l’hôte et la réparation tissulaire. Si cette précision peut être atteinte, des traitements basés sur NINJ1 pourraient offrir une nouvelle façon de maîtriser l’inflammation et la mort cellulaire délétères dans un large spectre de maladies.
Citation: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Mots-clés: NINJ1, mort cellulaire, inflammation, rupture de membrane, cibles thérapeutiques