Clear Sky Science · he
תפקיד NINJ1 במצבים פתולוגיים
כאשר תאים בוחרים להתפוצץ
התאים שלנו עטופים ב"עורות" חיצוניים עדינים ששומרים על ההבדל בין הפנימי של החיים לבין העולם החיצון. במשך עשורים, מדענים הניחו שכאשר ה"עורות" הללו נקרעים בסופו של דבר במהלך מוות תאי, זהו אירוע מקרי—כמו בלון שמתפוצץ. מאמר סקירה זה מראה שבעצם חלבון ממברנלי קטן בשם NINJ1 מתפקד כמפסק הריסה מובנה. על ידי קביעת המועד והאופן שבו התאים נקרעים, NINJ1 מעצב דלקת, תיקון עצבי, גדילת כלי דם, שליטה בזיהומים ואף סרטן—ומכאן שהוא יעד תרפואטי אטרקטיבי אך מורכב לעבודה.
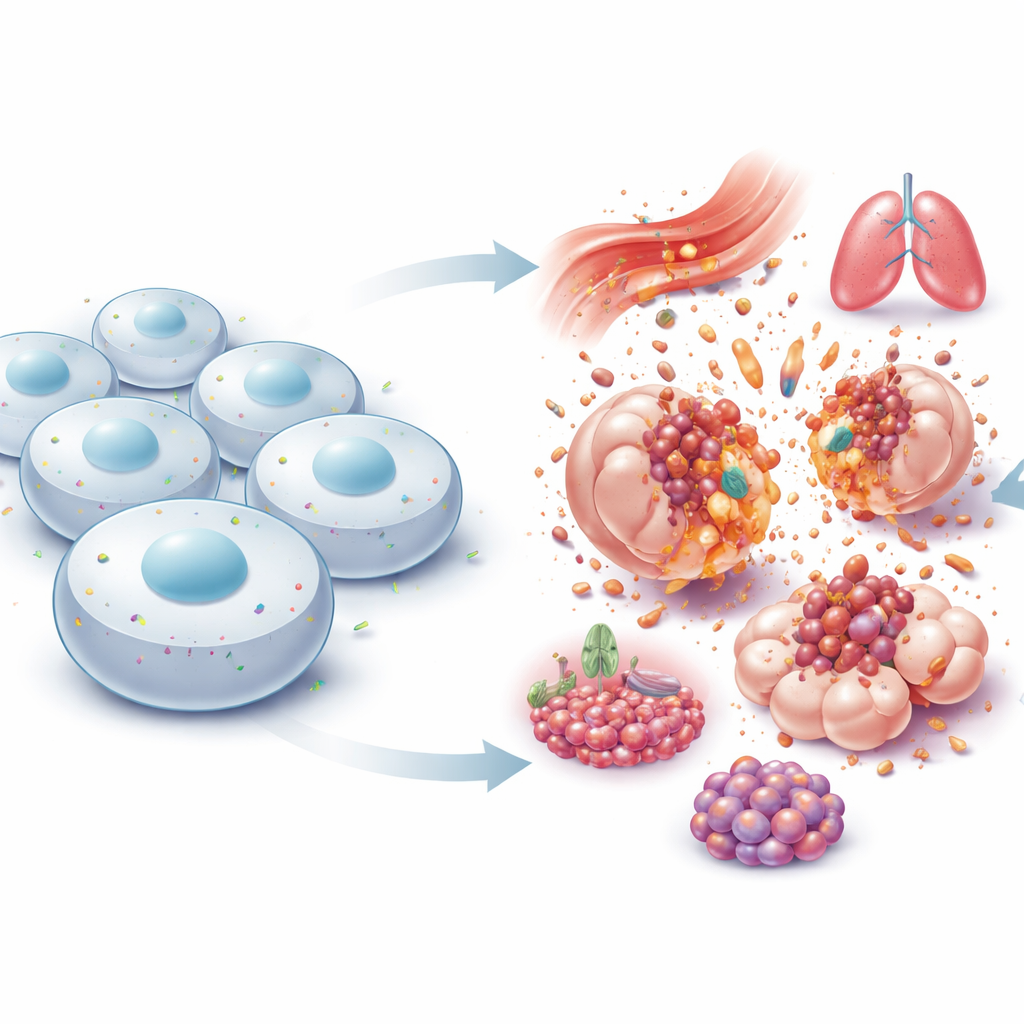
שומר שער זעיר בקצה התא
NINJ1 יושב בממברנה החיצונית של התאים ולכאורה התגלה לראשונה בעצבים שנפגעו, שם נראה כמעודד גדילה מחודשת של סיבים פגועים. שנים רבות התייחסו אליו כחלבון "דביק" פשוט שמאפשר לתאים להיצמד זה לזה. התפיסה הזאת השתנתה ב-2021, כאשר חוקרים הראו ש-NINJ1 הוא המבצע הפעיל של הקריעה הסופית בצורות רבות של מוות תאי ליטי מתפרץ. במקום שהממברנה תיכשל באופן פסיבי, מולקולות NINJ1 משנות צורה, מצטברות למבנים גדולים בצורת טבעת וחורצות חלקים מהממברנה, מה שמאפשר לתכולת התא להישפך לרקמה שמסביב. זה מערער על הרעיון הישן של קריעה אקראית לחלוטין ומגלה שהצעד האחרון במוות תאי ליטי מפוקח בקפידה.
חלבון אחד, שלושה פנים
המחברים טוענים שההתנהגויות שנראות סותרות של NINJ1 ניתנות להבנה דרך יכולתו לאמץ צורות פיזיקליות שונות. במצב השקט שלו, NINJ1 קיים בעיקר כאחדות בודדות הזוגיות בדימרים שעוזרות לתאים להיצמד זה לזה. כאשר אנזים חותך כגון MMP-9 קוצץ את מקטעו החיצוני, אותו מקטע משתחרר לנוזל הסביבתי ומתנהג ככימוקין—אות קטנה שמושכת ומנחה תאי חיסון. תחת אותות מתח חזקים, יחידות NINJ1 מאורגנות מחדש לטבעות אוליגומריות גדולות המשוקעות בממברנה, החורצות מקטעי ממברנה וגורמות לקריעה מלאה. שלוש הצורות הללו—דבקות, שליח מסיס ומ"חורר" ממברנה—נותנות לחלבון יחיד את היכולת לשלוט על תא-מגע, תנועת תאים והריסת תאים בהתאם להקשר.
כיצד קריעת תאים מעצבת בריאות ומחלה
מכיוון ש-NINJ1 קובע האם תאים דוהים בעדינות או מתפוצצים באלימות, הוא יושב בצומת של מחלות רבות. במצבים דלקתיים כמו דלקת לבלב קשה או גאוט, קריעת ממברנה מונעת על ידי NINJ1 מגדילה כאב ונפיחות על ידי שחרור אותות סכנה מתאים מתים; חסימת NINJ1 במודלים של בעלי חיים יכולה להקל על נזק לרקמות. בכלי דם, ל-NINJ1 יש חיים כפולים: צורות מסוימות מחמירות פגיעה בכלי דם בסוכרת, בעוד המקטע המסיס שלו יכול להרגיע דלקת בפלאקים עורקיים. בזיהומים, הקריעה המתווכת על ידי NINJ1 מסייעת לחשוף מיקרובים ולגייס תגובות חיסוניות, אך בספסיס ומחלות ויראליות קשות אותו תהליך יכול להאכיל דלקת מערכתית מציפה וקרישת דם. במוח ובעצבים, NINJ1 תומך בגדילה מחודשת של עצבים ותיקון כלי דם במצבים מסוימים, אך גם משתתף בדלקת מזיקה לאחר שבץ או טראומה.
NINJ1 בסרטן וטיפולים עתידיים
בסרטן, NINJ1 שוב מציג שתי פנים. בהתאם למצב המדכא גידול p53 ולאותות הרקמה שמסביב, הוא יכול לעזור לצמיחה והפצת הגידול או לסייע בהפעלת מוות תאי מגרה דלקת הנגרם על ידי טיפולים. המורכבות הזאת הופכת את NINJ1 ליעד תרפואטי פיתוי אך מסוכן. הסקירה ממפה אסטרטגיות ניסיוניות נוכחיות: תרכובות טבעיות ווויטמינים שמורידות רמות NINJ1, חומצות אמינו ומולקולות קטנות שמונעות את הרכבת הטבעות שלו, ופפטידים או נוגדנים מעוצבים שחוסמים את תפקידיו הדביקים או הכימוטקטיים. המחברים טוענים שטיפולים בטוחים באמת חייבים להיות "צורתיים"—מכוונים לטבעות שפורמות נקבים בפגיעה חריפה ברקמות, למקטע המסיס בדלקת כרונית, או לצורת ההיצמדות במחלות המונעות על ידי תנועה מזיקה של תאי חיסון.
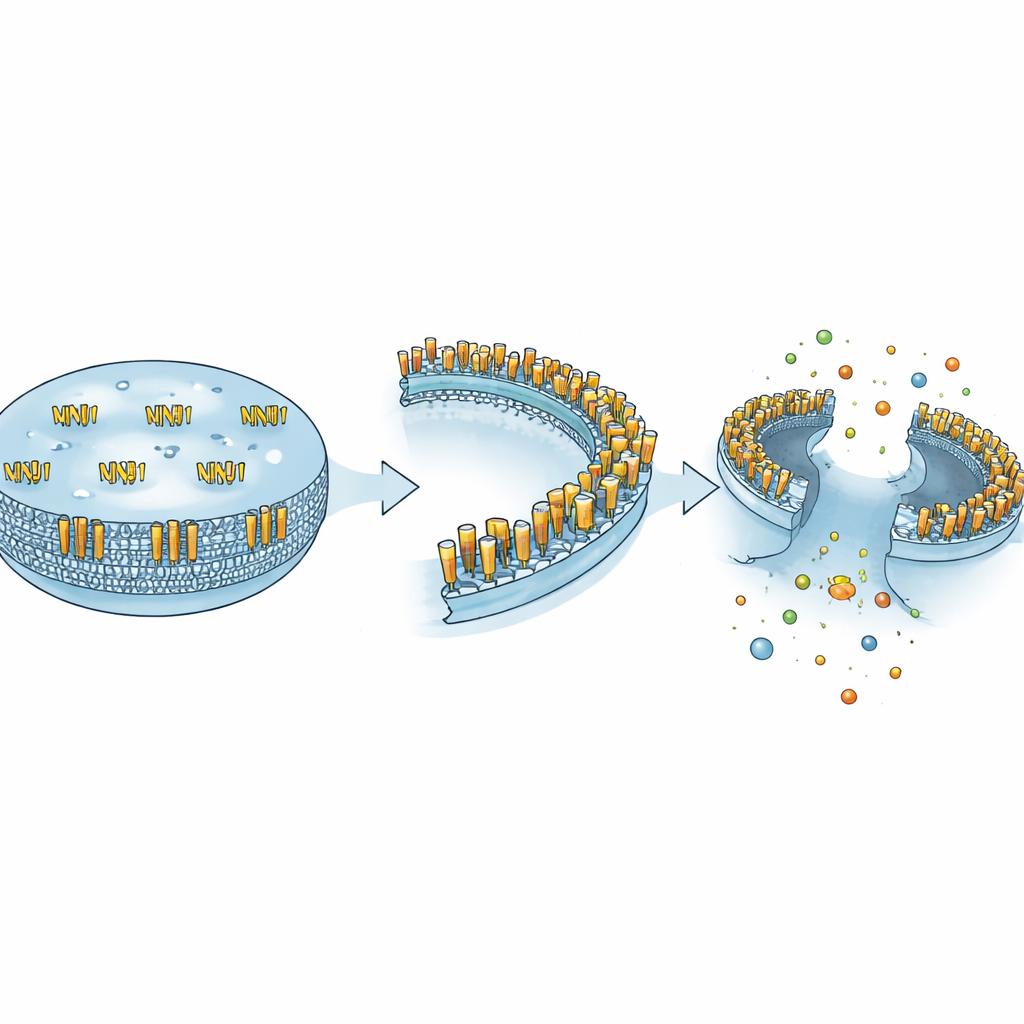
להפוך מפסק הרס תאי ליעד תרופתי
בסיכום, המאמר מסיק ש-NINJ1 אינו מפסק פשוט של כיבוי והדלקה למוות תאי, אלא מרכז בקרת רב-תכליתי שמבנהו קובע את תפקידו. על ידי קביעה אם תא נאחז, שולח אותות לעזרה או מתפורר, NINJ1 מקשר בין תיקון עצבי, חיסון, בריאות כלי דם, תוצאות זיהומיות והתנהגות סרטן. כיבוש מפסק ההריסה הזה לטובת טיפול ידרוש שליטה מדויקת—להכות בצורת המזיקה בתאים המתאימים בזמן המתאים תוך שמירה על תפקידיו המגוננים בהגנה על המאחסן ותיקון רקמות. אם ניתן להשיג דיוק כזה, טיפולים מבוססי NINJ1 יכולים להציע דרך חדשה לרסן דלקת ומוות תאי מזיקים בטווח רחב של מחלות.
ציטוט: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
מילות מפתח: NINJ1, מוות תאי, דלקת, קריעת ממברנה, מטרות תרפויטיות