Clear Sky Science · it
Il ruolo di NINJ1 nelle malattie
Quando le cellule scelgono di esplodere
Le nostre cellule sono avvolte da sottili membrane esterne che tengono l’interno della vita separato dal mondo esterno. Per decenni gli scienziati hanno supposto che quando quelle membrane si lacerano durante la morte cellulare, sia solo un impatto casuale—come lo scoppio di un palloncino. Questa review mostra invece che una piccola proteina di membrana chiamata NINJ1 funziona come un interruttore di demolizione incorporato. Decidendo quando e come le cellule si aprono, NINJ1 contribuisce a modellare l’infiammazione, la riparazione nervosa, la crescita dei vasi sanguigni, il controllo delle infezioni e persino il cancro—rendendola un bersaglio attraente ma complesso per future terapie.
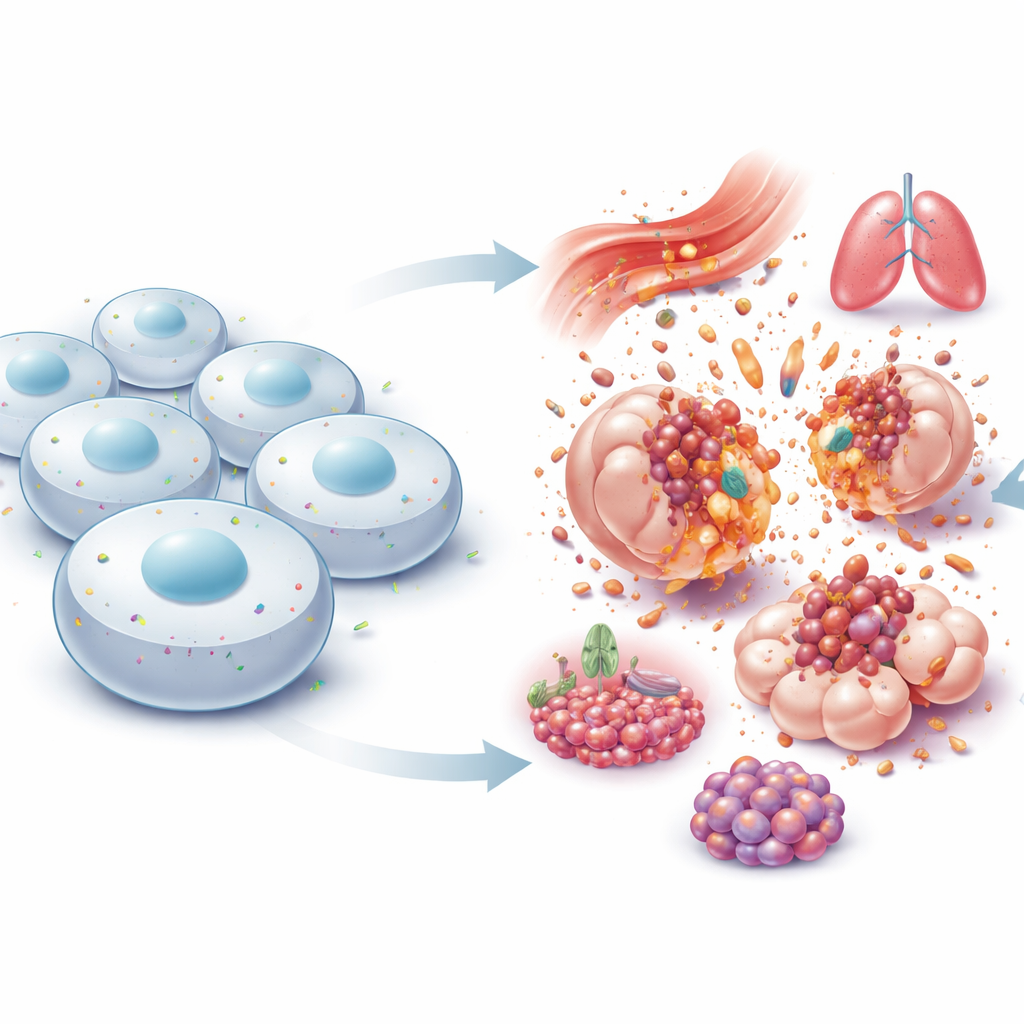
Un piccolo guardiano al confine della cellula
NINJ1 si trova nella membrana esterna delle cellule ed è stata scoperta originariamente nei nervi danneggiati, dove sembrava favorire la ricrescita delle fibre lesionate. Per anni è stata considerata una proteina semplicemente “adesiva” che permette alle cellule di restare attaccate l’una all’altra. Questa visione è cambiata nel 2021, quando i ricercatori hanno dimostrato che NINJ1 è l’esecutore attivo della lacerazione finale in molte forme di morte cellulare esplosiva. Invece che la membrana fallisca passivamente, le molecole di NINJ1 cambiano forma, si assemblano in grandi strutture ad anello e ritagliano porzioni di membrana, permettendo al contenuto cellulare di riversarsi nei tessuti circostanti. Questo ribalta l’idea di una rottura puramente accidentale e rivela che l’ultimo passo della morte cellulare litica è esso stesso finemente regolato.
Una proteina, tre volti
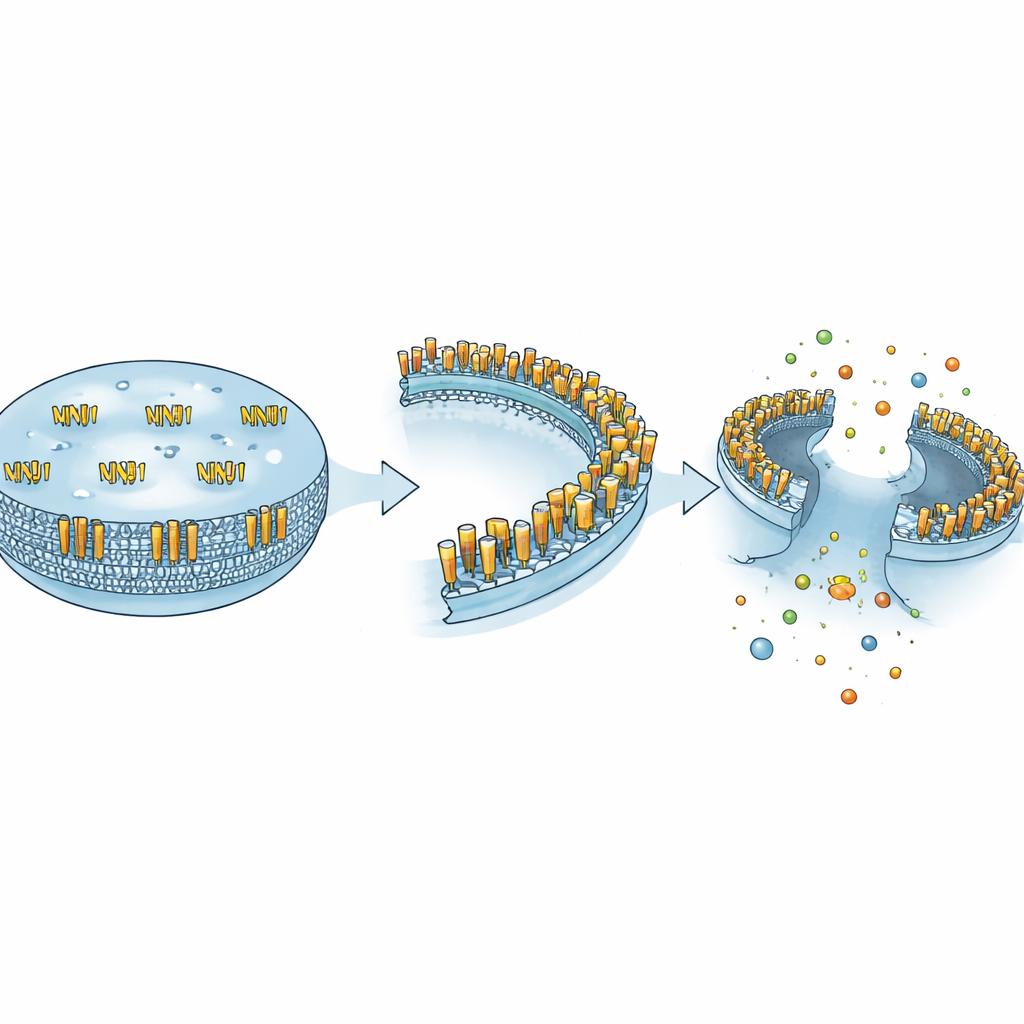
Gli autori sostengono che i comportamenti apparentemente contraddittori di NINJ1 possono essere compresi dalla sua capacità di assumere diverse forme fisiche. Nello stato quieto, NINJ1 esiste principalmente come unità singole appaiate in dimeri che aiutano le cellule ad aderire tra loro. Quando un enzima proteolitico come MMP-9 recide il suo segmento esterno, quel frammento viene rilasciato nel fluido circostante e si comporta come una chemochina—un piccolo segnale che attira e guida le cellule immunitarie. In presenza di segnali di stress intensi, le unità di NINJ1 si riorganizzano invece in grandi anelli oligomerici ancorati nella membrana, che asportano porzioni di membrana e causano la rottura completa. Queste tre forme—adesiva, messaggero solubile e “tagliatrice” di membrana—danno a una sola proteina la capacità di controllare il contatto cellulare, il movimento cellulare e la demolizione cellulare, a seconda del contesto.
Come l’esplosione cellulare modella salute e malattia
Poiché NINJ1 governa se le cellule svaniscono delicatamente o esplodono in modo esplosivo, si trova all’incrocio di molte malattie. In condizioni infiammatorie come la pancreatite grave o la gotta, la rottura guidata da NINJ1 amplifica dolore e gonfiore rilasciando segnali di pericolo dalle cellule morenti; il blocco di NINJ1 in modelli animali può attenuare il danno tissutale. Nei vasi sanguigni, NINJ1 ha una doppia vita: certe forme peggiorano il danno vascolare diabetico, mentre il suo frammento solubile può placare l’infiammazione nelle placche arteriose. Durante le infezioni, l’esplosione mediata da NINJ1 aiuta l’organismo a esporre i microrganismi e a mobilitare le difese immunitarie, tuttavia nella sepsi e nelle malattie virali gravi lo stesso processo può alimentare un’infiammazione sistemica travolgente e la coagulazione. Nel cervello e nei nervi, NINJ1 supporta la ricrescita nervosa e la riparazione vascolare in alcuni contesti, ma partecipa anche all’infiammazione dannosa dopo ictus o trauma.
NINJ1 nel cancro e trattamenti futuri
Nel cancro, NINJ1 mostra di nuovo due facce. A seconda dello stato del soppressore tumorale p53 e dei segnali del tessuto circostante, può favorire la crescita e la diffusione tumorale oppure contribuire a innescare la morte cellulare infiammatoria indotta dalla terapia. Questa complessità rende NINJ1 un bersaglio farmacologico allettante ma rischioso. La review descrive le strategie sperimentali attuali: composti naturali e vitamine che riducono i livelli di NINJ1, amminoacidi e piccole molecole che impediscono l’assemblaggio ad anello, e peptidi progettati o anticorpi che bloccano i ruoli adesivi o chemiotattici. Gli autori sostengono che terapie veramente sicure devono essere “specifiche per la forma”—mirate agli anelli che formano pori nel danno tissutale acuto, al frammento solubile nell’infiammazione cronica, o alla forma adesiva nelle malattie guidate dal traffico dannoso delle cellule immunitarie.
Trasformare un interruttore di rottura cellulare in un bersaglio farmacologico
Complessivamente, l’articolo conclude che NINJ1 non è un semplice interruttore on–off per la morte cellulare, ma un hub di controllo versatile la cui struttura determina il ruolo svolto. Decidendo se una cellula rimane attaccata, invia segnali di aiuto o si disintegra, NINJ1 collega insieme la riparazione nervosa, l’immunità, la salute dei vasi sanguigni, l’esito delle infezioni e il comportamento del cancro. Sfruttare questo interruttore per la terapia richiederà un controllo di precisione—colpire la forma dannosa nelle cellule giuste al momento giusto preservando i suoi ruoli protettivi nella difesa dell’ospite e nella riparazione dei tessuti. Se si potrà raggiungere tale precisione, i trattamenti basati su NINJ1 potrebbero offrire un nuovo modo per domare l’infiammazione e la morte cellulare dannose in un’ampia gamma di malattie.
Citazione: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Parole chiave: NINJ1, morte cellulare, infiammazione, rottura della membrana, bersagli terapeutici