Clear Sky Science · sv
NINJ1:s roll i sjukdomar
När celler väljer att sprängas
Våra celler är omslutna av känsliga yttre hinnor som håller det inre livet separerat från omvärlden. I årtionden antog forskare att när dessa hinnor slutligen brister under celldöd var det bara ett olyckligt pop—som en ballong som spricker. Denna översiktsartikel visar att i stället fungerar ett litet membranprotein kallat NINJ1 som en inbyggd rivningsbrytare. Genom att avgöra när och hur celler öppnar sig hjälper NINJ1 till att forma inflammation, nervreparation, tillväxt av blodkärl, infektionkontroll och till och med cancer—vilket gör det till ett attraktivt men komplicerat mål för framtida läkemedel.
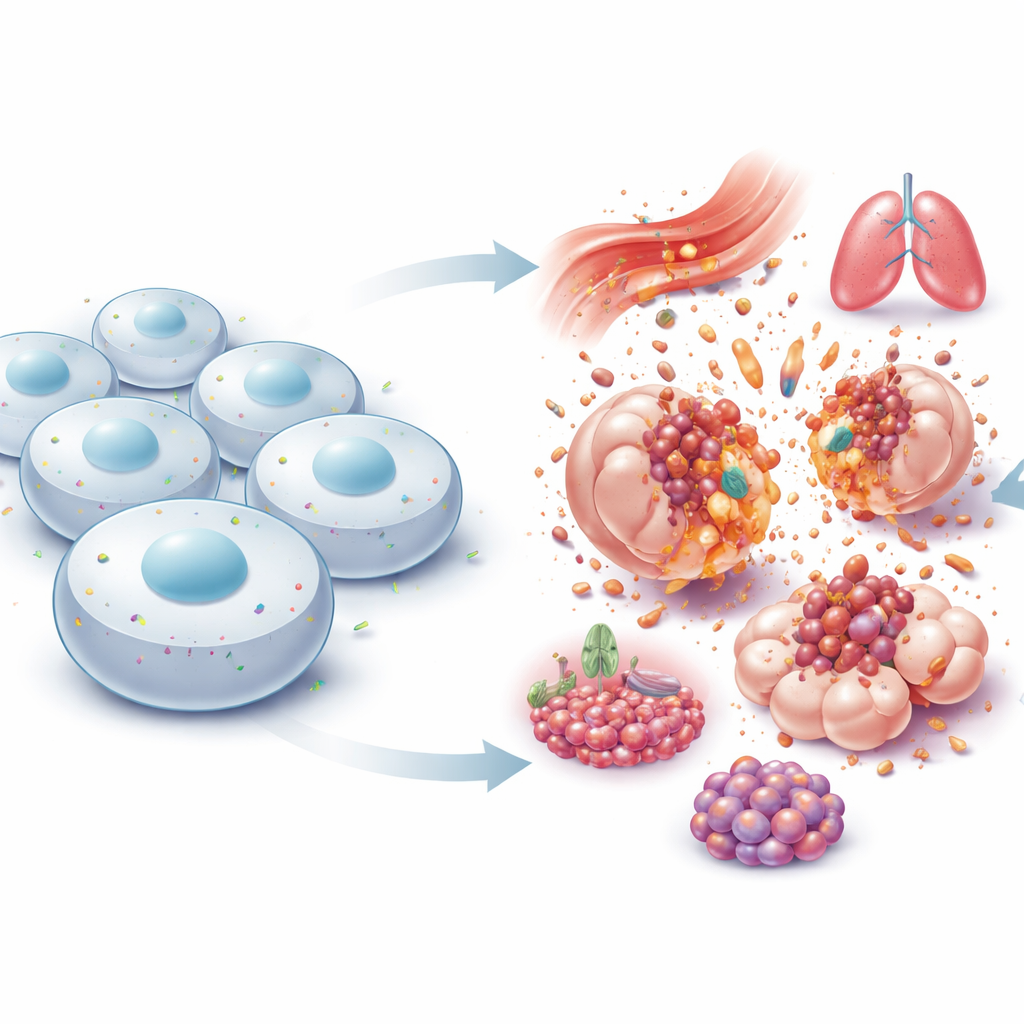
En liten grindvakt vid cellens kant
NINJ1 sitter i cellernas yttre membran och upptäcktes ursprungligen i skadade nerver, där det verkade hjälpa skadade fibrer att växa tillbaka. I åratal behandlades det som ett enkelt ”klibbigt” protein som låter celler hålla ihop. Den bilden förändrades 2021 när forskare visade att NINJ1 är den aktiva utlösaren av den sista revorna i många former av explosiv celldöd. I stället för att membranet havererar passivt ändrar NINJ1-molekyler form, samlas till stora ringliknande strukturer och skär ut bitar av membranet, vilket tillåter cellens innehåll att spillas ut i omgivande vävnad. Detta kullkastar den gamla idén om en rent slumpmässig ruptur och visar att det sista steget i lytisk celldöd i sig är noggrant reglerat.
Ett protein, tre skepnader
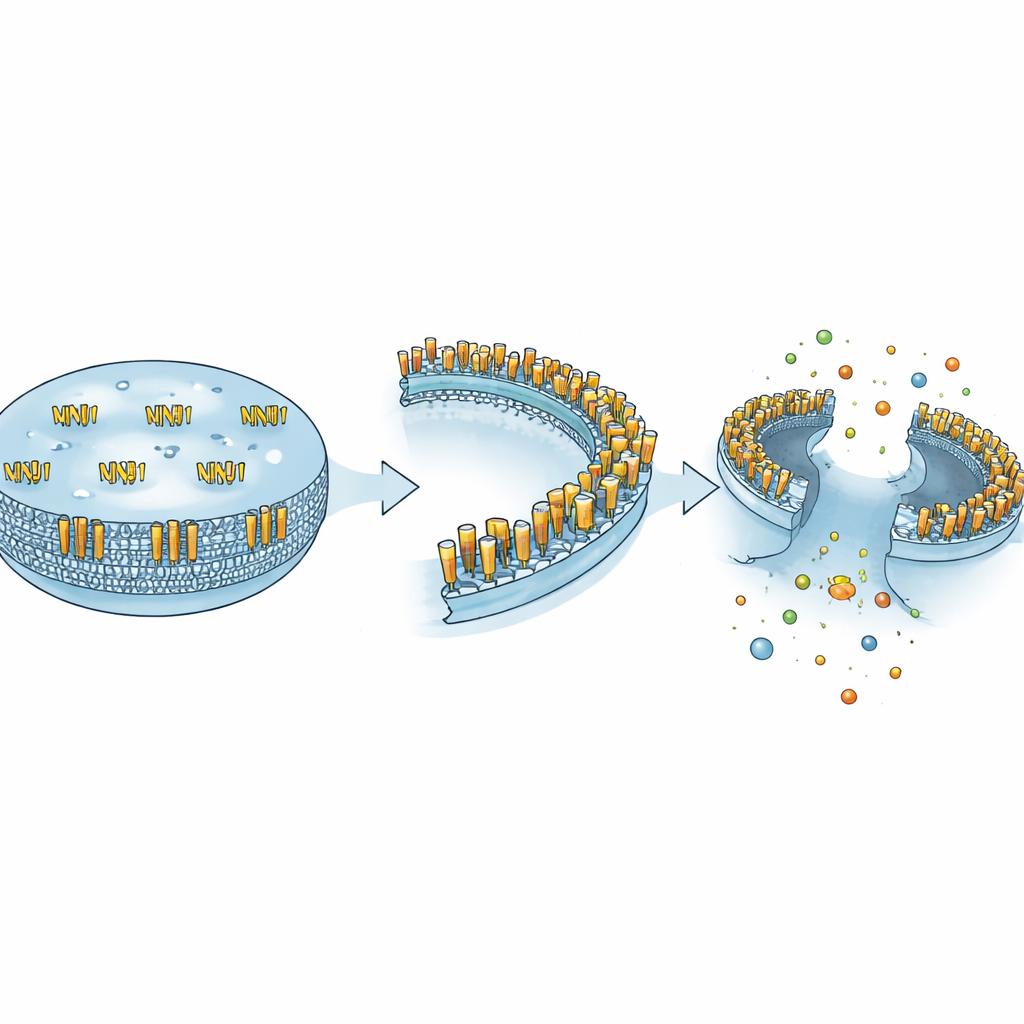
Författarna hävdar att NINJ1:s till synes motsägelsefulla beteenden kan förstås genom dess förmåga att anta olika fysiska former. I sitt lugna tillstånd finns NINJ1 huvudsakligen som enheter parade i dimerer som hjälper celler att fästa vid varandra. När ett klippande enzym som MMP-9 avlägsnar dess yttre segment frisätts den fragmentet till omgivande vätska och beter sig som en kemokin—en liten signal som lockar och vägleder immunceller. Vid starka stressignaler omorganiserar sig NINJ1-enheterna i stället till stora oligomeriska ringar förankrade i membranet, vilka skär ut membranlappar och orsakar fullständig ruptur. Dessa tre former—adhesiv, löslig budbärare och membran-”skärare”—ger ett och samma protein förmågan att kontrollera cellkontakt, cellrörelse och cellexplosion beroende på kontext.
Hur cellsprängning formar hälsa och sjukdom
Eftersom NINJ1 styr om celler tynar bort försiktigt eller exploderar, står det vid korsningen för många sjukdomar. Vid inflammatoriska tillstånd som svår pankreatit eller gikt förstärker NINJ1-drivna rupturer smärta och svullnad genom att släppa ut faresignaler från döende celler; att blockera NINJ1 i djurmodeller kan dämpa vävnadsskada. I blodkärl har NINJ1 ett dubbelt liv: vissa former förvärrar diabetesrelaterade kärlskador, medan dess lösliga fragment kan lugna inflammation i artärplack. Under infektioner hjälper NINJ1-medierad sprängning kroppen att blotta mikrober och samla immunförsvaret, men vid sepsis och svåra virusinfektioner kan samma process elda på överväldigande, kroppsomfattande inflammation och koagulation. I hjärnan och nerverna understöder NINJ1 nervåterväxt och kärlreparation i vissa situationer, men deltar också i skadlig inflammation efter stroke eller trauma.
NINJ1 i cancer och framtida behandlingar
I cancer visar NINJ1 återigen två ansikten. Beroende på tumörsuppressorn p53:s status och signalerna i den omgivande vävnaden kan det antingen underlätta tumörtillväxt och spridning eller hjälpa till att utlösa inflammatorisk, terapiinducerad celldöd. Denna komplexitet gör NINJ1 till ett frestande men riskfyllt läkemedelsmål. Översikten kartlägger nuvarande experimentella strategier: naturliga föreningar och vitaminer som sänker NINJ1-nivåer, aminosyror och små molekyler som förhindrar dess ringliknande sammankomster, samt designade peptider eller antikroppar som blockerar dess adhesiva eller kemotaktiska roller. Författarna menar att verkligt säkra terapier måste vara ”formspecifika”—inriktade på porebildande ringar vid akut vävnadsskada, på det lösliga fragmentet vid kronisk inflammation eller på den adhesiva formen i sjukdomar som drivs av skadlig immuncellsrörelse.
Att förvandla en cellulär strömbrytare till en läkemedelsmåltavla
Sammanfattningsvis konkluderar artikeln att NINJ1 inte är en enkel på/av-brytare för celldöd, utan en mångsidig kontrollknutpunkt vars struktur avgör dess uppgift. Genom att bestämma om en cell håller fast, sänder ut hjälpsignaler eller spricker sönder länkar NINJ1 samman nervreparation, immunitet, kärlhälsa, infektionsutfall och cancerbeteende. Att utnyttja denna brytare för terapi kräver noggrann precision—att träffa den skadliga formen i rätt celler vid rätt tidpunkt samtidigt som dess skyddande roller i värdförsvar och vävnadsreparation bevaras. Om den precisionen kan uppnås kan NINJ1-baserade behandlingar erbjuda ett nytt sätt att tygla skadlig inflammation och celldöd över ett brett spektrum av sjukdomar.
Citering: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Nyckelord: NINJ1, celldöd, inflammation, membranruptur, terapeutiska måltavlor