Clear Sky Science · de
Die Rolle von NINJ1 bei Krankheiten
Wenn Zellen sich zum Zerplatzen entscheiden
Unsere Zellen sind von empfindlichen Außenhäuten umgeben, die das Innere des Lebens von der Außenwelt trennen. Jahrzehntelang gingen Wissenschaftler davon aus, dass das Einreißen dieser Häute beim Zelltod ein bloßer Zufall sei – ähnlich dem Platzen eines Ballons. Dieser Übersichtsartikel zeigt jedoch, dass ein kleines Membranprotein namens NINJ1 wie ein eingebauter Abrissschalter wirkt. Indem es entscheidet, wann und wie Zellen aufplatzen, beeinflusst NINJ1 Entzündungen, Nervenreparatur, Blutgefäßbildung, Infektionskontrolle und sogar Krebs – und macht es zu einem attraktiven, aber schwierigen Ziel für zukünftige Medikamente.
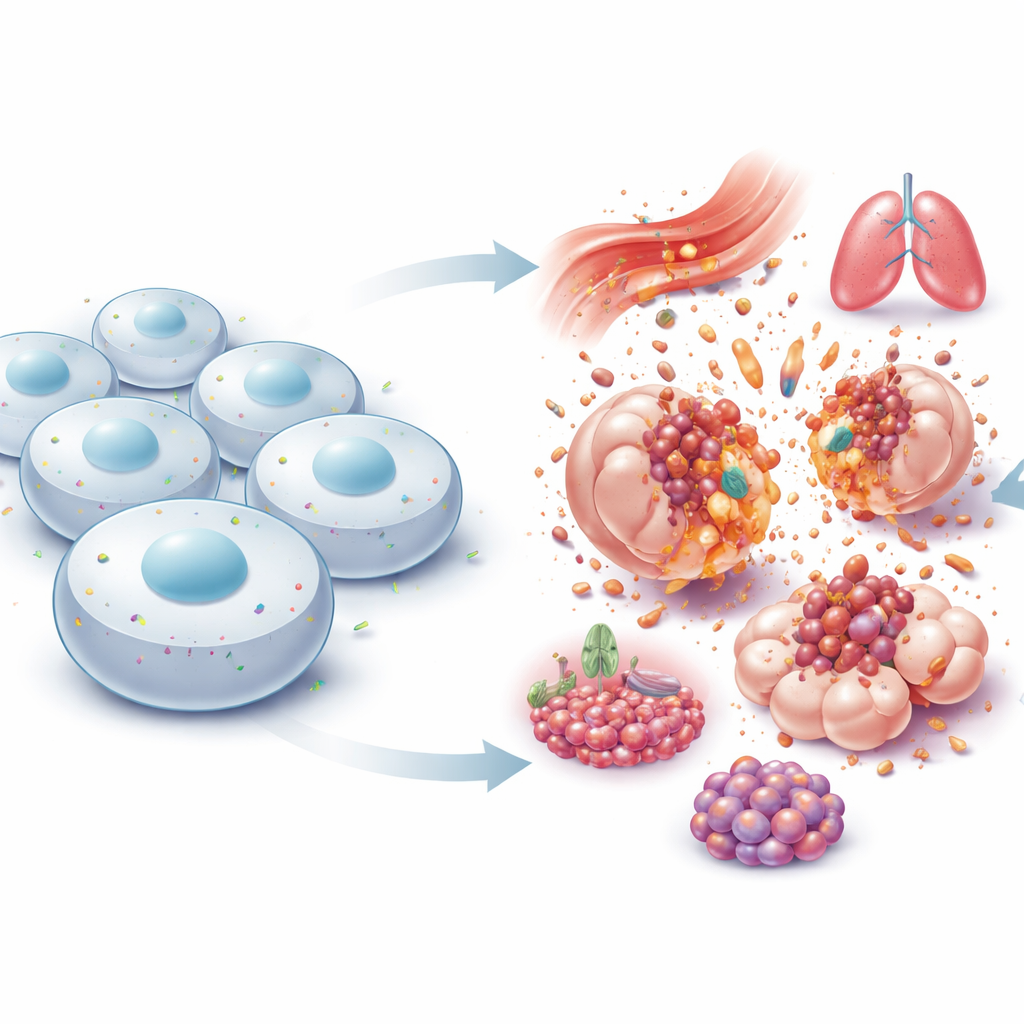
Ein winziger Wächter an der Zellkante
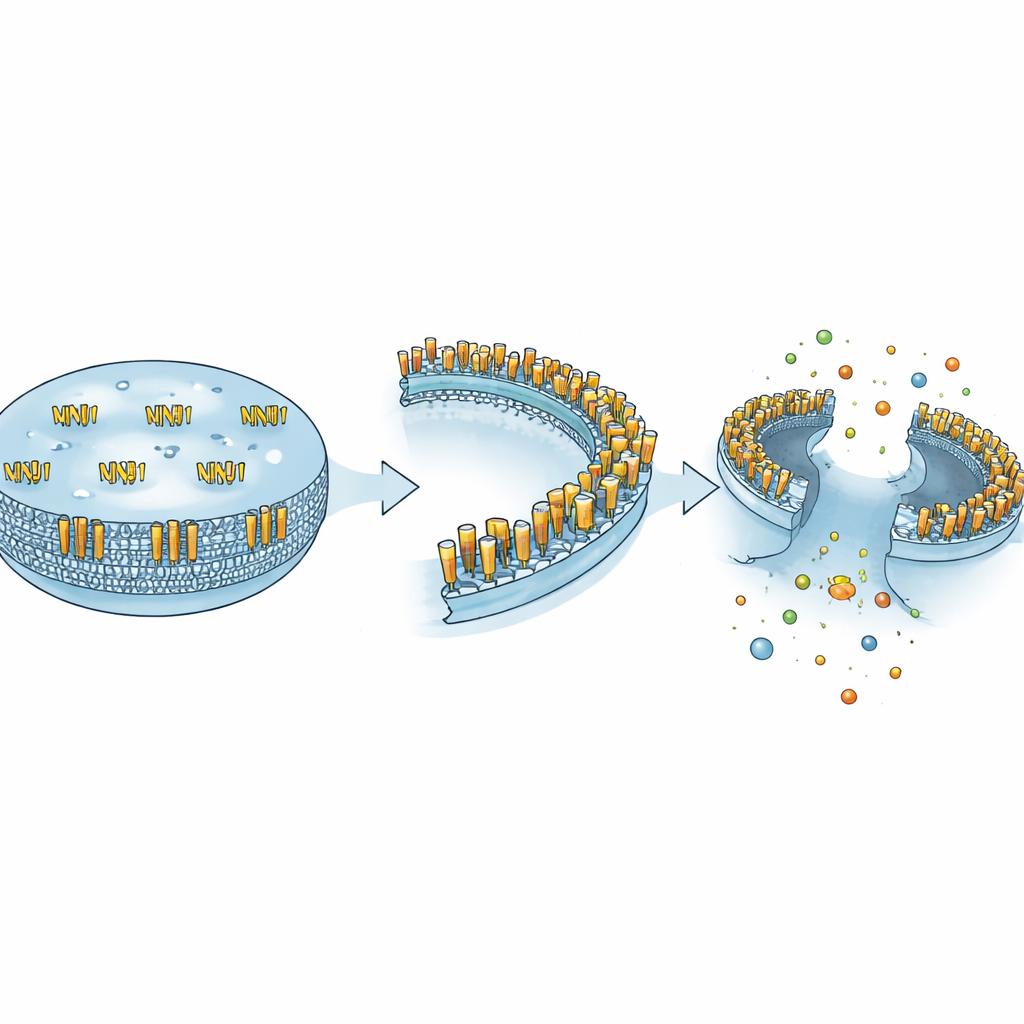
NINJ1 sitzt in der Außenmembran von Zellen und wurde ursprünglich in verletzten Nerven entdeckt, wo es offenbar das Nachwachsen beschädigter Fasern förderte. Jahrelang galt es als einfaches „haftendes“ Protein, das Zellen hilft, aneinanderzubleiben. Diese Sicht änderte sich 2021, als Forscher zeigten, dass NINJ1 der aktive Vollstrecker des letzten Risses bei vielen Formen explosiven Zelltods ist. Statt dass die Membran passiv versagt, verändern NINJ1-Moleküle ihre Form, sammeln sich zu großen ringförmigen Strukturen und schneiden Membranstücke heraus, sodass der Zellinhalt ins umliegende Gewebe ausströmt. Das kehrt die alte Vorstellung einer rein zufälligen Ruptur um und zeigt, dass der letzte Schritt des lytischen Zelltods selbst sorgfältig reguliert wird.
Ein Protein, drei Gesichter
Die Autoren argumentieren, dass sich NINJ1s scheinbar widersprüchliche Verhaltensweisen durch seine Fähigkeit erklären lassen, verschiedene physikalische Formen anzunehmen. Im ruhigen Zustand liegt NINJ1 überwiegend als einzelne Einheiten in Dimeren vor, die Zellen helfen, aneinander zu haften. Wenn eine schneidende Protease wie MMP‑9 sein äußeres Segment abtrennt, wird dieses Fragment in die umgebende Flüssigkeit freigesetzt und wirkt wie ein Chemokin – ein kleines Signal, das Immunzellen anzieht und lenkt. Unter starken Stresssignalen reorganisieren sich NINJ1-Einheiten hingegen zu großen oligomeren Ringen in der Membran, die Membranflächen herausschneiden und vollständige Rupturen verursachen. Diese drei Formen – adhesiv, löslicher Botenstoff und membranbildender „Schneider“ – verleihen einem Protein die Fähigkeit, Zellkontakte, Zellbewegung und Zelldemontage kontextabhängig zu steuern.
Wie das Aufplatzen von Zellen Gesundheit und Krankheit prägt
Weil NINJ1 darüber entscheidet, ob Zellen sanft verklingen oder explosiv platzen, steht es an der Schnittstelle vieler Erkrankungen. Bei entzündlichen Zuständen wie schwerer Pankreatitis oder Gicht verstärkt NINJ1‑vermittelte Ruptur Schmerz und Schwellung, indem Gefahrensignale aus sterbenden Zellen freigesetzt werden; das Blockieren von NINJ1 in Tiermodellen kann Gewebeschäden mildern. In Blutgefäßen führt NINJ1 ein Doppelspiel: bestimmte Formen verschlechtern diabetische Gefäßschäden, während sein lösliches Fragment Entzündungen in Arterioskleroseplaques dämpfen kann. Bei Infektionen hilft NINJ1‑vermitteltes Aufplatzen dem Körper, Mikroben freizulegen und Abwehrreaktionen zu mobilisieren, doch bei Sepsis und schweren Virusinfektionen kann derselbe Prozess überwältigende, systemische Entzündungen und Gerinnung antreiben. Im Gehirn und Nervensystem unterstützt NINJ1 in einigen Situationen Nervenregeneration und Gefäßreparatur, beteiligt sich jedoch auch an schädigenden Entzündungsprozessen nach Schlaganfall oder Trauma.
NINJ1 bei Krebs und künftigen Behandlungen
Auch beim Krebs zeigt NINJ1 wieder zwei Gesichter. Je nach Status des Tumorsuppressors p53 und den Signalen des umliegenden Gewebes kann es entweder das Tumorwachstum und die Ausbreitung fördern oder am Einleiten entzündlicher, therapieinduzierter Zelltodesprozesse mitwirken. Diese Komplexität macht NINJ1 zu einem verlockenden, aber riskanten Arzneimittelziel. Die Übersicht beschreibt aktuelle experimentelle Strategien: Naturstoffe und Vitamine, die NINJ1‑Spiegel senken, Aminosäuren und kleine Moleküle, die seine ringförmigen Assemblierungen verhindern, sowie designte Peptide oder Antikörper, die seine adhäsiven oder chemotaktischen Rollen blockieren. Die Autoren plädieren dafür, dass wirklich sichere Therapien „form‑spezifisch“ sein müssen – gezielt gegen die porenbildenden Ringe bei akuten Gewebeschäden, gegen das lösliche Fragment bei chronischer Entzündung oder gegen die adhäsive Form bei Erkrankungen, die durch schädlichen Immunzell‑Trafficking getrieben werden.
Den zellulären Abschalter in ein Arzneimittelziel verwandeln
Insgesamt schließt der Artikel, dass NINJ1 kein einfacher An‑/Aus‑Schalter des Zelltods ist, sondern eine vielseitige Steuerzentrale, deren Struktur ihre Funktion bestimmt. Indem es entscheidet, ob eine Zelle sich festhält, Hilfesignale sendet oder auseinanderbricht, verbindet NINJ1 Nervenreparatur, Immunität, Gefäßgesundheit, Infektionsergebnisse und Krebsverhalten. Um diesen Abschalter therapeutisch zu nutzen, wird präzise Kontrolle erforderlich sein – die schädliche Form in den richtigen Zellen zur richtigen Zeit zu treffen und gleichzeitig seine schützenden Rollen in Abwehr und Gewebereparatur zu erhalten. Gelingt diese Präzision, könnten NINJ1‑basierte Behandlungen einen neuen Weg eröffnen, schädliche Entzündungen und Zelltod bei vielen Erkrankungen zu zähmen.
Zitation: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Schlüsselwörter: NINJ1, Zelltod, Entzündung, Membranruptur, therapeutische Ziele