Clear Sky Science · ru
Роль NINJ1 в заболеваниях
Когда клетки выбирают взрыв
Наши клетки покрыты тонкими внешними оболочками, которые отделяют внутреннее пространство жизни от внешнего мира. Долгое время ученые полагали, что когда эти оболочки в конце концов рвутся при гибели клетки, это просто невезение — как лопнувший шарик. В этом обзоре показано, что на самом деле небольшая мембранная белок NINJ1 действует как встроенный демонтажный переключатель. Решая, когда и как клетки разрываются, NINJ1 формирует воспаление, восстановление нервов, рост сосудов, контроль инфекций и даже поведение рака — делая его привлекательной, но сложной мишенью для будущих лекарств.
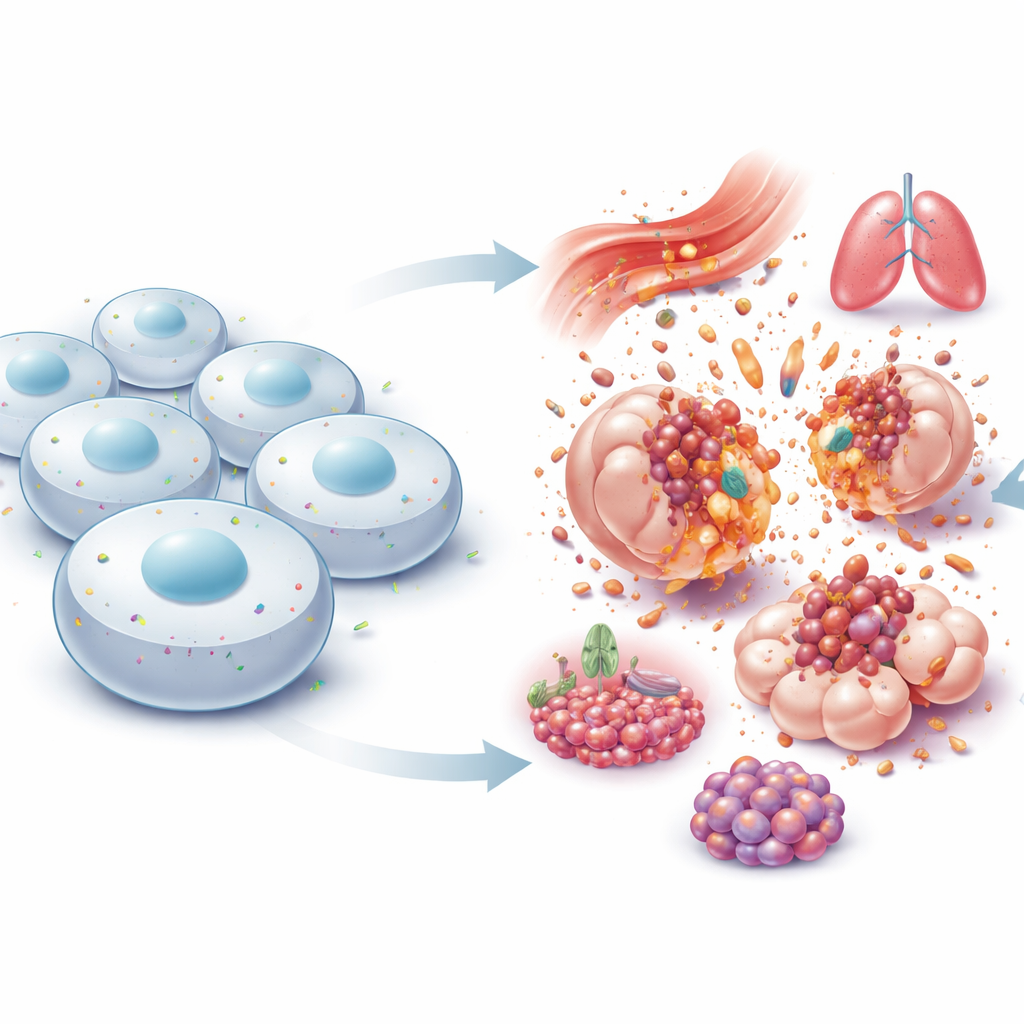
Крошечный шлагбаум на краю клетки
NINJ1 располагается во внешней мембране клеток и первоначально была обнаружена в поврежденных нервах, где, как казалось, помогает волокнам восстанавливаться. Годы считали её простой «липкой» белковой, позволяющей клеткам удерживаться друг за друга. Это представление изменилось в 2021 году, когда исследователи показали, что NINJ1 является активным исполнителем финального разрыва при многих формах взрывной гибели клеток. Вместо пассивной поломки мембраны молекулы NINJ1 меняют форму, собираются в крупные кольцеобразные структуры и вырезают участки мембраны, что позволяет содержимому клетки вылиться в окружающую ткань. Это опровергает старую идею о чисто случайном разрыве и демонстрирует, что последний этап лизисной гибели клеток сам по себе строго регулируется.
Один белок — три лица
Авторы утверждают, что кажущееся противоречивое поведение NINJ1 можно объяснить её способностью принимать разные физические формы. В спокойном состоянии NINJ1 существует преимущественно как одиночные единицы, спаренные в димеры, которые помогают клеткам прочно сцепляться. Когда протеаза, например MMP-9, отрезает её внешний сегмент, этот фрагмент высвобождается в окружающую жидкость и ведёт себя как хемокин — небольшой сигнальный молекула, привлекающая и направляющая иммунные клетки. Под сильными стрессовыми сигналами единицы NINJ1 переорганизуются в крупные олигомерные кольца, встраивающиеся в мембрану, которые вырезают участки мембраны и вызывают полный разрыв. Эти три формы — адгезивная, растворимая сигнальная и мембранная «резающая» — дают одному белку возможность контролировать клеточные контакты, миграцию клеток и их разрушение в зависимости от контекста.
Как разрыв клеток формирует здоровье и болезни
Поскольку NINJ1 регулирует, тихо ли клетки угасают или взрывоопасно разрываются, она находится на перекрестке многих заболеваний. При воспалительных состояниях, таких как тяжелый панкреатит или подагра, разрыв, опосредованный NINJ1, усиливает боль и отек, выпуская сигналы опасности из умирающих клеток; блокирование NINJ1 в моделях на животных может уменьшать повреждение ткани. В кровеносных сосудах NINJ1 имеет двойную природу: некоторые её формы усугубляют сосудистое повреждение при диабете, тогда как её растворимый фрагмент может утихомиривать воспаление в атеросклеротических бляшках. Во время инфекций разрыв, опосредованный NINJ1, помогает организму обнажать микробов и мобилизовать иммунную защиту, но при сепсисе и тяжёлых вирусных заболеваниях тот же процесс может подпитывать подавляющее, генерализованное воспаление и тромбообразование. В мозге и нервах NINJ1 способствует регенерации нервов и восстановлению сосудов в одних условиях, но также участвует в повреждающем воспалении после инсульта или травмы.
NINJ1 в раке и будущие подходы к лечению
В раке NINJ1 снова демонстрирует двойственность. В зависимости от статуса супрессора опухолей p53 и сигналов окружающей ткани она может либо способствовать росту и метастазированию опухоли, либо помогать запускать воспалительную, индуцированную терапией гибель клеток. Эта сложность делает NINJ1 заманчивой, но рискованной мишенью для лекарств. Обзор описывает текущие экспериментальные стратегии: природные соединения и витамины, понижающие уровни NINJ1; аминокислоты и малые молекулы, препятствующие её кольцевой сборке; и разработанные пептиды или антитела, блокирующие её адгезивные или хемотаксические функции. Авторы утверждают, что по-настоящему безопасные терапии должны быть «специфичны по форме» — нацелены на порообразующие кольца при остром повреждении ткани, на растворимый фрагмент при хроническом воспалении или на адгезивную форму при заболеваниях, вызванных вредной миграцией иммунных клеток.
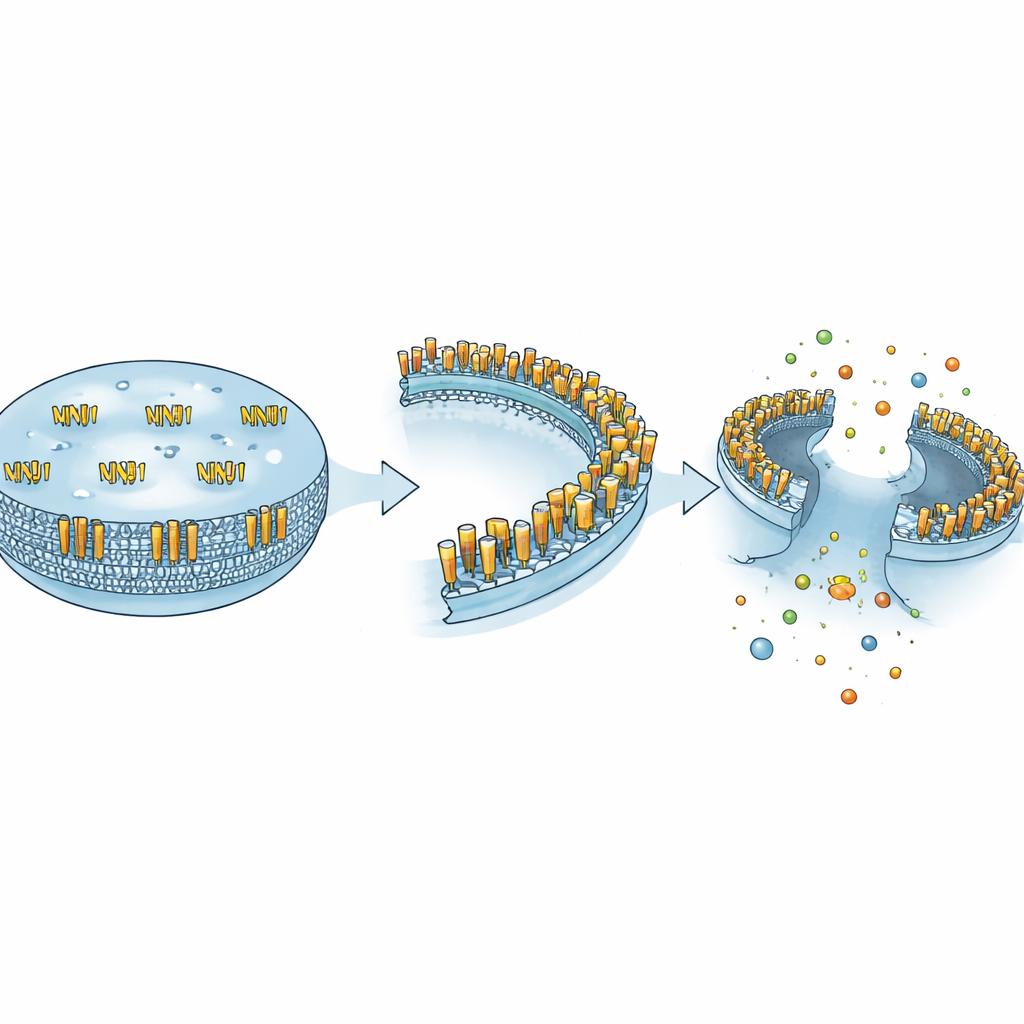
Превращение клеточного выключателя в лекарственную мишень
В целом статья делает вывод, что NINJ1 — не простой выключатель «вкл/выкл» для гибели клеток, а универсальный центр управления, чья структура определяет функцию. Решая, удержится ли клетка, пошлет ли она сигнал о помощи или разорвётся, NINJ1 связывает вместе восстановление нервов, иммунитет, здоровье сосудов, исходы инфекций и поведение рака. Использование этого «выключателя» в терапии потребует точного контроля — поражать вредную форму в нужных клетках в нужное время, сохраняя при этом её защитные роли в защите хозяина и восстановлении тканей. Если такую точность удастся достичь, препараты на основе NINJ1 могут предложить новый способ укротить пагубное воспаление и гибель клеток при широком спектре заболеваний.
Цитирование: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Ключевые слова: NINJ1, смерть клеток, воспаление, разрыв мембраны, терапевтические мишени