Clear Sky Science · nl
De rol van NINJ1 bij ziekten
Wanneer cellen ervoor kiezen te barsten
Onze cellen zijn omhuld door fragiele buitenlagen die het binnenste van het leven scheiden van de buitenwereld. Decennialang gingen wetenschappers ervan uit dat wanneer die lagen bij celdood uiteindelijk scheuren, dat gewoon een ongelukje was—als een ballon die knapt. Dit overzichtsartikel laat zien dat een klein membraaneiwit genaamd NINJ1 in plaats daarvan fungeert als een ingebouwde sloopknop. Door te bepalen wanneer en hoe cellen openbarsten, helpt NINJ1 ontsteking, zenuwherstel, bloedvatgroei, infectiebestrijding en zelfs kanker te sturen—waardoor het een aantrekkelijk maar lastig doelwit is voor toekomstige geneesmiddelen.
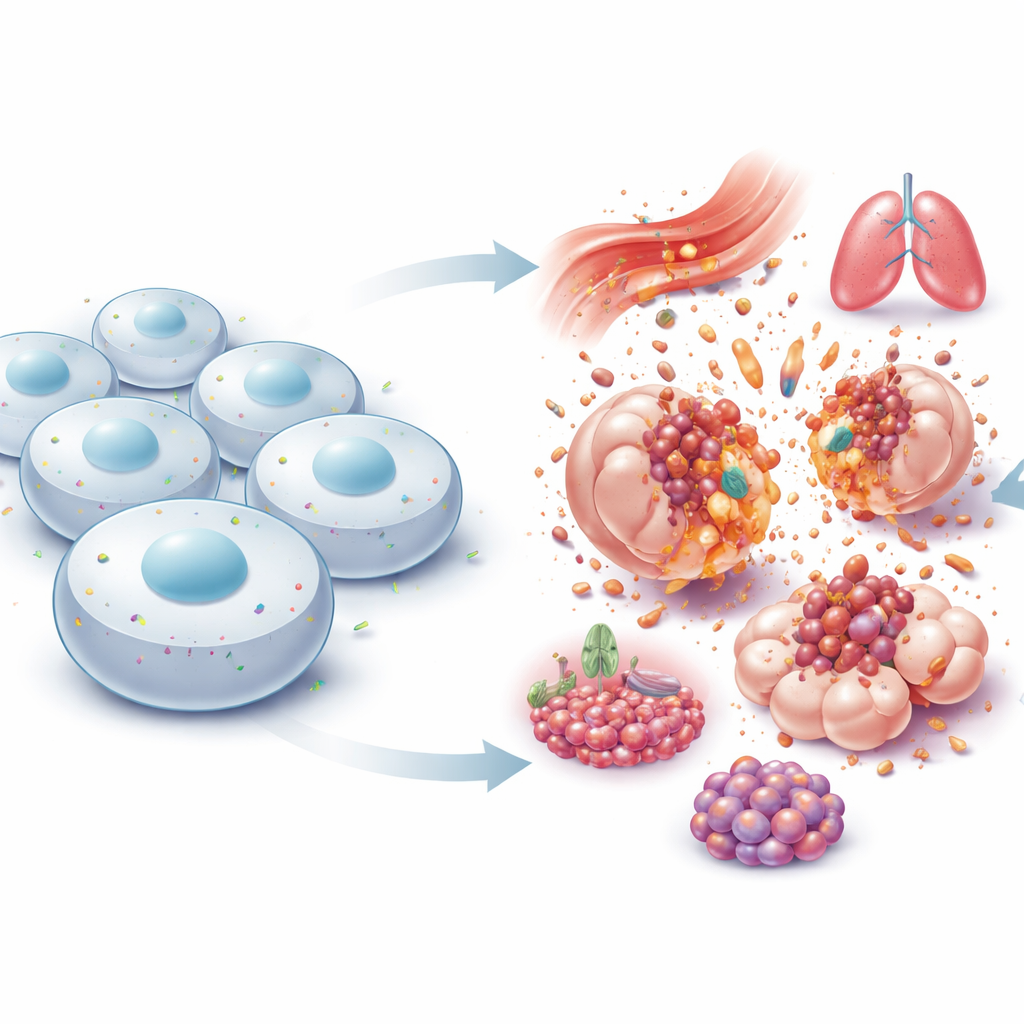
Een kleine poortwachter aan de rand van de cel
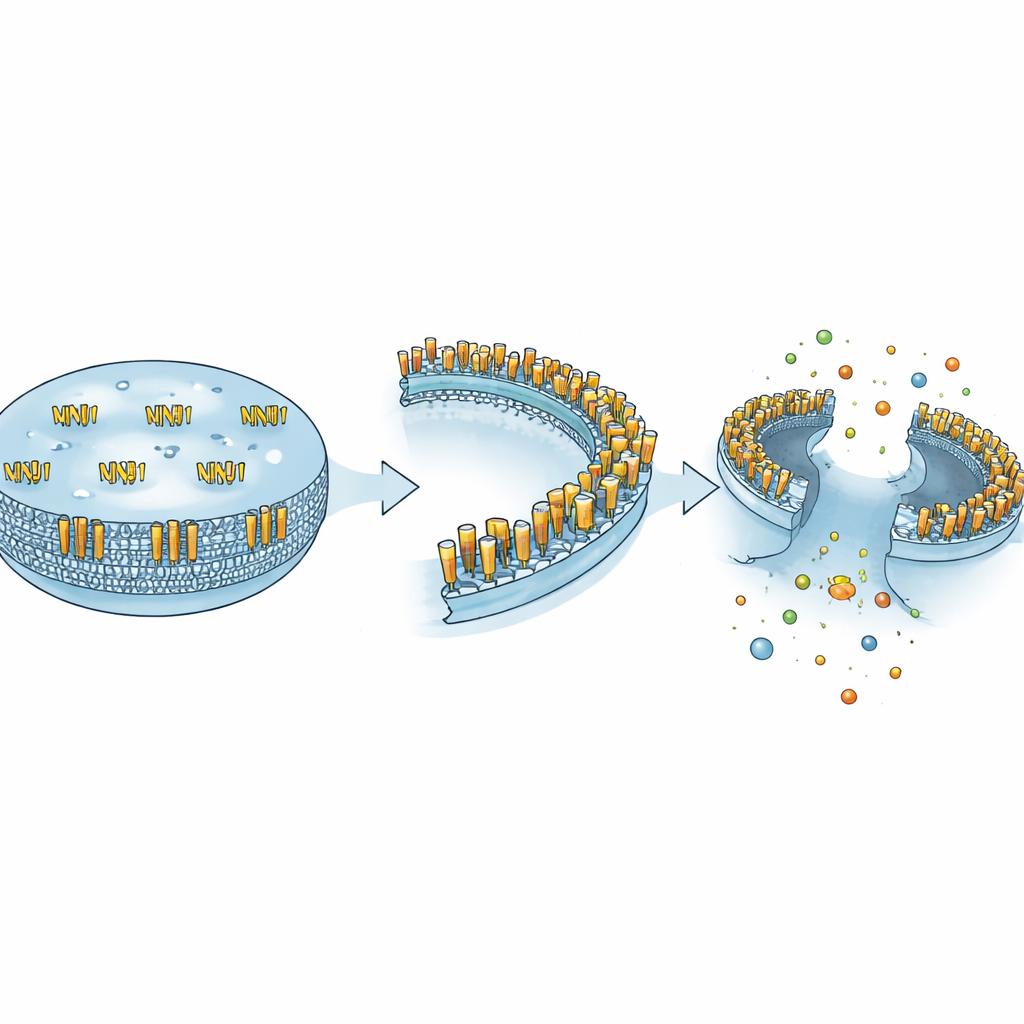
NINJ1 zit in het buitenmembraan van cellen en werd oorspronkelijk ontdekt in beschadigde zenuwen, waar het leek te helpen bij het teruggroeien van beschadigde vezels. Jarenlang werd het gezien als een eenvoudig “plakkerig” eiwit dat cellen aan elkaar liet hechten. Dat beeld veranderde in 2021, toen onderzoekers aantonen dat NINJ1 de actieve uitvoerder is van de laatste scheur bij veel vormen van explosieve celdood. In plaats van dat het membraan passief faalt, veranderen NINJ1-moleculen van vorm, verzamelen ze zich tot grote ringachtige structuren en snijden ze stukken uit het membraan, waardoor de inhoud van de cel in het omringende weefsel kan lekken. Dit weerlegt het oude idee van een puur toevallige ruptuur en laat zien dat de laatste stap van lytische celdood op zichzelf zorgvuldig gereguleerd is.
Eén eiwit, drie gedaanten
De auteurs betogen dat NINJ1’s ogenschijnlijk tegenstrijdige gedragingen begrepen kunnen worden uit het vermogen om verschillende fysische vormen aan te nemen. In de rustige toestand bestaat NINJ1 voornamelijk als enkelheden die paargewijs in dimeren voorkomen en helpen cellen aan elkaar te laten kleven. Wanneer een knipend enzym zoals MMP-9 zijn buitensegment afknipt, wordt dat fragment in de omliggende vloeistof vrijgegeven en gedraagt het zich als een chemokine—een klein signaal dat immuuncellen aantrekt en leidt. Onder sterke stresssignalen reorganiseren NINJ1-eenheden zich juist tot grote oligomere ringen verankerd in het membraan, die membraanpatches uitsnijden en volledige ruptuur veroorzaken. Deze drie vormen—adhesief, oplosbaar boodschapper en membraan-”snijder”—geven één eiwit de mogelijkheid om celcontact, celbeweging en celdemolitie te regelen, afhankelijk van de context.
Hoe celbarsten gezondheid en ziekte vormt
Omdat NINJ1 bepaalt of cellen zachtjes wegvallen of explosief uiteenbarsten, staat het op het kruispunt van veel ziekten. Bij ontstekingsaandoeningen zoals ernstige pancreatitis of jicht versterkt NINJ1-gedreven ruptuur pijn en zwelling door gevaarlijke signalen uit stervende cellen los te laten; het blokkeren van NINJ1 in diermodellen kan weefselschade verminderen. In bloedvaten heeft NINJ1 een dubbelrol: bepaalde vormen verergeren diabetesgerelateerde vaatschade, terwijl het oplosbare fragment ontsteking in arteriële plaques kan verminderen. Tijdens infecties helpt NINJ1-gemedieerde barstvorming het lichaam microben bloot te leggen en immuunreacties te mobiliseren, maar bij sepsis en ernstige virusziekten kan hetzelfde proces overweldigende, lichaamsbrede ontsteking en stolling aanwakkeren. In de hersenen en zenuwen ondersteunt NINJ1 in sommige omstandigheden zenuwregeneratie en vaatherstel, maar het draagt ook bij aan schadelijke ontsteking na een beroerte of trauma.
NINJ1 bij kanker en toekomstige behandelingen
Bij kanker toont NINJ1 opnieuw twee gezichten. Afhankelijk van de status van de tumorsuppressor p53 en de signalen in de omliggende weefsels, kan het zowel de tumorgroei en -verspreiding bevorderen als helpen ontstekingsgerelateerde, therapie-geïnduceerde celdood teweeg te brengen. Deze complexiteit maakt NINJ1 tot een verleidelijk maar risicovol geneesmiddeldoelwit. Het overzicht schetst huidige experimentele strategieën: natuurlijke verbindingen en vitamines die NINJ1-niveaus verlagen, aminozuren en kleine moleculen die de ringvormende assemblages verhinderen, en ontworpen peptiden of antilichamen die zijn adhesieve of chemotactische rollen blokkeren. De auteurs stellen dat echt veilige therapieën “vorm-specifiek” moeten zijn—gericht op de pore-vormende ringen bij acute weefselschade, op het oplosbare fragment bij chronische ontsteking, of op de adhesieve vorm bij ziekten die worden aangedreven door schadelijke immuunceltrajecten.
Een cellulaire sloopknop tot een medicijndoel maken
Al met al concluderen de auteurs dat NINJ1 geen eenvoudige aan/uit-schakelaar is voor celdood, maar een veelzijdig controlepunt waarvan de structuur zijn functie bepaalt. Door te beslissen of een cel vasthoudt, hulpsignalen uitstuurt of uiteenbarst, verbindt NINJ1 zenuwherstel, immuniteit, bloedvaten, infectie-uitkomsten en kankergedrag. Het benutten van deze sloopknop voor therapie vereist nauwkeurige controle—het schadelijke eiwitvorm in de juiste cellen op het juiste moment raken, terwijl de beschermende rollen in gastheerverdediging en weefselherstel behouden blijven. Als die precisie haalbaar is, zouden op NINJ1 gebaseerde behandelingen een nieuwe manier kunnen bieden om schadelijke ontsteking en celdood bij een breed scala aan ziekten te temperen.
Bronvermelding: Bao, S., Chen, F., Guo, Z. et al. The role of NINJ1 in diseases. Cell Death Discov. 12, 193 (2026). https://doi.org/10.1038/s41420-026-03064-4
Trefwoorden: NINJ1, celdood, ontsteking, membraanruptuur, therapeutische doelwitten