Clear Sky Science · tr
Yağ asidi oksidasyonu, asetil-CoA bağımlı H3K9ac yeniden programlanmasını yönlendirerek tiroid kanserinde BRAFV600E inhibisyonuna adaptif direnç gelişimini destekler
Tiroid kanseri olan kişiler için neden önemli
BRAFV600E adı verilen yaygın bir tiroid kanseri mutasyonuna yönelik hedefe yönelik ilaçlar, agresif hastalık yaşayan kişiler için umut vaat etti. Ancak birçok tümör ilk başta küçülüp ardından yeniden büyüyor; tedaviye rağmen hayatta kalmanın yollarını buluyor. Bu çalışma, kanser hücreleri içinde gizli bir kaçış yolunu ortaya koyuyor: yağ yakımını ve gen kontrolünü yeniden düzenleyen metabolik bir sapma; nihayetinde BRAF bloke edici ilaçların etkisini azaltıyor. Bu yolun anlaşılması, kanserin geri dönmesini engelleyecek yeni kombinasyon tedavilerine işaret edebilir.
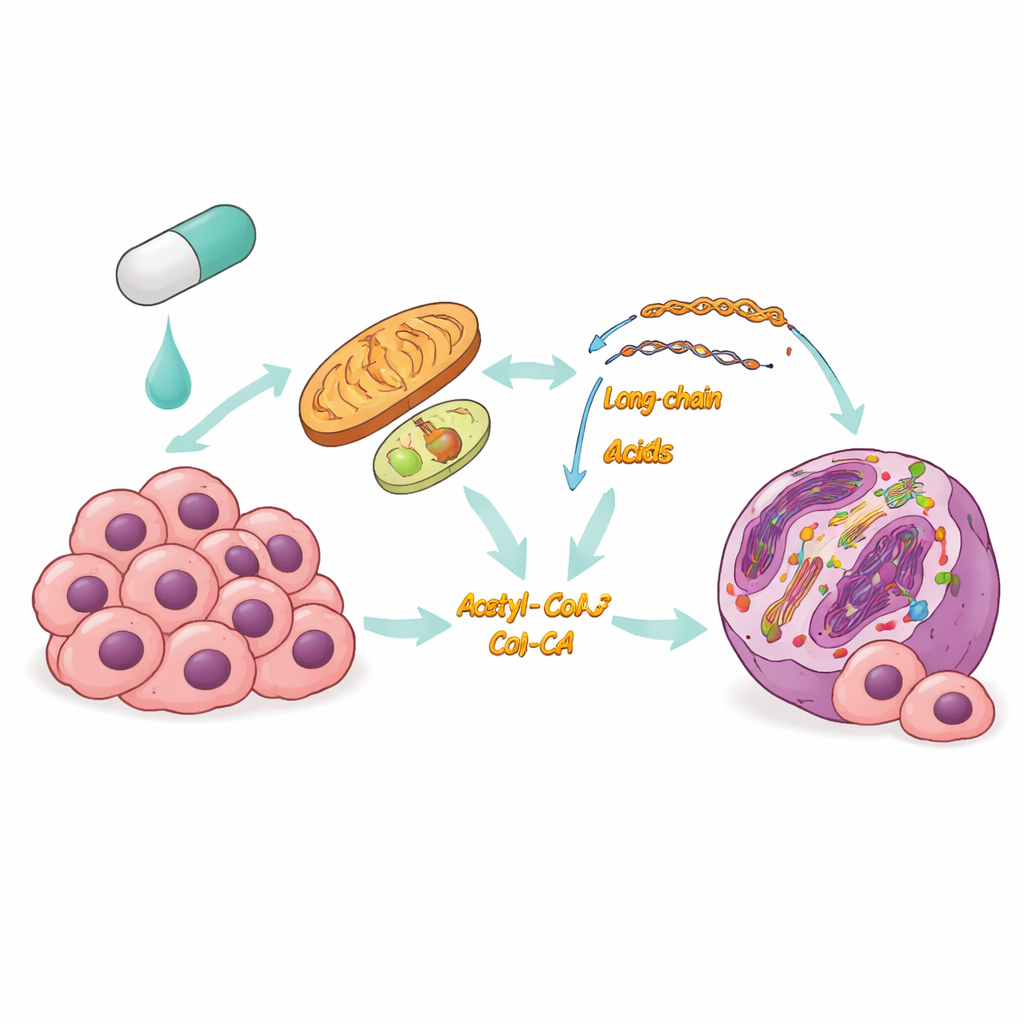
Mevcut hedefe yönelik tedavilerdeki sorun
Tiroid kanseri, hormon üreten bezlerin en sık görülen kanseridir ve birçok vaka yavaş ilerlese de bazı türler hızla yayılabilir ve tedavisi zordur. Bu agresif tümörlerde BRAFV600E sıklıkla büyümeyi yöneten anahtar bir rol oynar; bu da BRAF bloke edici ilaçları çekici bir strateji haline getirir. Ancak hastalarda yaygın olarak direnç gelişir: ilaçlar ilk başta işe yarar, sonra etkinliklerini kaybeder çünkü ayakta kalan kanser hücreleri uyum sağlar. Araştırmacılar, hücrelerin besin ve enerji yönetimindeki değişikliklerin bu uyumun temelinde olabileceğini düşündü, fakat ayrıntılar belirsizdi.
Kanser hücreleri hayatta kalmak için yakıtını değiştirir
Ekip, bir BRAF inhibitörüne maruz kalan tiroid kanseri hücrelerinde gen aktivitesi profillemesi ve metabolit ölçümlerinin bir kombinasyonunu kullandı. Şeker yakma yolları baskılanırken, hücrelerin yağ asidi oksidasyonunu keskin biçimde artırdığını—temelde glikoz yakımından mitokondri ve ilişkili bölmeler içinde yağ yakımına geçtiklerini—buldular. Yağları bu yola sokan anahtar enzimler yükseldi, yağ damlacıkları tüketildi ve hem oksijen kullanımı hem de enerji çıktısı arttı. Önemli olarak, bu değişim geçici bir tepki değildi: uzun dönem ilaç direnci geliştirmiş hücreler de yağ asidi oksidasyonunu açık tuttu; bu da BRAF blokajı altında temel bir hayatta kalma stratejisi olduğunu gösteriyordu.
Hücrenin talimat kitabını yeniden yazan metabolik bir sinyal
Yağ yakmak yalnızca enerjiyi sağlamaz. Yağ asitleri parçalandıkça asetil-CoA üretirler; bu küçük molekül, histon adı verilen DNA paketleyici proteinler üzerinde kimyasal etiketlerin yapı taşı olarak da görev yapar. Araştırmacılar, BRAF inhibisyonu altında artan yağ asidi oksidasyonunun asetil-CoA düzeylerini yükselttiğini ve bunun da H3K9 asetilasyonu olarak bilinen özgül bir histon modifikasyonunu artırdığını gösterdi. Bu modifikasyon yerel DNA yapısını gevşetir ve yakındaki genleri aktive etme eğilimindedir. Ekip, thioridazine ile yağ asidi oksidasyonunu bloke ettiğinde asetil-CoA’nın düştüğünü ve bu asetilasyon işaretinin azaldığını; asetil-CoA’yı yenileyen bir öncü eklenirse kısmi olarak geri geldiğini gösterdi. Genom çapında haritalama, artmış asetilasyonun hayatta kalma ve terapi direnciyle ilişkili genlerin promotörleri yakınında kümelendiğini ortaya koydu.
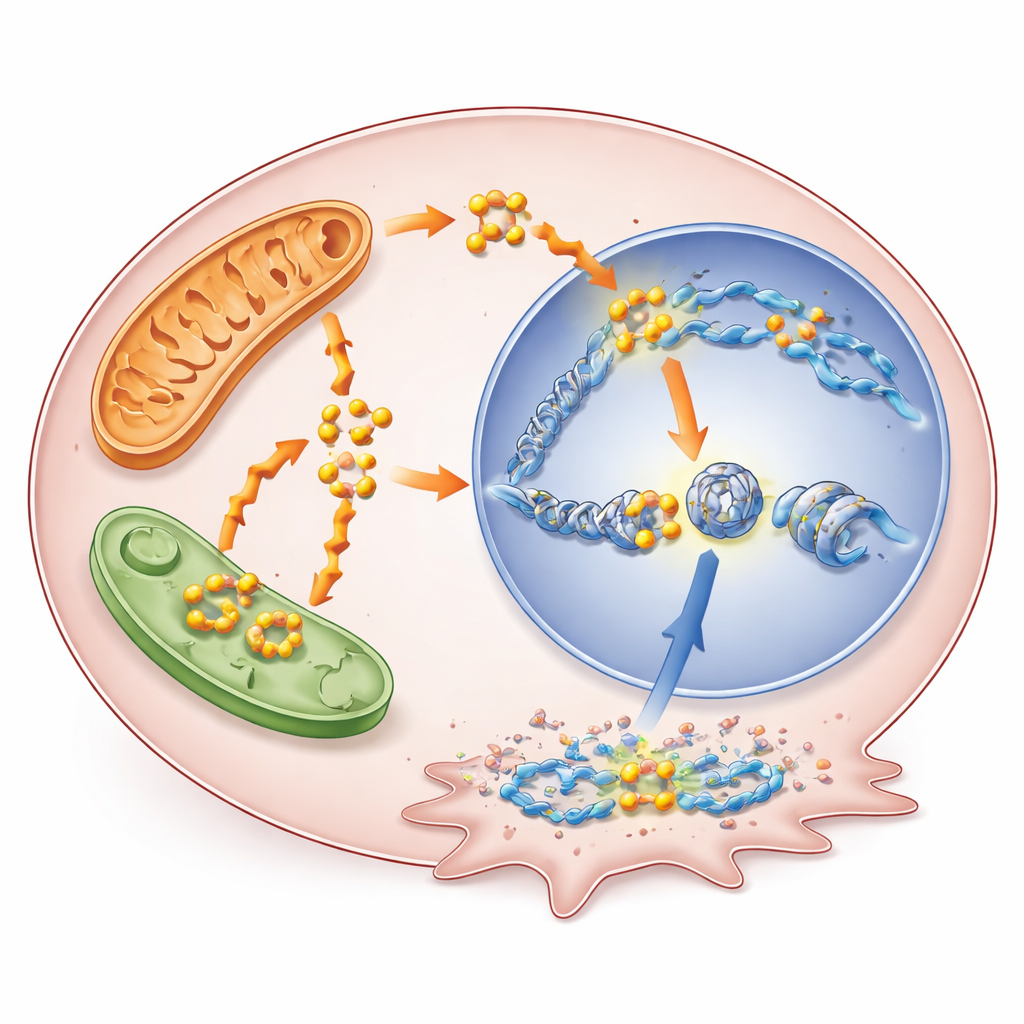
Yeni öne çıkan bir problem yaratan gen
Bu şekilde açılan genler arasında RUNX1 öne çıktı. RUNX1, daha önce diğer kanserlerde ilaç direnciyle ilişkilendirilmiş bir transkripsiyon faktörüdür—gen kontrol proteinidir—ancak tiroid tümörlerinde yeterince incelenmemiştir. Burada, BRAF bloke edildiğinde RUNX1’in düzenleyici bölgeleri ek H3K9 asetilasyonu kazandı ve etkinliği birçok tiroid kanseri modelinde, kronik direnç gelişmiş hücreler dahil, yükseldi. Hasta tümör verilerinde yüksek RUNX1 düzeyleri daha ileri evre hastalık, lenf nodu yayılımı ve daha kötü sonuçlarla koreleydi. Bilim insanları tiroid kanseri hücrelerinde RUNX1’i baskıladıklarında, bu hücreler daha yavaş büyüdü ve göç ile invazyon yetenekleri azaldı; bu da tümörleri daha agresif hale getirmede doğrudan bir rolünü işaret ediyor.
Kaçış yolunu kesmek için tedavileri birleştirmek
Yağ asidi oksidasyonu ve RUNX1’in her ikisi de BRAF inhibisyonuna karşı hücrelerin dayanmasına yardım ediyor gibi göründüğünden, araştırmacılar bu yolları bloke etmenin mevcut ilaçları daha etkili kılıp kılamayacağını test etti. Hücre hatlarında, yağ asidi oksidasyonu engelleyicisi ile BRAF inhibitörlerinin eşleştirilmesi tek başına kullanılan her iki ilaçtan daha fazla kanser hücresi ölümüne yol açtı. İnsan tiroid tümör greftleri taşıyan farelerde kombinasyon, tek başına BRAF inhibisyonundan daha etkili bir şekilde tümörleri küçülttü. Benzer bir strateji, bir hasta örneğinden yetiştirilen mini-tümör organoidinde klinikte kullanılan BRAF ve MEK inhibitör ikilisinin etkisini artırdı. Paralel olarak, RUNX1’in küçük-molekül inhibitörü tiroid kanseri hücrelerini BRAF hedefli tedaviye karşı daha hassas hale getirdi; bu da bu metabolik–epigenetik eksenin terapötik olarak hedef alınabilir olduğunu pekiştiriyor.
Gelecekteki bakım için ne anlama geliyor
Uzman olmayanlar için temel mesaj şudur: Bazı tiroid kanserleri hedefe yönelik tedaviye, hem yakıt tercihini hem de DNA okunuşunu değiştirerek dayanır. Daha fazla yağ yakarak hücreler, RUNX1 gibi hayatta kalmayı destekleyen genleri açan bir kimyasal sinyal üretir ve BRAF bloke edici ilaçlara uyum sağlamalarına yardımcı olur. Bu zinciri kesmek—ya yağ yıkımını engelleyerek ya da RUNX1 etkinliğini azaltarak—kanser hücrelerini tedavi altında ölme olasılığı daha yüksek hale getirir. Bu bulgular henüz preklinik olmakla birlikte, metabolizmayı hedef alan ilaçların mevcut hedefe yönelik tedavilerle kombinasyonunu içeren gelecekteki çalışmalara açık ve mantıklı bir gerekçe sunuyor; bu da agresif tiroid kanserinde direnci geciktirmek veya aşmak için umut veriyor.
Atıf: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
Anahtar kelimeler: tiroid kanseri, BRAF inhibisyonu, yağ asidi oksidasyonu, epigenetik yeniden programlama, ilaç direnci