Clear Sky Science · fr
L’oxydation des acides gras alimente une reprogrammation dépendante de l’acétyl-CoA de H3K9ac favorisant la résistance adaptative à l’inhibition de BRAFV600E dans le cancer de la thyroïde
Pourquoi cela importe pour les personnes atteintes d’un cancer de la thyroïde
Les médicaments ciblés qui visent une mutation courante du cancer de la thyroïde, appelée BRAFV600E, ont suscité de l’espoir chez les patients atteints de tumeurs agressives. Pourtant, de nombreux cancers diminuent d’abord puis rebondissent, trouvant des moyens de survivre malgré le traitement. Cette étude révèle une voie d’échappement cachée au sein des cellules cancéreuses : un détour métabolique qui réoriente leur combustion des lipides et la régulation de leurs gènes, réduisant finalement l’efficacité des médicaments bloquant BRAF. Comprendre cette voie pourrait indiquer de nouvelles combinaisons thérapeutiques pour empêcher la rechute du cancer.
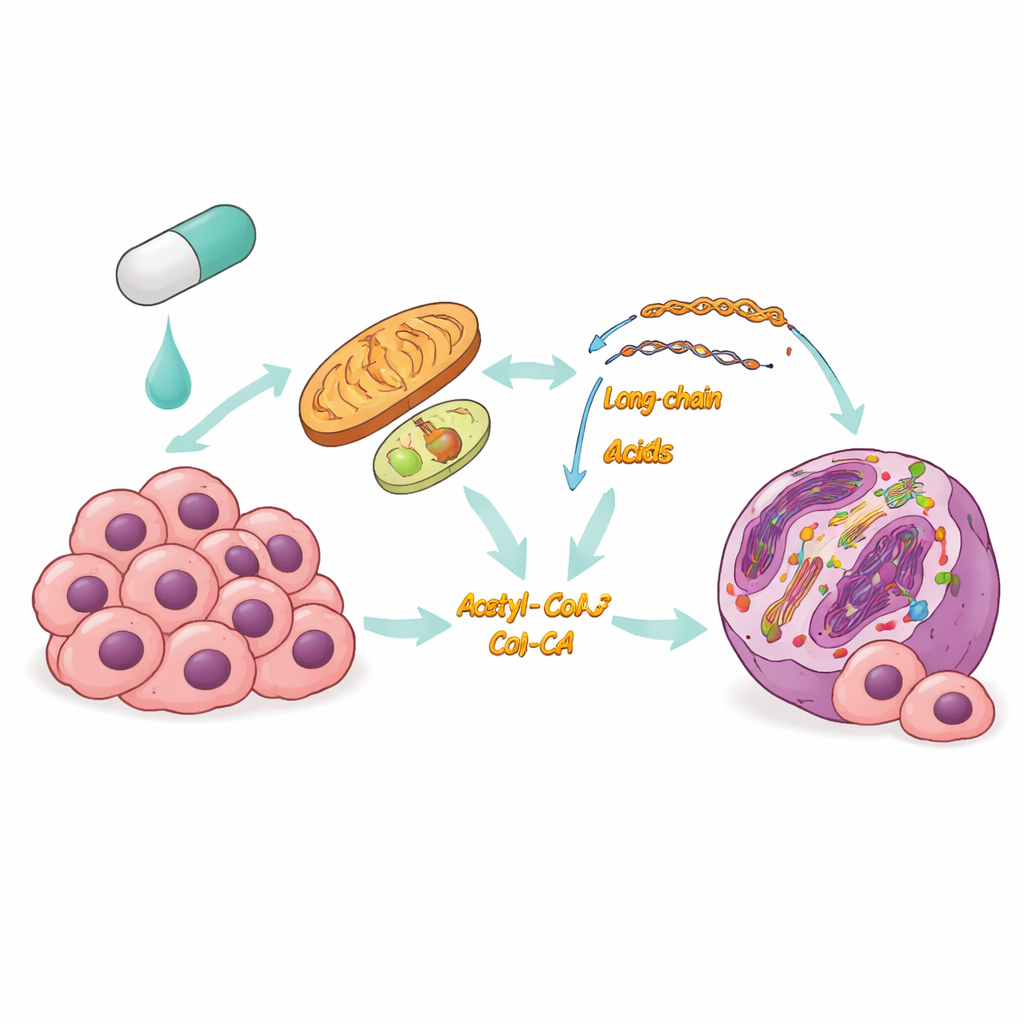
Le problème des traitements ciblés actuels
Le cancer de la thyroïde est le cancer le plus fréquent des glandes endocrines et, si de nombreux cas évoluent lentement, certaines formes se propagent rapidement et sont difficiles à traiter. Dans ces tumeurs agressives, BRAFV600E agit souvent comme un interrupteur maître qui stimule la croissance, faisant des inhibiteurs de BRAF une stratégie séduisante. Cependant, les patients développent couramment une résistance : les médicaments fonctionnent au départ, puis perdent de leur efficacité à mesure que les cellules cancéreuses survivantes s’adaptent. Les chercheurs soupçonnaient que des changements dans la gestion des nutriments et de l’énergie pouvaient sous-tendre cette adaptation, mais les détails restaient flous.
Les cellules cancéreuses changent de carburant pour survivre
L’équipe a utilisé une combinaison de profils d’activité génique et de mesures de métabolites dans des cellules de cancer de la thyroïde exposées à un inhibiteur de BRAF. Ils ont constaté que, tandis que les voies de combustion du glucose étaient atténuées, les cellules augmentaient fortement l’oxydation des acides gras — passant essentiellement de la combustion du glucose à celle des lipides dans les mitochondries et compartiments associés. Les enzymes clés qui acheminent les lipides vers cette voie ont été suractivées, les gouttelettes lipidiques ont été consommées, et l’utilisation d’oxygène ainsi que la production d’énergie ont augmenté. Il est important de noter que ce basculement n’était pas éphémère : les cellules ayant développé une résistance à long terme au médicament maintenaient l’oxydation des acides gras activée, ce qui suggère qu’il s’agit d’une stratégie de survie centrale sous blocage de BRAF.
Un signal métabolique qui réécrit le manuel d’instructions de la cellule
La combustion des lipides fait plus que maintenir l’énergie. Lorsqu’ils sont dégradés, les acides gras génèrent de l’acétyl-CoA, une petite molécule qui sert également de précurseur pour des marques chimiques sur les protéines d’emballage de l’ADN appelées histones. Les chercheurs ont montré que l’augmentation de l’oxydation des acides gras sous inhibition de BRAF élevait les niveaux d’acétyl-CoA, ce qui augmentait à son tour une modification histone spécifique connue sous le nom d’acétylation de H3K9. Cette modification assouplit localement la structure de l’ADN et tend à activer les gènes voisins. Lorsque l’équipe a bloqué l’oxydation des acides gras avec le médicament thioridazine, l’acétyl-CoA a diminué et cette marque d’acétylation a chuté ; l’ajout d’un précurseur reconstituant l’acétyl-CoA la rétablit partiellement. Le cartographie à l’échelle du génome a révélé que l’acétylation accrue se concentrait près des promoteurs de gènes impliqués dans la survie et la résistance thérapeutique.
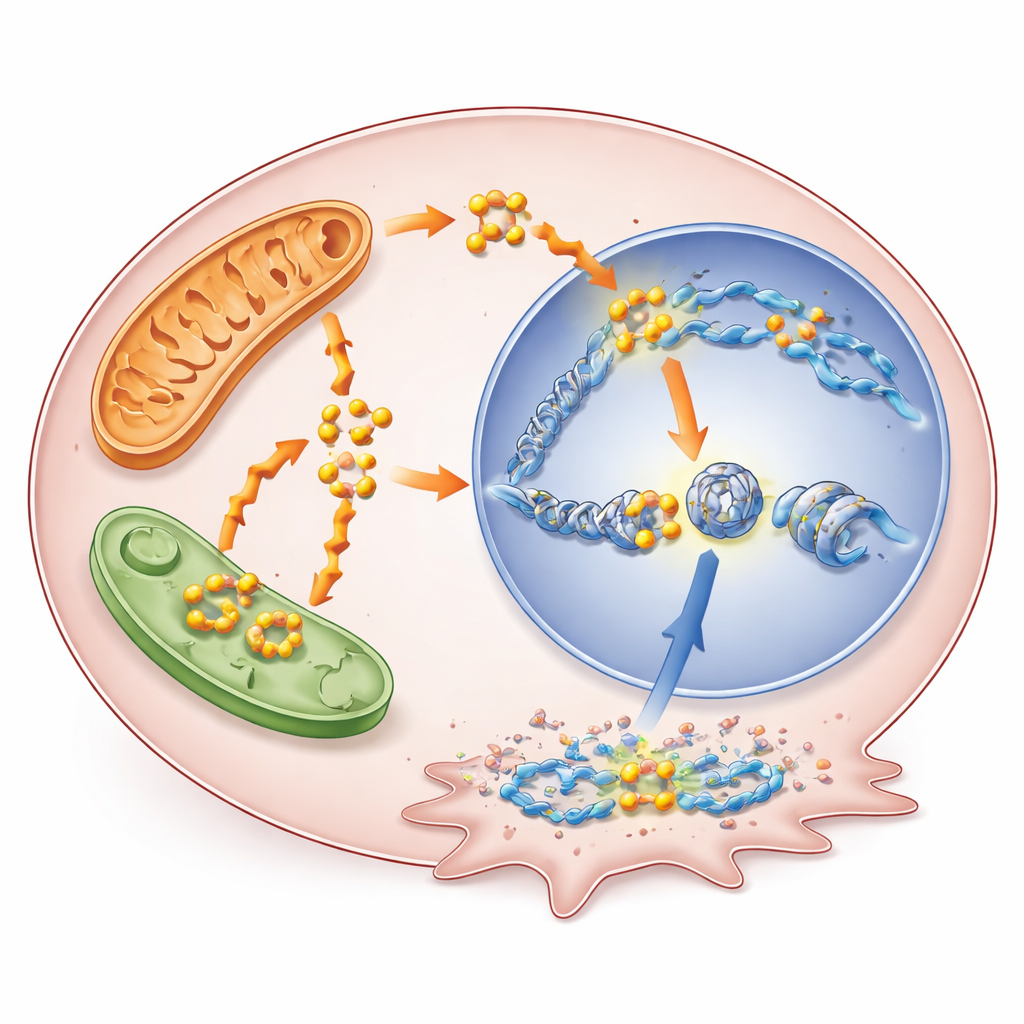
Un gène nouvellement mis en évidence comme fauteur de troubles
Parmi les gènes activés de cette façon, un appelé RUNX1 s’est distingué. RUNX1 est un facteur de transcription — une protéine de contrôle génique — précédemment impliqué dans la résistance aux médicaments dans d’autres cancers, mais peu étudié dans les tumeurs thyroïdiennes. Ici, ses régions régulatrices ont gagné en acétylation H3K9 lorsque BRAF était bloqué, et son activité a augmenté dans plusieurs modèles de cancer de la thyroïde, y compris des cellules devenues chroniquement résistantes. Des niveaux élevés de RUNX1 dans les données tumorales de patients corrélaient avec une maladie plus avancée, une dissémination ganglionnaire et des résultats plus défavorables. Lorsque les scientifiques ont réduit l’expression de RUNX1 dans des cellules de cancer thyroïdien, ces cellules ont proliféré plus lentement et étaient moins capables de migrer et d’envahir, ce qui suggère un rôle direct dans l’agressivité tumorale.
Combiner les traitements pour couper la voie d’échappement
Parce que l’oxydation des acides gras et RUNX1 semblaient aider les cellules à résister à l’inhibition de BRAF, les chercheurs ont testé si bloquer ces voies pouvait rendre les traitements existants plus puissants. Dans des lignées cellulaires, associer un bloqueur de l’oxydation des acides gras à des inhibiteurs de BRAF a provoqué plus de mort cellulaire cancéreuse que chaque médicament seul. Chez des souris porteuses de greffons tumoraux humains de la thyroïde, la combinaison a réduit les tumeurs plus efficacement que l’inhibition de BRAF seule. Une stratégie similaire a renforcé l’effet d’une double combinaison clinique BRAF/MEK dans un organoïde tumoral issu d’un échantillon de patient. Parallèlement, un inhibiteur de petite molécule ciblant RUNX1 a rendu les cellules de cancer thyroïdien plus sensibles à la thérapie ciblée contre BRAF, renforçant l’idée que cet axe métabolique–épigénétique est exploitable thérapeutiquement.
Ce que cela signifie pour les soins futurs
Pour les non-spécialistes, le message clé est que certains cancers de la thyroïde survivent aux traitements ciblés en changeant à la fois leur choix de carburant et la lecture de leur ADN. En brûlant davantage de lipides, les cellules génèrent un signal chimique qui ouvre des gènes favorisant la survie comme RUNX1, ce qui les aide à s’adapter aux médicaments bloquant BRAF. Interrompre cette chaîne — soit en bloquant la dégradation des acides gras, soit en atténuant l’activité de RUNX1 — rend les cellules cancéreuses plus susceptibles de mourir sous traitement. Bien que ces résultats soient encore précliniques, ils donnent une justification claire pour des futurs essais combinant des médicaments ciblant le métabolisme avec les thérapies ciblées existantes afin de retarder ou surmonter la résistance dans les cancers thyroïdiens agressifs.
Citation: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
Mots-clés: cancer de la thyroïde, inhibition de BRAF, oxydation des acides gras, reprogrammation épigénétique, résistance aux médicaments