Clear Sky Science · ar
أكسدة الأحماض الدهنية تحفّز إعادة برمجة H3K9ac المعتمدة على أسيتيل-كوإنزيم A لتعزيز المقاومة التكيفية ضد تثبيط BRAFV600E في سرطان الغدة الدرقية
لماذا هذا يهم مرضى سرطان الغدة الدرقية
الأدوية المُستهدفة التي تصيب طفرة شائعة في سرطان الغدة الدرقية تسمى BRAFV600E أثارت آمالاً لمرضى المصابين بأورام عدوانية. ومع ذلك، تنكمش العديد من الأورام في البداية ثم تعاود الانتفاخ، متنقلةً طرقًا للبقاء على قيد الحياة رغم العلاج. تكشف هذه الدراسة عن طريق هروب داخل الخلايا السرطانية: التفافٌ استقلابي يعيد توصيل كيفية حرقها للدهون وكيفية التحكم في جيناتها، ما يضعف في النهاية أثر أدوية حجب BRAF. فهم هذا المسار قد يشير إلى تراكيب علاجية جديدة تمنع عودة الورم.
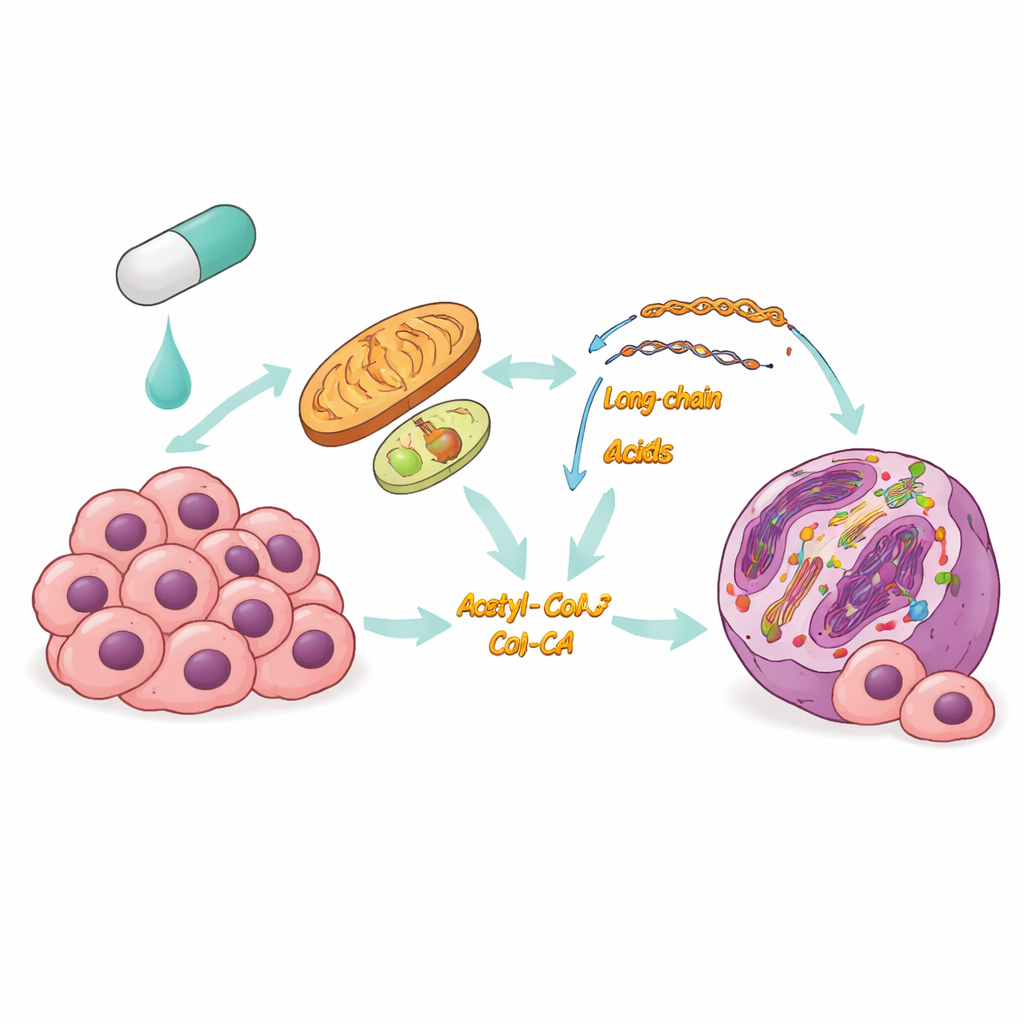
المشكلة في العلاجات المستهدفة الحالية
سرطان الغدة الدرقية هو الأكثر شيوعًا بين سرطانات الغدد الصماء، وبينما تكون كثير من الحالات بطيئة النمو، بعض الأنماط قد تنتشر بسرعة ويصعب علاجها. في هذه الأورام العدوانية، غالبًا ما يعمل BRAFV600E كمفتاح رئيسي يدفع النمو، مما يجعل أدوية حجب BRAF استراتيجية جذابة. ومع ذلك، يطوّر المرضى مقاومة شائعة: تنجح الأدوية في البداية ثم تفقد فاعليتها مع تكيف الخلايا السرطانية الناجية. افترض الباحثون أن تغييرات في كيفية تعامل الخلايا مع المغذيات والطاقة قد تكون وراء هذا التكيف، لكن التفاصيل كانت غير واضحة.
الخلايا السرطانية تغيّر مصدر وقودها للبقاء
استخدم الفريق مزيجًا من معايرة نشاط الجينات وقياسات المستقلبات في خلايا سرطان الغدة الدرقية المعرضة لمثبط BRAF. وجدوا أنه بينما تقلصت مسارات حرق السكر، زادّت الخلايا بقوة من أكسدة الأحماض الدهنية — بمعنى أنها انتقلت من حرق الجلوكوز إلى حرق الدهون داخل الميتوكوندريا ومُخازن مرتبطة. صعدت مستويات الإنزيمات الرئيسية التي تُدخل الدهون في هذا المسار، استُهلكت قطرات الدهون، وزاد كل من استهلاك الأكسجين وإنتاج الطاقة. والأهم أن هذا التحوّل لم يكن مؤقتًا: الخلايا التي طورت مقاومة طويلة الأمد للمركب أبقت أكسدة الأحماض الدهنية مفعلة، ما يشير إلى أنها استراتيجية بقاء أساسية تحت حجب BRAF.
إشارة استقلابية تعيد كتابة تعليمات الخلية
حرق الدهون يفعل أكثر من مجرد إبقاء الأضواء مضاءة. أثناء تفكيك الأحماض الدهنية تتولد جزيئات أسيتيل-كوإنزيم A، وهي جزيئات صغيرة تعمل أيضًا كلبنات لبناء وشاخصات كيميائية على بروتينات تغليف الحمض النووي المسماة النيوكليوسومات (الهستونات). أظهر الباحثون أن ارتفاع أكسدة الأحماض الدهنية تحت تثبيط BRAF عزز مستويات الأسيتيل-كوإنزيم A، مما أدى بدوره إلى زيادة تعديل هستوني محدد يعرف بأسيتلة H3K9. هذا التعديل يرخّي بنية الحمض النووي محليًا ويميل إلى تنشيط الجينات القريبة. عندما عطّل الفريق أكسدة الأحماض الدهنية باستخدام الدواء ثيوريدازين، انخفض الأسيتيل-كوإنزيم A وهبطت هذه العلامة الأسيتيلية؛ وإضافة سلف يعيد تخليق الأسيتيل-كوإنزيم A استعادت العلامة جزئيًا. كشفت خرائط على مستوى الجينوم أن الزيادة في الأسيتلة تركزت بالقرب من محفزات جينات متورطة في البقاء ومقاومة العلاج.
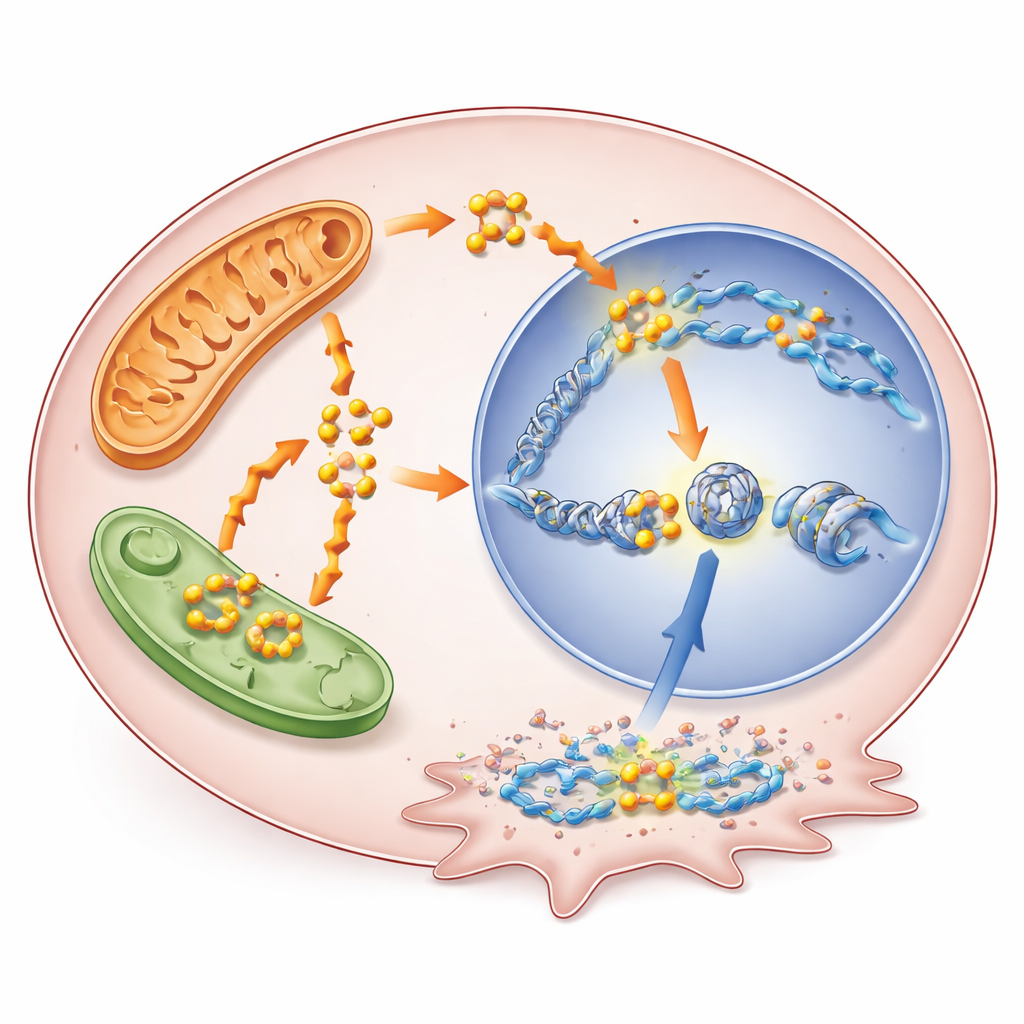
جين مزعج جديد بالملف
من بين الجينات التي نُشِطت بهذه الطريقة، برز جين يُدعى RUNX1. RUNX1 هو عامل نسخي — بروتين يتحكم في الجينات — وقد رُبط سابقًا بمقاومة الأدوية في سرطانات أخرى، لكنه لم يُدرس جيدًا في أورام الغدة الدرقية. هنا، اكتسبت مناطق التنظيم الخاصة به مزيدًا من أسيتلة H3K9 عند حجب BRAF، وارتفع نشاطه في نماذج متعددة من سرطان الغدة الدرقية، بما في ذلك الخلايا التي أصبحت مقاومة مزمنة. لدى بيانات مرضى الأورام، ارتبطت مستويات RUNX1 العالية بمرحلة مرض متقدمة، وانتشار للعقد اللمفاوية، وسوء النتائج. عند خفض RUNX1 في خلايا سرطان الغدة الدرقية، نمت تلك الخلايا أبطأ وكانت أقل قدرة على الهجرة والغزو، ما يشير إلى دور مباشر في جعل الأورام أكثر عدوانية.
الدمج العلاجي لقطع طريق الهروب
لأن كلًا من أكسدة الأحماض الدهنية وRUNX1 بدا أنهما يساعدان الخلايا على تحمل تثبيط BRAF، اختبر الباحثون ما إذا كان حجب هذه المسارات يمكن أن يجعل الأدوية الحالية أقوى. في خطوط خلوية، أدى الجمع بين مانع لأكسدة الأحماض الدهنية ومثبطات BRAF إلى وفاة خلوية سرطانية أكثر مما يفعله أي دواء بمفرده. في فئران حاملة لزرعات أورام بشرية من الغدة الدرقية، قلّص المزيج الأورام بفعالية أكبر من تثبيط BRAF وحده. عزّزت استراتيجية مماثلة أثر مجموعة سريرية مستخدمة من مثبطي BRAF وMEK في عضوية ورمية مصغرة نمت من عينة مريض. وبالتوازي، جعل مثبط جزيئي صغير لـ RUNX1 خلايا سرطان الغدة الدرقية أكثر عرضة للعلاج المستهدف ضد BRAF، مما يدعم فكرة أن هذا المحور الاستقلابي-الفوق وراثي قابل للاستغلال علاجيًا.
ماذا يعني هذا لرعاية المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن بعض سرطانات الغدة الدرقية تنجو من العلاج المستهدف من خلال تغيير كلٍّ من اختيار الوقود وكيفية قراءة حمضها النووي. بحرق مزيد من الدهون، تولد الخلايا إشارة كيميائية تفتح جينات تعزز البقاء مثل RUNX1، مما يساعدها على التكيّف مع أدوية حجب BRAF. قطع هذه السلسلة — إما عبر منع تفكك الأحماض الدهنية أو بتخفيف نشاط RUNX1 — يجعل الخلايا السرطانية أكثر عرضة للموت أثناء العلاج. بينما لا تزال هذه النتائج ما قبل سريرية، فإنها تضع مبررًا واضحًا لتجارب مستقبلية تجمع أدوية موجهة للاستقلاب مع العلاجات المستهدفة القائمة لتأخير أو التغلب على المقاومة في سرطان الغدة الدرقية العدواني.
الاستشهاد: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
الكلمات المفتاحية: سرطان الغدة الدرقية, تثبيط BRAF, أكسدة الأحماض الدهنية, إعادة برمجة فوق وراثية, مقاومة الدواء