Clear Sky Science · de
Fettsäureoxidation treibt acetyl‑CoA‑abhängige H3K9ac‑Umschreibung voran und fördert adaptive Resistenz gegen BRAF V600E‑Hemmung bei Schilddrüsenkrebs
Warum das für Menschen mit Schilddrüsenkrebs wichtig ist
Gezielte Medikamente, die auf eine häufige Schilddrüsenkrebs‑Mutation namens BRAF V600E abzielen, haben Hoffnungen bei Patienten mit aggressiver Erkrankung geweckt. Viele Tumoren schrumpfen zwar anfangs, schlagen dann aber zurück und finden Wege, trotz Behandlung zu überleben. Diese Studie deckt eine verborgene Fluchtstrecke innerhalb der Krebszellen auf: eine metabolische Umleitung, die umstellt, wie sie Fette verbrennen und ihre Gene regulieren, und dadurch die Wirkung von BRAF‑blockierenden Arzneien abschwächt. Das Verständnis dieses Wegs könnte auf neue Kombinationstherapien hinweisen, die verhindern, dass der Krebs zurückkommt.
Das Problem mit aktuellen zielgerichteten Behandlungen
Schilddrüsenkrebs ist die häufigste Krebserkrankung der hormonproduzierenden Drüsen; während viele Fälle langsam wachsen, können bestimmte Formen schnell streuen und schwer zu behandeln sein. In diesen aggressiven Tumoren wirkt BRAF V600E oft als Hauptschalter, der das Wachstum antreibt, weshalb BRAF‑blockierende Medikamente eine attraktive Strategie darstellen. Patienten entwickeln jedoch häufig Resistenzen: Die Medikamente wirken zunächst, verlieren dann aber an Wirksamkeit, wenn sich überlebende Krebszellen anpassen. Forscher vermuteten, dass Veränderungen im Umgang der Zellen mit Nährstoffen und Energie dieser Anpassung zugrunde liegen könnten, doch die Details waren unklar.
Krebszellen wechseln den Brennstoff, um zu überleben
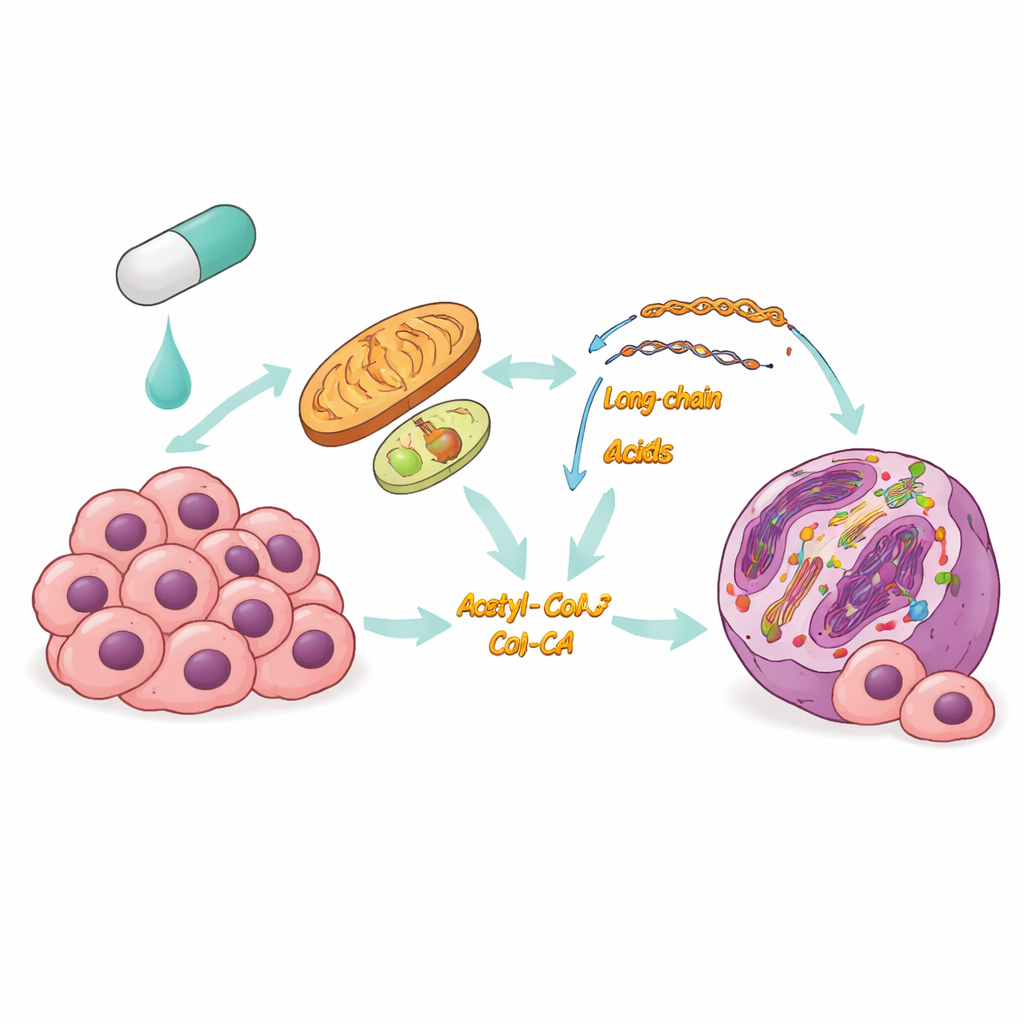
Das Team nutzte eine Kombination aus Genaktivitätsprofilierung und Messungen von Metaboliten in Schilddrüsenzellen, die einem BRAF‑Inhibitor ausgesetzt waren. Sie stellten fest, dass während die zuckerverbrennenden Wege gedämpft wurden, die Zellen die Fettsäureoxidation deutlich erhöhten – im Grunde wechselten sie vom Glukose‑ zum Fettstoffwechsel in Mitochondrien und verwandten Kompartimenten. Schlüsselenzyme, die Fette in diesen Weg leiten, wurden hochreguliert, Lipidtropfen wurden verbraucht und sowohl Sauerstoffverbrauch als auch Energieoutput stiegen. Wichtig ist, dass dieser Wechsel kein flüchtiger Effekt war: Zellen, die langfristig resistente Eigenschaften entwickelt hatten, behielten die Fettsäureoxidation bei, was darauf hindeutet, dass sie eine zentrale Überlebensstrategie unter BRAF‑Blockade darstellt.
Ein metabolisches Signal, das das Bedienungsbuch der Zelle umschreibt
Fettverbrennung leistet mehr als nur Energieversorgung. Beim Abbau von Fettsäuren entsteht Acetyl‑CoA, ein kleines Molekül, das auch als Baustein für chemische Markierungen an den DNA‑verpackenden Proteinen, den Histonen, dient. Die Forscher zeigten, dass die erhöhte Fettsäureoxidation unter BRAF‑Hemmung die Acetyl‑CoA‑Spiegel anhob, was wiederum eine spezifische Histonmodifikation, bekannt als H3K9‑Acetylierung, verstärkte. Diese Modifikation lockert die lokale DNA‑Struktur und aktiviert tendenziell nahegelegene Gene. Wenn das Team die Fettsäureoxidation mit dem Wirkstoff Thioridazin blockierte, fielen die Acetyl‑CoA‑Werte und die Acetylierungsmarke sank; die Zugabe einer Vorstufe, die Acetyl‑CoA wieder auffüllt, stellte sie teilweise wieder her. Genomweite Kartierungen zeigten, dass die erhöhte Acetylierung in der Nähe von Promotoren von Genen gebündelt war, die an Überleben und Therapie‑Resistenz beteiligt sind.
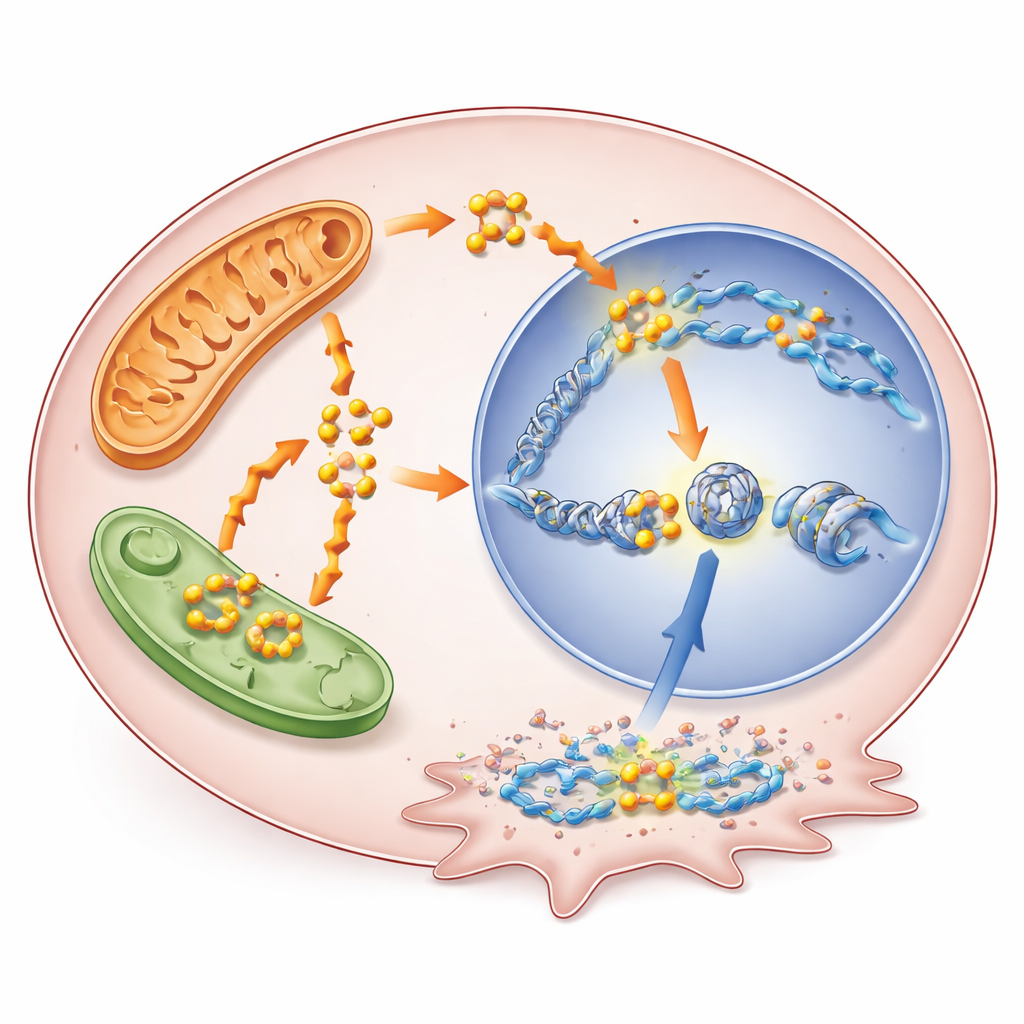
Ein neu hervorgehobenes Schädling‑Gen
Unter den auf diese Weise aktivierten Genen stach eines namens RUNX1 hervor. RUNX1 ist ein Transkriptionsfaktor – ein Genkontrollprotein –, das zuvor in anderen Krebsarten mit Arzneimittelresistenz in Verbindung gebracht wurde, aber in Schilddrüsentumoren wenig untersucht war. Hier erhielten seine regulatorischen Regionen bei BRAF‑Blockade zusätzliche H3K9‑Acetylierung, und seine Aktivität stieg in mehreren Schilddrüsenkrebsmodellen, einschließlich Zellen, die chronisch resistent geworden waren. Hohe RUNX1‑Spiegel in Patientendaten korrelierten mit fortgeschrittener Erkrankung, nodaler Metastasierung und schlechterem Verlauf. Wenn die Wissenschaftler RUNX1 in Schilddrüsenzellen herunterregulierten, wuchsen diese Zellen langsamer und waren weniger fähig zu migrieren und zu invasieren, was auf eine direkte Rolle bei der Verschärfung der Tumoraggressivität hinweist.
Kombinationstherapien, um die Fluchtroute abzuschneiden
Da sowohl Fettsäureoxidation als auch RUNX1 den Zellen offenbar halfen, BRAF‑Hemmung zu überstehen, prüften die Forscher, ob das Blockieren dieser Wege existierende Medikamente verstärken könnte. In Zelllinien führte die Kombination eines Fettsäureoxidationshemmers mit BRAF‑Inhibitoren zu mehr Krebszelltod als jedes der beiden Medikamente allein. Bei Mäusen mit menschlichen Schilddrüsentumor‑Grafts schrumpften die Tumoren unter der Kombination wirksamer als unter alleiniger BRAF‑Hemmung. Eine ähnliche Strategie verstärkte die Wirkung eines klinisch eingesetzten Doppelblocks aus BRAF‑ und MEK‑Inhibitoren in einem aus einer Patientenprobe gezüchteten Mini‑Tumor‑Organoid. Parallel dazu machte ein kleinmolekularer RUNX1‑Inhibitor Schilddrüsenzellen anfälliger für BRAF‑gerichtete Therapie, was die Idee stützt, dass diese metabolisch‑epigenetische Achse therapeutisch nutzbar ist.
Was das für die zukünftige Versorgung bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft: Einige Schilddrüsenkrebse überleben gezielte Behandlung, indem sie sowohl ihre Brennstoffwahl als auch die Art und Weise ändern, wie ihre DNA gelesen wird. Durch verstärkte Fettverbrennung erzeugen die Zellen ein chemisches Signal, das Überlebensgene wie RUNX1 öffnet und ihnen hilft, sich an BRAF‑blockierende Medikamente anzupassen. Das Unterbrechen dieser Kette – entweder durch Blockade des Fettabbaus oder durch Dämpfung der RUNX1‑Aktivität – macht die Krebszellen wahrscheinlicher, unter Therapie abzusterben. Auch wenn diese Befunde noch präklinisch sind, liefern sie eine klare Begründung für künftige Studien, die stoffwechselorientierte Medikamente mit bestehenden zielgerichteten Therapien kombinieren, um Resistenz bei aggressivem Schilddrüsenkrebs hinauszuzögern oder zu überwinden.
Zitation: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
Schlüsselwörter: Schilddrüsenkrebs, BRAF‑Hemmung, Fettsäureoxidation, epigenetische Umprogrammierung, Arzneimittelresistenz