Clear Sky Science · he
חמצון חומצות שומן מדרבן רה-תכנות תלוי אצטיל-CoA של H3K9ac כדי לקדם עמידות אדפטיבית לעיכוב BRAFV600E בסרטן התריס
מדוע זה חשוב לאנשים עם סרטן התריס
תרופות ממוקדות שמכוונות למוטציה נפוצה בסרטן התריס, שנקראת BRAFV600E, עוררו תקווה למטופלים עם מחלה אגרסיבית. עם זאת, גידולים רבים מצטמצמים בתחילה ואז חוזרים לגדול, ומוצאים דרכים לשרוד למרות הטיפול. המחקר הזה חושף נתיב נמלט נסתר בתוך תאי הסרטן: סטת מטבוליזם שמשנה את הדרך שבה הם שורפים שומנים ושולטים על הביטוי הגני, ובסופו של דבר מחלישה את השפעת התרופות החוסמות את BRAF. הבנת נתיב זה עשויה להצביע על קומבינציות טיפוליות חדשות שמונעות מהסרטן לחזור.
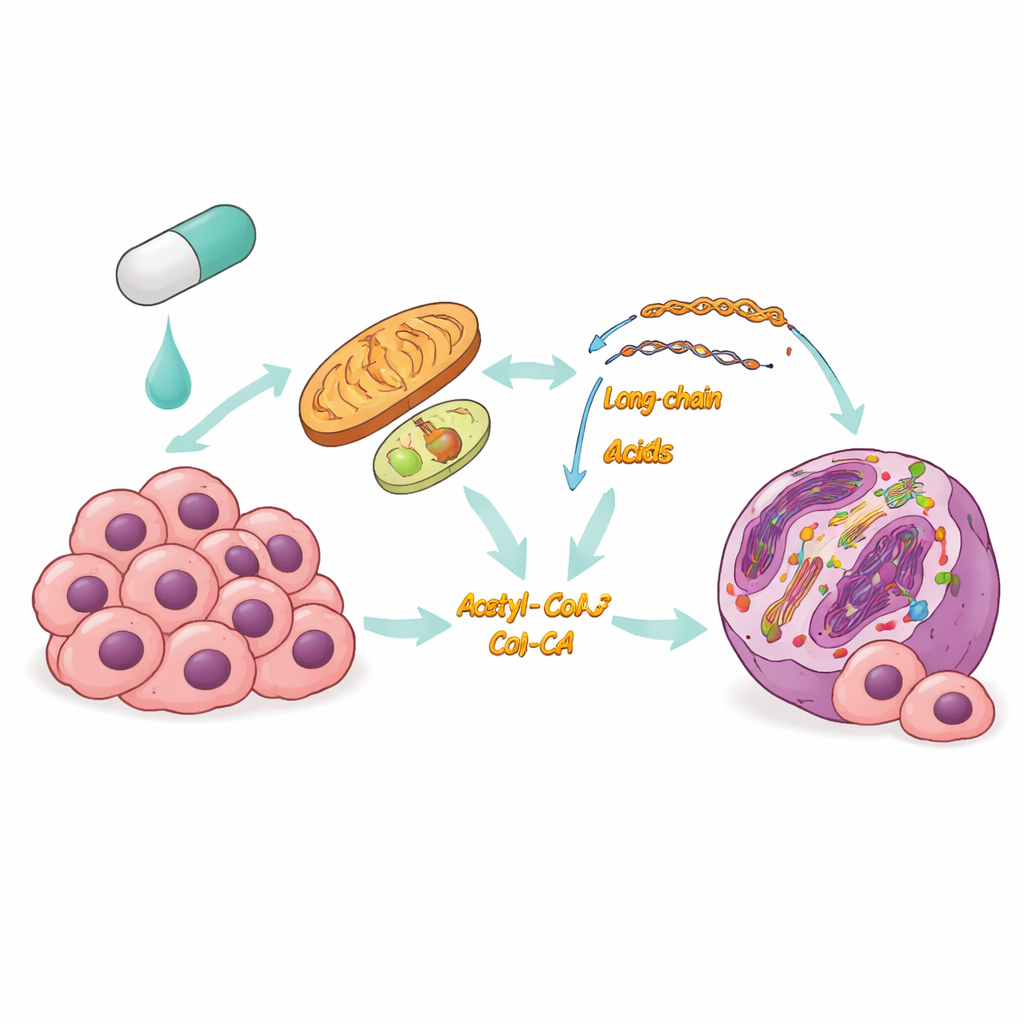
הבעיה עם הטיפולים הממוקדים הנוכחיים
סרטן התריס הוא הסרטן השכיח ביותר של בלוטות ההפרשה ההורמונלית, ובזמן שרבים מהמקרים צומחים באיטיות, צורות מסוימות יכולות להתפשט במהירות ולהיות קשות לטיפול. בגידולים אגרסיביים אלה, BRAFV600E משמש לעתים כמתג מרכזי שמניע גדילה, מה שהופך חוסמי BRAF לאסטרטגיה מושכת. עם זאת, מטופלים בדרך כלל מפתחים עמידות: התרופות פועלות בתחילה ואז מאבדות יעילות ככל שתאי הסרטן שורדים ומסתגלים. החוקרים חשדו ששינויים באופן שבו התאים מנהלים חומרים מזינים ואנרגיה עשויים לעמוד בבסיס הסתגלות זו, אך הפרטים היו לא ברורים.
תאי הסרטן משנים דלק כדי לשרוד
הצוות השתמש בשילוב של פרופיל ביטוי גנים והמדידות מטבוליטיות בתאי סרטן התריס שנתונים לעיכוב BRAF. הם מצאו שבעוד מסלולי שריפת הסוכר הושתקו, התאים הגבירו באופן חזק את חמצון חומצות השומן — למעשה החלפת דלק משריפת גלוקוז לשריפת שומנים בתוך המיטוכונדריה ומחלקות קשורות. אנזימים מרכזיים שמזינים שומנים למסלול זה הוגברו, טיפות שומן צורכו, ושני צריכת החמצן ותפוקת האנרגיה עלו. חשוב: המעבר הזה לא היה ברק חלבוני חולף — תאים שפיתחו עמידות ארוכת טווח שמרו על חמצון חומצות שומן פעיל, דבר המצביע כי זה אסטרטגיית הישרדות מרכזית תחת חסימת BRAF.
אות מטבולי שמכתיב מחדש את ספר ההוראות של התא
שריפת שומנים עושה יותר מאשר לשמור על התא פועל. כאשר חומצות שומן נשברות, הן יוצרות אצטיל-CoA, מולקולה קטנה שגם משמשת כאבן בניין לתגיות כימיות על חלבוני אריזת ה-DNA הנקראים היסטונים. החוקרים הראו שחמצון חומצות שומן מוגבר תחת עיכוב BRAF הגביר את רמות האצטיל-CoA, שבעקבותיהן עלתה מודיפיקציה היסטונית ספציפית הידועה כאצטילציה של H3K9. מודיפיקציה זו מרחיבה את מבנה ה-DNA בסביבתה ונוטה להפעיל גנים סמוכים. כשהצוות חסם חמצון שומנים בעזרת התרופה תיאורידאזין, האצטיל-CoA ירד וסימן האצטילציה נחלש; הוספת קדם-חומר שמחדש אצטיל-CoA השיבה חלקית את האצטילציה. מיפוי ברמת הגנום חשף שהאצטילציה המוגברת רוכזה בקרבת פרומוטורים של גנים המעורבים בהישרדות ובעמידות לטיפול.
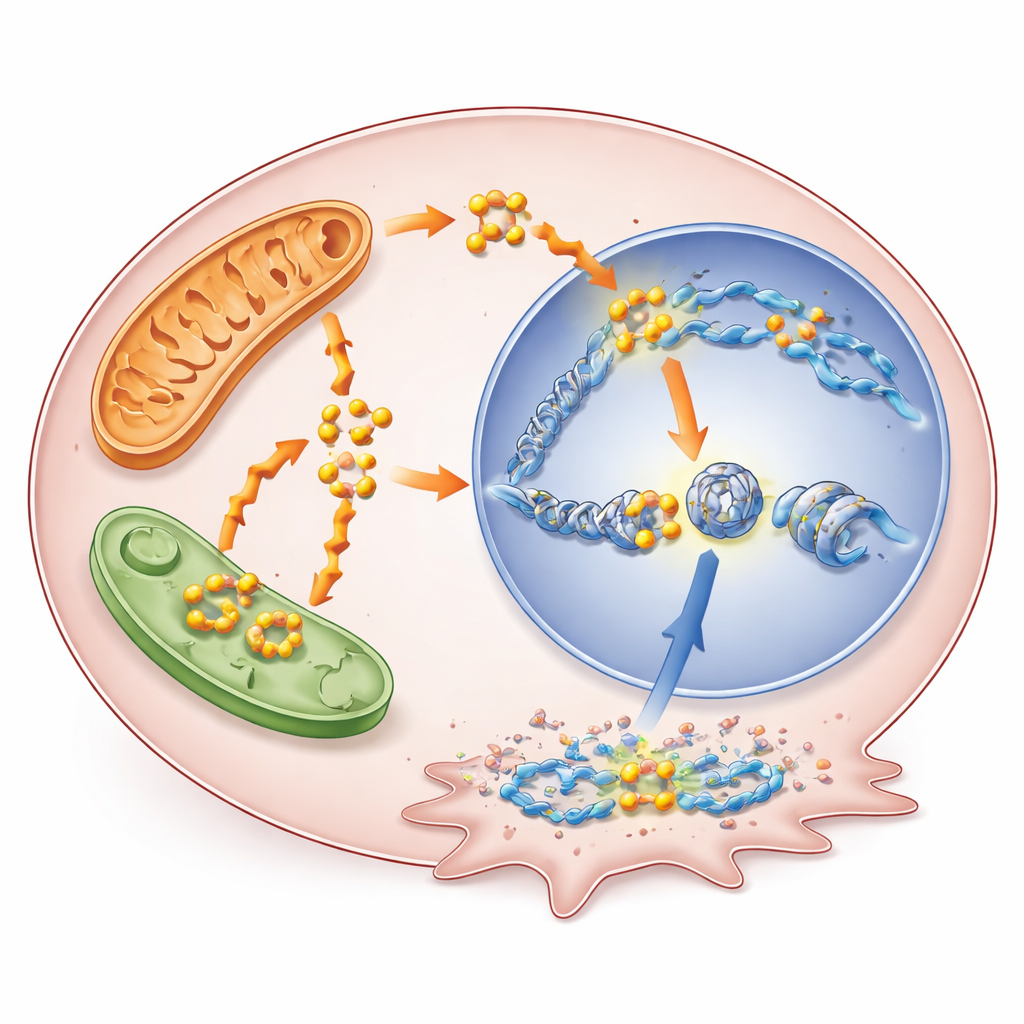
גן חדש שהודגש כגורם בעייתי
בין הגנים שהופעלו בדרך זו, אחד בשם RUNX1 בלט. RUNX1 הוא גורם שעתוק — חלבון בקרה גני — שהוצג בעבר כמעורב בעמידות לתרופות בסוגי סרטן אחרים, אך לא נחקר היטב בגידולי תריס. כאן, אזורי הבקרה שלו צברו אצטילציה מוגברת של H3K9 כשה-BRAF נחסם, ופעילותו עלתה במספר מודלים של סרטן התריס, כולל תאים שהפכו לעמידים כרוניים. רמות RUNX1 גבוהות בנתוני גידולים של מטופלים נקשרו למחלה מתקדמת יותר, ניצול קשרי קשריות לימפה ותוצאות גרועות יותר. כאשר המדענים הורידו את RUNX1 בתאי סרטן התריס, אותם תאים גדלו לאט יותר והיו פחות מסוגלים להתנועע ולפלוש, מה שמצביע על תפקיד ישיר בהפיכת הגידולים לאגרסיביים יותר.
שילוב טיפולים כדי לחסום את נתיב המילוט
מכיוון שחמצון חומצות שומן ו-RUNX1 שניהם נראו מסייעים לתאים לעמוד בפני עיכוב BRAF, החוקרים בדקו האם חסימת מסלולים אלה תוכל להגביר את עוצמתן של תרופות קיימות. בקווי תאים, צירוף חוסם חמצון שומנים עם חוסמי BRAF גרם למות תאי סרטן רב יותר מאשר כל אחת מהתרופות לבדה. בעכברים שנשאו שתלים של גידולים אנושיים של תריס, הקומבינציה הקטינה את הגידולים ביעילות רבה יותר מאשר עיכוב BRAF לבדו. אסטרטגיה דומה הגביר את השפעת צמד קליני של חוסמי BRAF ו-MEK באורגנואיד מיני-גידול שגודל מדגימה של מטופל. במקביל, מעכב מולקולרי קטן של RUNX1 הפך את תאי סרטן התריס לפגיעים יותר לטיפול ממוקד ב-BRAF, מה שמחזק את הרעיון שהציר המטבולי-אפיגנטי הזה ניתן למניפולציה תרופתית.
מה משמעות זה לטיפול בעתיד
עבור קוראים שאינם מומחים, המסר המרכזי הוא שמספר מקרי סרטן התריס שורדים טיפול ממוקד על ידי שינוי גם של בחירת הדלק שלהם וגם של הדרך שבה נקראת ה-DNA שלהם. על ידי שריפת יותר שומן, התאים מייצרים אות כימי שפותח גנים המקדמים הישרדות כמו RUNX1, ובעצם מסייע להם להסתגל לתרופות החוסמות BRAF. חיתוך השרשרת הזו — או על ידי חסימת פירוק חומצות שומן או על ידי דיכוי פעילות RUNX1 — מעלה את הסיכוי שהתאים הסרטניים ימותו במהלך הטיפול. בעוד שממצאים אלה עדיין פרה-קליניים, הם מציירים רציונל ברור לניסויים עתידיים שמשלבים תרופות ממוקדות במטבוליזם עם טיפולים מוכחים כדי לעכב או להתגבר על עמידות בסרטן התריס האגרסיבי.
ציטוט: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
מילות מפתח: סרטן התריס, עיכוב BRAF, חמצון חומצות שומן, רה-תכנות אפיגנטי, עמידות לתרופות