Clear Sky Science · sv
Oxidation av fettsyror driver acetyl-CoA-beroende omprogrammering av H3K9ac för att främja adaptiv resistens mot BRAFV600E-hämning vid tyreoideacancer
Varför detta är viktigt för personer med tyreoideacancer
Målinriktade läkemedel som riktar sig mot en vanlig mutation i tyreoideacancer, kallad BRAFV600E, har väckt förhoppningar hos patienter med aggressiv sjukdom. Många tumörer krymper först men kommer sedan tillbaka genom att hitta sätt att överleva trots behandling. Denna studie avslöjar en dold flyktväg inne i cancercellerna: en metabol omväg som omkopplar hur de bryter ner fett och styr genuttryck, vilket i slutändan dämpar effekten av BRAF-blockerande läkemedel. Att förstå denna väg kan peka ut nya kombinationsbehandlingar som förhindrar att cancern återkommer.
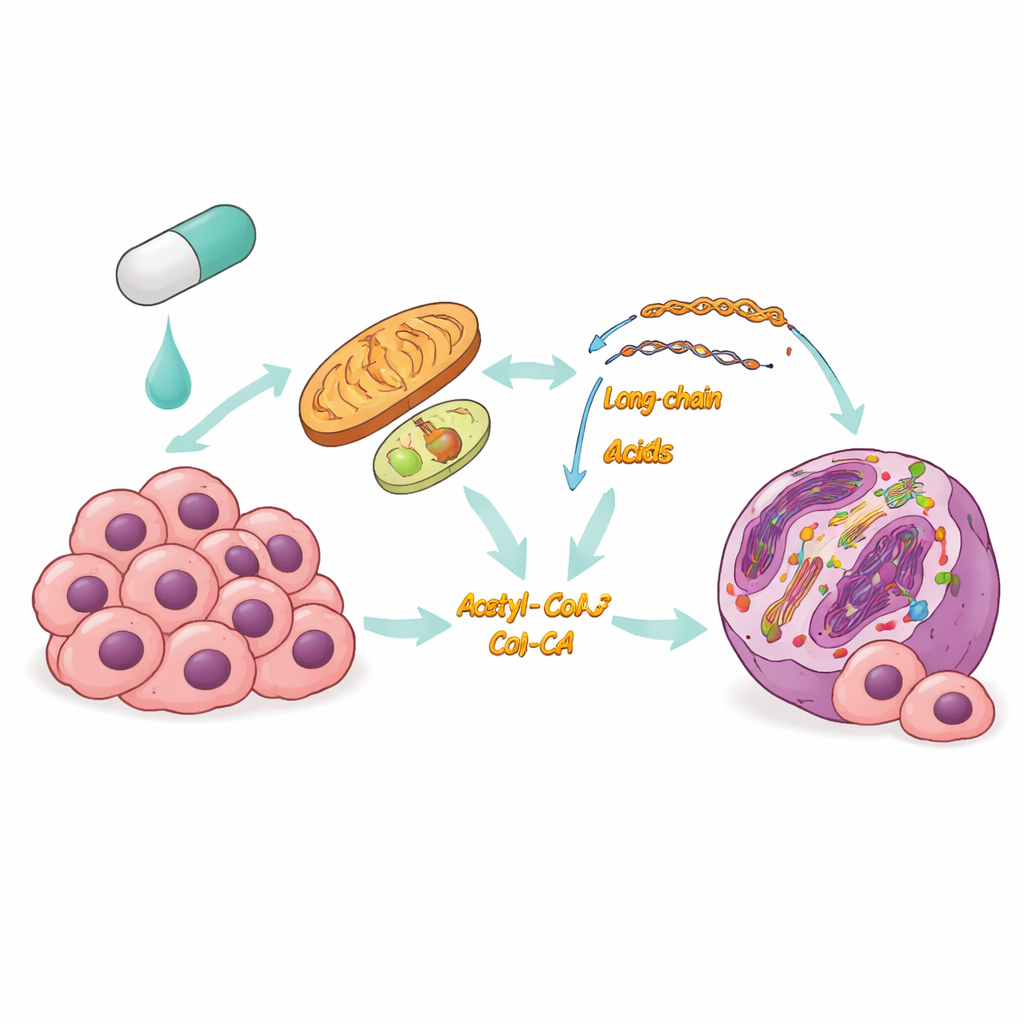
Problemet med nuvarande målinriktade behandlingar
Tyreoideacancer är den vanligaste cancerformen i de hormonproducerande körtlarna, och medan många fall växer långsamt kan vissa former sprida sig snabbt och vara svåra att behandla. I dessa aggressiva tumörer fungerar ofta BRAFV600E som en huvudströmbrytare som driver tillväxt, vilket gör BRAF-hämmande läkemedel till en attraktiv strategi. Patienter utvecklar dock ofta resistens: läkemedlen fungerar initialt men tappar sedan effektivitet när överlevande cancerceller anpassar sig. Forskare misstänkte att förändringar i hur cellerna hanterar näring och energi kunde ligga bakom denna anpassning, men detaljerna var oklara.
Cancerceller byter bränsle för att överleva
Forskarna använde en kombination av genaktivitetsprofilering och mätningar av metaboliter i tyreoideacancerceller exponerade för en BRAF-hämmare. De fann att medan glukosförbränningsvägar dämpades ökade cellerna kraftigt oxidationen av fettsyror—i praktiken en växling från att bränna glukos till att bränna fett i mitokondrier och relaterade kompartment. Nyckelenzymer som för in fetter i denna väg uppreglerades, lipiddroppar förbrukades och både syreförbrukning och energiproduktion ökade. Viktigt är att detta skifte inte var flyktigt: celler som utvecklat långvarig läkemedelsresistens hade fortsatt påslagen fettsyreoxidation, vilket tyder på att det är en kärnstrategi för överlevnad under BRAF-blockad.
En metabol signal som skriver om cellens instruktionsmanual
Att förbränna fett gör mer än att bara hålla igång energiförsörjningen. När fettsyror bryts ner bildas acetyl-CoA, en liten molekyl som också fungerar som byggsten för kemiska märken på DNA-paketerande proteiner kallade histoner. Forskarna visade att ökad fettsyreoxidation under BRAF-hämning ökade nivåerna av acetyl-CoA, vilket i sin tur ökade en specifik histonmodifikation känd som H3K9-acetylering. Denna modifiering luckrar upp den lokala DNA-strukturen och tenderar att aktivera närliggande gener. När teamet blockerade fettsyreoxidation med läkemedlet thioridazin föll acetyl-CoA och denna acetyleringsmarkör minskade; tillsats av en prekursor som återfyllde acetyl-CoA återställde den delvis. Genom kartläggning över genomet visade sig den förhöjda acetyleringen samla sig nära promotorer för gener involverade i överlevnad och terapiresistens.
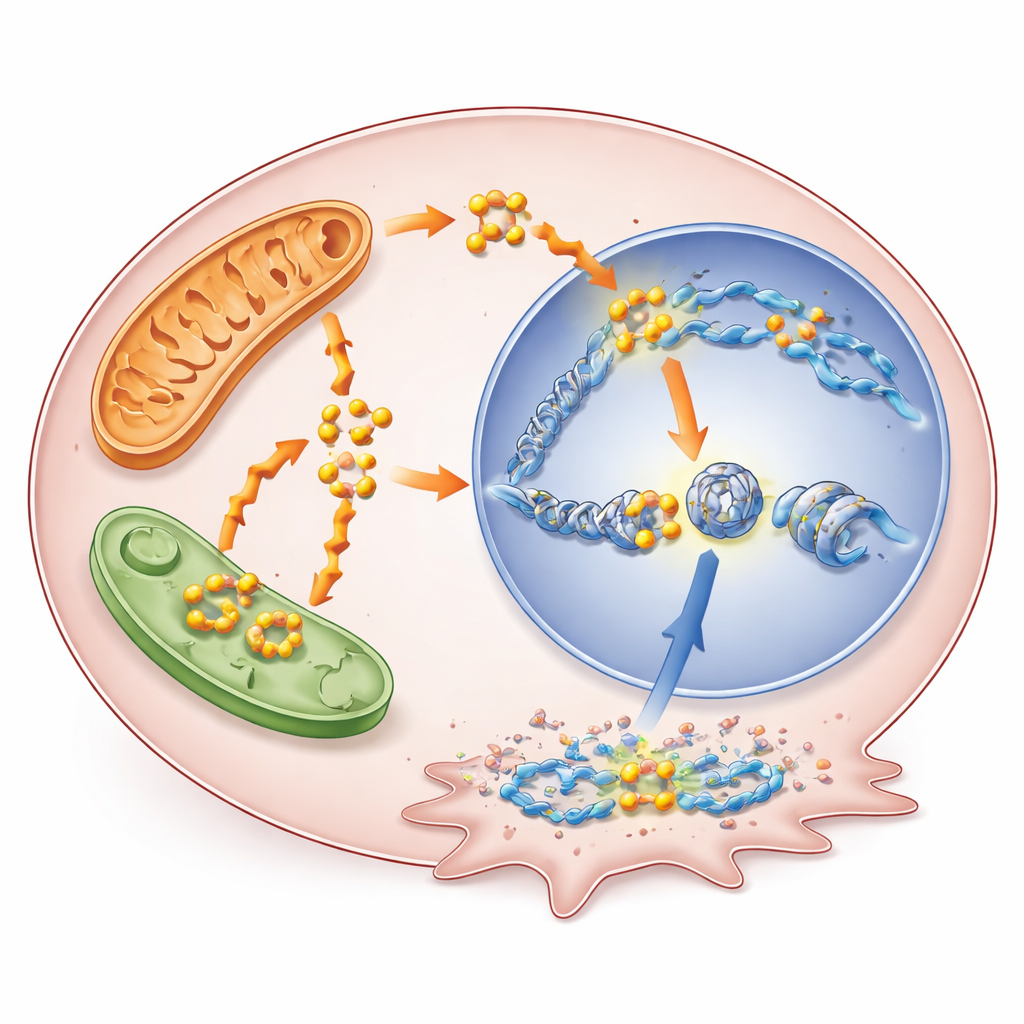
Ett nyupplyst problemmakargene
Bland de gener som aktiverades på detta sätt utmärkte sig en som heter RUNX1. RUNX1 är en transkriptionsfaktor—ett protein som styr genreglering—som tidigare kopplats till läkemedelsresistens i andra cancerformer, men som inte studerats väl i tyreoideatumörer. Här fick dess regulatoriska regioner ökad H3K9-acetylering när BRAF blockerades, och dess aktivitet steg i flera tyreoideacancermodeller, inklusive celler som blivit kroniskt resistenta. Höga RUNX1-nivåer i patientdata korrelerade med mer avancerad sjukdom, spridning till lymfkörtlar och sämre utfall. När forskarna sänkte RUNX1 i tyreoideacancerceller växte dessa celler långsammare och hade minskad förmåga att migrera och invadera, vilket pekar på en direkt roll i att göra tumörer mer aggressiva.
Kombinera behandlingar för att stänga flyktvägen
Där fettsyreoxidation och RUNX1 båda verkade hjälpa celler att stå emot BRAF-hämning testade forskarna om blockering av dessa vägar kunde öka effekten av befintliga läkemedel. I cellinjer utlöste kombinationen av en hämmare av fettsyreoxidation och BRAF-hämmare mer cancercellsdöd än något av läkemedlen ensamt. I möss med mänskliga tyreoideatumörtransplantat krympte kombinationen tumörer mer effektivt än enbart BRAF-hämning. En liknande strategi ökade effekten av en kliniskt använd kombination av BRAF- och MEK-hämmare i ett mini-tumororganoid framodlat från ett patientprov. Parallellt gjorde en småmolekylär hämmare av RUNX1 tyreoideacancerceller mer känsliga för BRAF-riktad terapi, vilket stärker idén att denna metabolisk-epigenetiska axel är terapeutiskt utnyttjbar.
Vad detta betyder för framtida vård
För icke-specialister är huvudbudskapet att vissa tyreoideacancerformer överlever målinriktad behandling genom att ändra både sitt bränsleval och hur deras DNA läses. Genom att förbränna mer fett skapar cellerna en kemisk signal som öppnar överlevnadsfrämjande gener som RUNX1, vilket hjälper dem anpassa sig till BRAF-blockerande läkemedel. Att avbryta denna kedja—antingen genom att blockera fettnedbrytning eller genom att dämpa RUNX1:s aktivitet—gör cancercellerna mer benägna att dö under behandling. Även om dessa fynd fortfarande är prekliniska ger de en tydlig motivering för framtida kliniska prövningar som kombinerar metabolisminriktade läkemedel med befintlig målinriktad terapi för att fördröja eller övervinna resistens i aggressiv tyreoideacancer.
Citering: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
Nyckelord: tyreoideacancer, BRAF-hämning, oxidation av fettsyror, epigenetisk omprogrammering, läkemedelsresistens