Clear Sky Science · pl
Utlenianie kwasów tłuszczowych napędza reprogramowanie zależne od acetyl-CoA markera H3K9ac, sprzyjając adaptacyjnej odporności na hamowanie BRAFV600E w raku tarczycy
Dlaczego to ma znaczenie dla osób z rakiem tarczycy
Leki celowane przeciwko powszechnemu w raku tarczycy temu o nazwie BRAFV600E wzbudziły nadzieję u pacjentów z agresywną postacią choroby. Jednak wiele guzów początkowo zmniejsza się, a potem nawraca, znajdując sposoby na przetrwanie mimo terapii. W tym badaniu odkryto ukrytą drogę ucieczki wewnątrz komórek nowotworowych: metaboliczne obejście, które przebudowuje sposób spalania tłuszczów i kontrolowania genów, co ostatecznie osłabia działanie leków blokujących BRAF. Zrozumienie tej ścieżki może wskazać nowe terapie łączone, które zapobiegną nawracaniu nowotworu.
Problem z obecnymi terapiami celowanymi
Rak tarczycy jest najczęstszym nowotworem gruczołów wydzielania wewnętrznego; choć wiele przypadków rośnie powoli, niektóre formy szybko się rozsiewają i są trudne do leczenia. W tych agresywnych guzach BRAFV600E często działa jak główny przełącznik napędzający wzrost, co czyni leki blokujące BRAF atrakcyjną strategią. Jednak pacjenci często rozwijają oporność: leki działają początkowo, a potem tracą skuteczność, gdy przetrwałe komórki nowotworowe adaptują się. Badacze podejrzewali, że zmiany w gospodarce składników odżywczych i energii mogą leżeć u podstaw tej adaptacji, ale szczegóły były niejasne.
Komórki nowotworowe zmieniają paliwo, by przetrwać
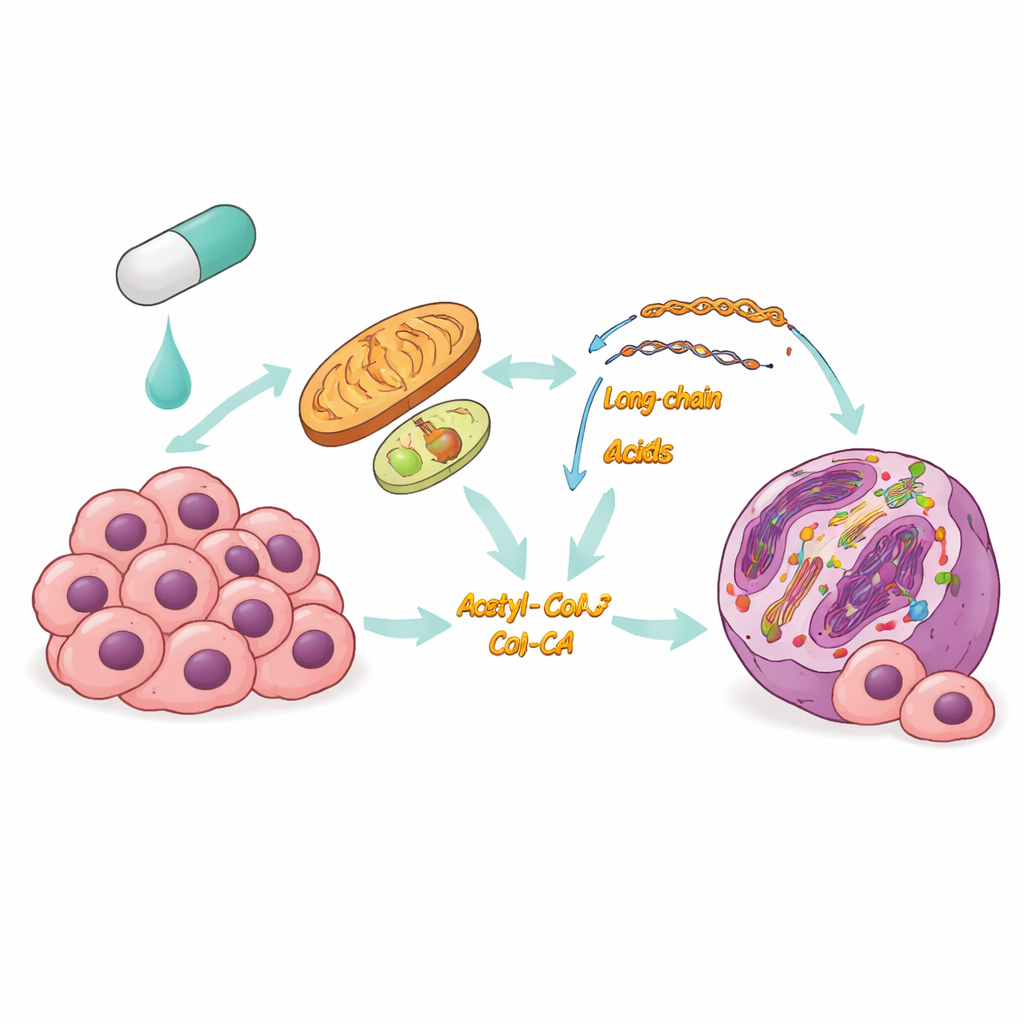
Zespół zastosował kombinację profilowania aktywności genów i pomiarów metabolitów w komórkach raka tarczycy eksponowanych na inhibitor BRAF. Stwierdzono, że podczas gdy szlaki spalania cukru były osłabione, komórki zdecydowanie zwiększyły utlenianie kwasów tłuszczowych — zasadniczo przełączając się ze spalania glukozy na spalanie tłuszczów w mitochondriach i powiązanych przedziałach. Kluczowe enzymy wprowadzające tłuszcze do tego szlaku nasiliły ekspresję, krople lipidowe zostały wykorzystane, a zarówno zużycie tlenu, jak i produkcja energii wzrosły. Co ważne, ta zmiana nie była przemijającym epizodem: komórki, które rozwinęły długoterminową oporność na lek, utrzymywały aktywne utlenianie kwasów tłuszczowych, co sugeruje, że jest to podstawowa strategia przetrwania podczas blokady BRAF.
Sygnal metaboliczny, który przepisuje instrukcję komórki
Spalanie tłuszczów robi więcej niż tylko podtrzymuje energetykę. Rozkład kwasów tłuszczowych generuje acetyl-CoA, małą cząsteczkę służącą także jako donor grupy do modyfikacji białek histonowych pakujących DNA. Badacze wykazali, że zwiększone utlenianie kwasów tłuszczowych podczas hamowania BRAF podnosi poziomy acetyl-CoA, co z kolei zwiększa konkretną modyfikację histonową znaną jako acetylacja H3K9. Ta modyfikacja rozluźnia lokalną strukturę chromatyny i zwykle aktywuje pobliskie geny. Kiedy zespół zablokował utlenianie kwasów tłuszczowych lekiem thioridazyną, acetyl-CoA spadł, a znacznik acetylacji zmalał; dodanie prekursora odtwarzającego zasoby acetyl-CoA częściowo przywróciło ten efekt. Mapowanie w skali genomu ujawniło, że zwiększona acetylacja koncentrowała się w pobliżu promotorów genów zaangażowanych w przetrwanie i oporność na terapię.
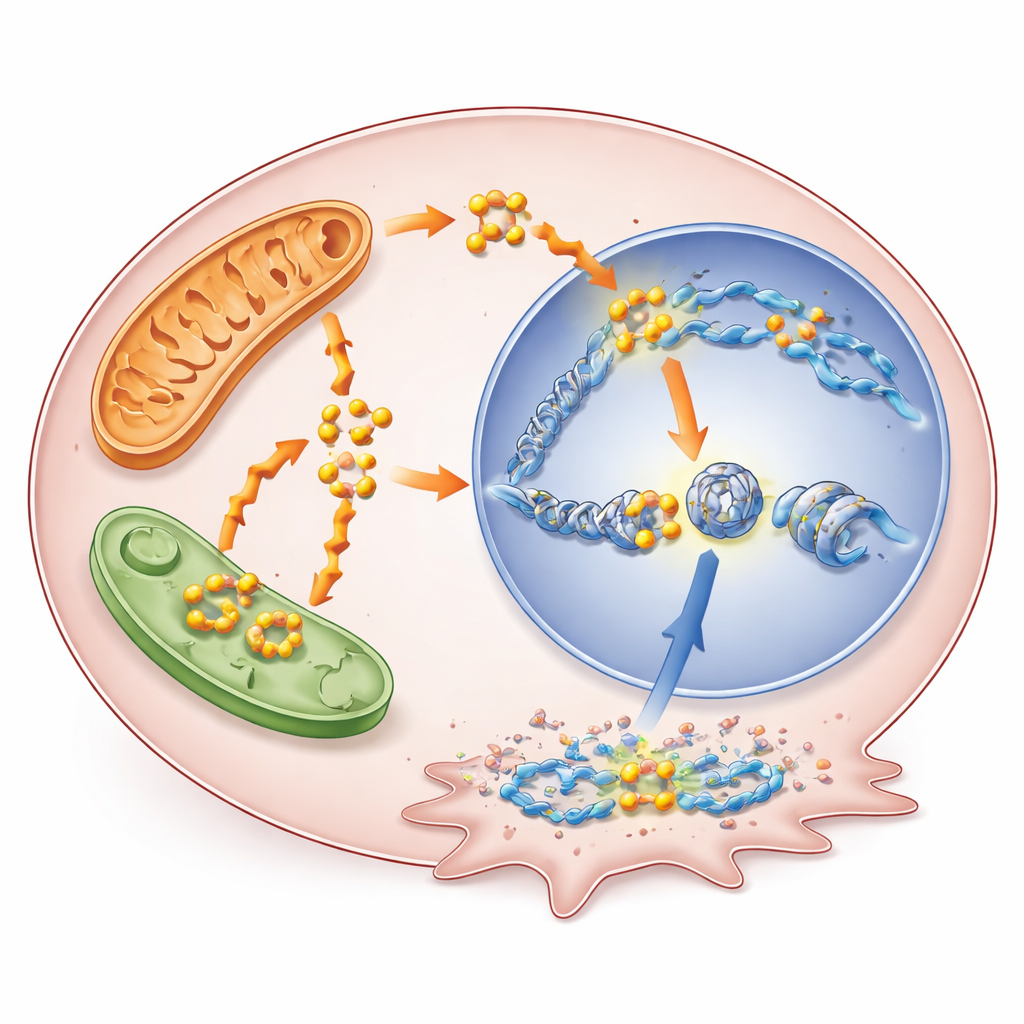
Nowo wskazany sprawca
Wśród genów włączonych w ten sposób wyróżniał się RUNX1. RUNX1 to czynnik transkrypcyjny — białko kontrolujące geny — wcześniej powiązane z opornością na leki w innych nowotworach, ale słabo zbadane w guzach tarczycy. W tym badaniu regiony regulacyjne RUNX1 zyskały dodatkową acetylację H3K9 po zablokowaniu BRAF, a jego aktywność wzrosła w wielu modelach raka tarczycy, w tym w komórkach chronically odpornych. Wyskie poziomy RUNX1 w danych pacjentów korelowały z bardziej zaawansowaną chorobą, zajęciem węzłów chłonnych i gorszymi wynikami. Gdy naukowcy zmniejszyli ekspresję RUNX1 w komórkach raka tarczycy, te komórki wolniej rosły i miały mniejszą zdolność migracji i inwazji, co wskazuje na bezpośrednią rolę w zwiększaniu agresywności guzów.
Łączenie terapii, by odciąć drogę ucieczki
Ponieważ zarówno utlenianie kwasów tłuszczowych, jak i RUNX1 wydawały się pomagać komórkom przetrwać blokadę BRAF, badacze sprawdzili, czy zahamowanie tych szlaków może zwiększyć skuteczność istniejących leków. W liniach komórkowych połączenie inhibitora utleniania kwasów tłuszczowych z inhibitorami BRAF wywołało więcej śmierci komórek nowotworowych niż którykolwiek z leków osobno. U myszy z implantami ludzkich guzów tarczycy kombinacja skuteczniej zmniejszała guzy niż samo hamowanie BRAF. Podobna strategia zwiększyła skuteczność klinicznie stosowanego zestawu inhibitorów BRAF i MEK w mini-guzie (organoidzie) wyhodowanym z próbki pacjenta. Równolegle, inhibitor małocząsteczkowy RUNX1 uczynił komórki raka tarczycy bardziej podatnymi na terapię ukierunkowaną na BRAF, co wzmacnia ideę, że ta oś metaboliczno‑epigenetyczna jest możliwa do wykorzystania terapeutycznego.
Co to oznacza dla przyszłej opieki
Dla czytelników niebędących specjalistami kluczowy przekaz jest taki: niektóre raki tarczycy przetrwają terapię celowaną, zmieniając zarówno wybór paliwa, jak i sposób odczytu DNA. Spalając więcej tłuszczu, komórki wytwarzają sygnał chemiczny, który otwiera geny sprzyjające przetrwaniu, takie jak RUNX1, pomagając im zaadaptować się do leków blokujących BRAF. Przerwanie tego łańcucha — przez blokadę rozkładu kwasów tłuszczowych lub stłumienie aktywności RUNX1 — zwiększa prawdopodobieństwo śmierci komórek nowotworowych podczas terapii. Choć wyniki są nadal przedkliniczne, przedstawiają jasne uzasadnienie dla przyszłych badań klinicznych łączących leki ukierunkowane na metabolizm z istniejącymi terapiami celowanymi, aby opóźnić lub pokonać oporność w agresywnym raku tarczycy.
Cytowanie: Wang, X., Zhang, J., Yuan, J. et al. Fatty acid oxidation drives acetyl-CoA-dependent H3K9ac reprogramming to promote adaptive resistance to BRAFV600E inhibition in thyroid cancer. Cell Death Dis 17, 329 (2026). https://doi.org/10.1038/s41419-026-08575-7
Słowa kluczowe: rak tarczycy, hamowanie BRAF, utlenianie kwasów tłuszczowych, reprogramowanie epigenetyczne, oporność na leki