Clear Sky Science · tr
Hızlı CAR taraması ve sürekli çözülenlere dirençli immünoterapi için sirküler RNA ile yönlendirilen CAR-NK hücreleri
Gelecekteki kanser tedavileri için bunun önemi
Birçok kişi, bağışıklık sistemini kansere saldıracak şekilde yeniden programlayan CAR‑T hücre terapilerinden haberdardır. Ancak bu tedaviler pankreas kanseri gibi zorlu katı tümörlere karşı zorluk yaşadı. Bu çalışma, tümörlerin tedaviden kaçmak için sık kullandıkları bir numaralı hilelerden biri—tedavi hedefini oluşturan yapıyı hücre yüzeyinden koparıp salma—karşısında bile işlevini sürdürebilen farklı bir bağışıklık hücresi türü olan doğal öldürücü (NK) hücrelerini mühendislik yoluyla güçlendirmenin yeni bir yolunu gösteriyor. Çalışma ayrıca bu tür hücre terapilerini daha hızlı tasarlanabilir ve üretimi daha kolay hale getirebilecek yeni bir RNA teknolojisini tanıtıyor.
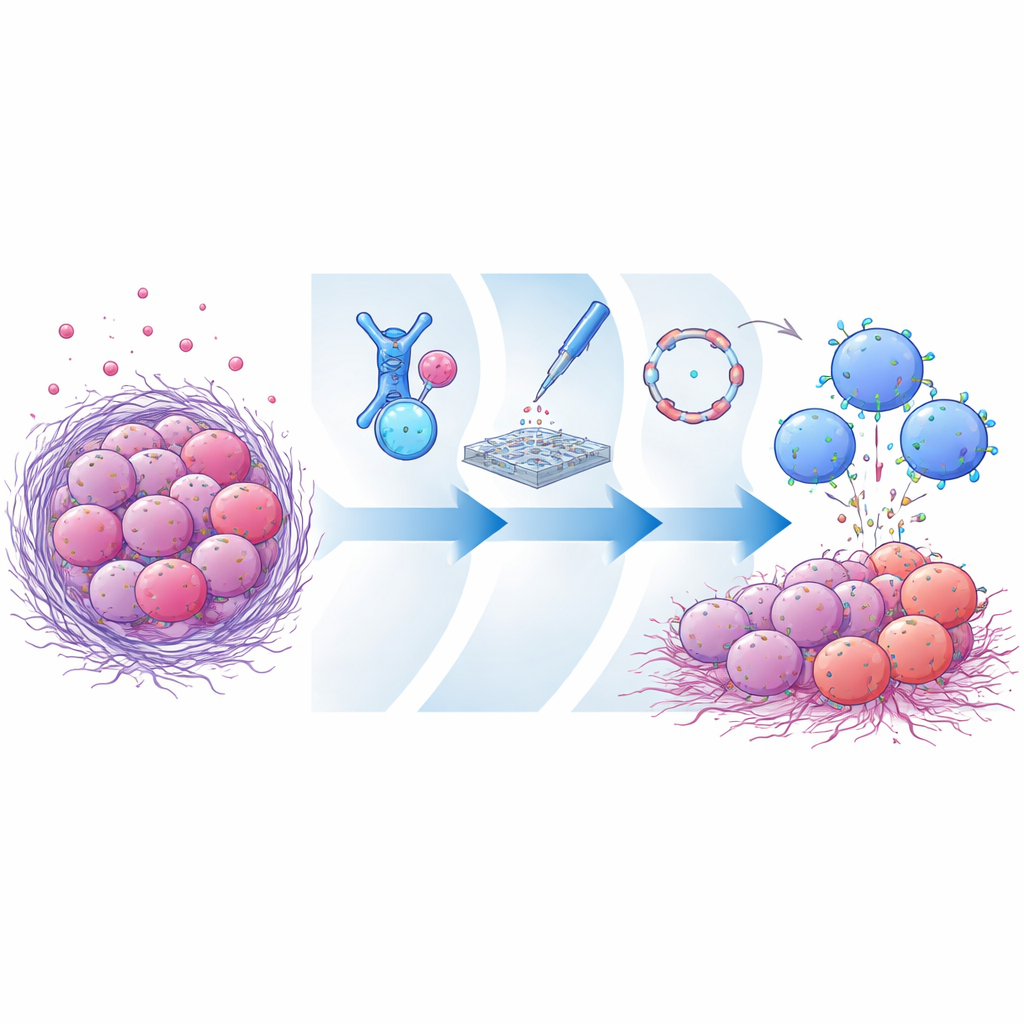
Tümörün kaybolan hedef numarası
Birçok agresif kanserde mesotelin adı verilen yüzey molekülü yüksek düzeyde bulunur. Sağlıklı dokularda çok daha az bulunduğundan, mesotelin deneysel ilaçlar ve hücre terapileri için popüler bir hedef olmuştur. Ancak tümörler mesotelinin dış kısmını kesip kana salarak bu molekülü koparabilir. Bu serbest parçalar, tedavi edici antikorları veya CAR reseptörlerini tümör hücüresi yüzeyine ulaşmadan önce oyalayan birer kandırmaca (dekoı) gibi davranır. Önceki terapiler çoğunlukla kolayca koparılan mesotelinin uzak bölgelerine bağlıydı, bu yüzden bu deko etkisine özellikle duyarlıydılar. Zorluk, koparma sonrası hücre yüzeyinde kalan bir bağlanma bölgesi bulmak ve aynı zamanda bağışıklık hücrelerinin tümörle sıkı, etkili bir temas kurmasına imkan vermektir.
Kanser hücresine daha iyi bir tutuş bulmak
Araştırmacılar ilk olarak mesotelin tanıyan çok büyük bir antikor fragmanı kütüphanesi oluşturdu ve bunları maya hücreleri üzerinde sergiledi. Birkaç seçim turu ile intakt, zarla bağlı mesotelin versiyonuna güçlü bağlanan ancak çözünmüş dökülmüş forma neredeyse bağlanmayan adaylar zenginleştirildi. Öne çıkan antikor fragmanlarından biri olan CLMS10, kesilme sonrası hücre zarına bağlı kalan mesotelin bölümüne—zarın hemen yakınına—tutunuyordu. Bilgisayar modellemeleri, bu pozisyonun kesim noktasının kendisiyle örtüştüğünü, böylece mesotelini serbest bırakan enzimleri fiziksel olarak engellediğini ya da en azından zarla bağlı formu tercih ettiğini öne sürdü. CLMS10 CAR tasarımlarına konulduğunda ve primer insan NK hücrelerinde test edildiğinde, bu hücreler mesotelin‑pozitif kanser hücrelerini etkili biçimde öldürdü ve birkaç karşılaştırma CAR’ının aksine yüksek düzeyde çözülebilir mesotelin varlığından büyük ölçüde etkilenmedi.
Doğrudan insan NK hücrelerinde hızlı test
Yavaş viral yöntemler veya vekil hücre hatları yerine ekip, insan donör NK hücrelerinde doğrudan mühendislik tarzı bir hızlı test platformu benimsedi. Farklı CAR tasarımlarını lineer haberci RNA (mRNA) olarak kodladılar ve bunları elektriksel geçirgenlik (elektroporasyon) ile teslim ederek NK hücrelerinin her aday reseptörü geçici olarak ifade etmesine izin verdiler. Bu, çeşitli antikor fragmanlarının, sinyalleme domainlerinin ve ek immün güçlendiricilerin gerçekçi NK hücrelerinde immortalize vekiller yerine nasıl performans gösterdiğini hızla karşılaştırmayı mümkün kıldı. Yan yana yapılan işlevsel testler yoluyla, CLMS10’u OX40 ve CD3ζ domainlerini içeren bir dahili sinyal modülüyle birleştirmenin tümör öldürmesini, NK hücre degranülasyonunu ve metabolik dayanıklılığı önemli ölçüde artırdığını buldular. Sitokin interlökin‑21’in eş zamanlı verilmesi performansı daha da keskinleştirerek NK hücrelerinin besin fakiri, baskılayıcı tümör benzeri koşullarda etkinliğini sürdürmesine yardımcı oldu.
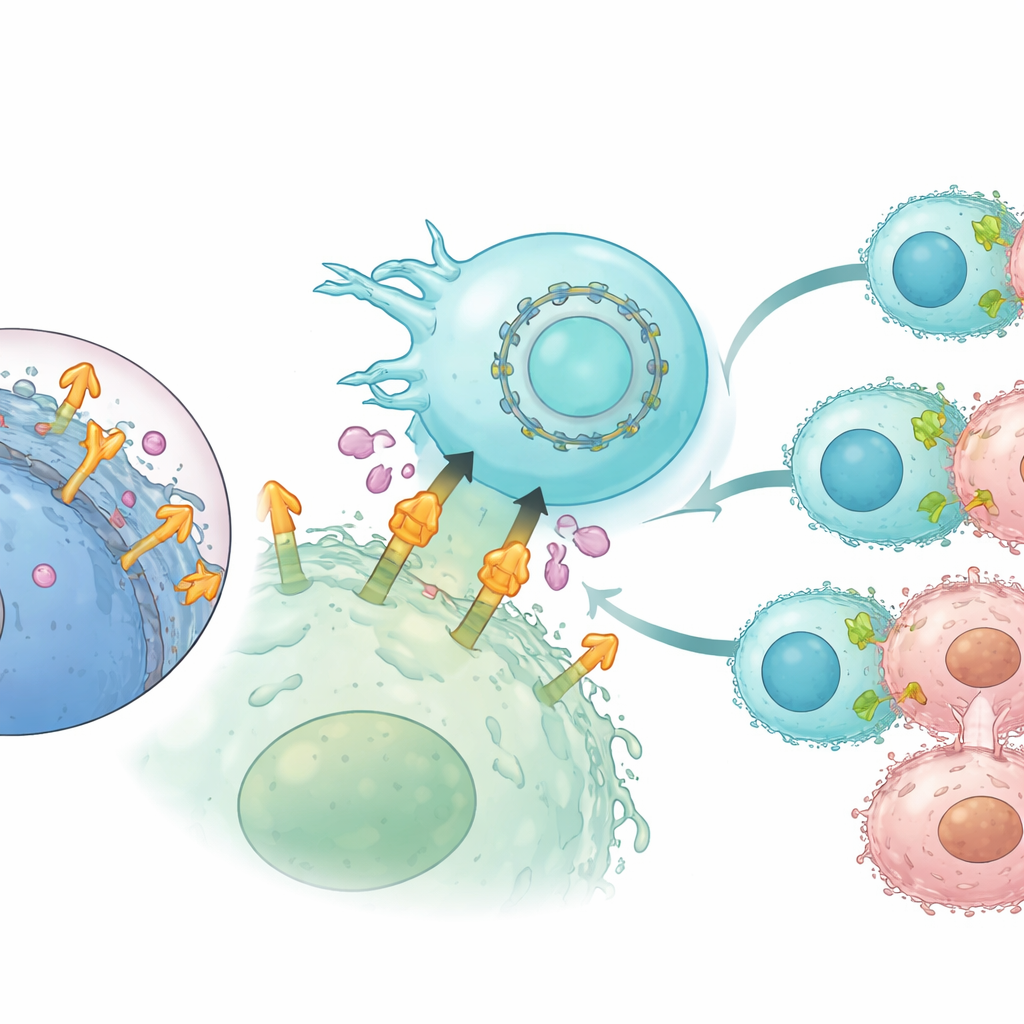
Sirküler RNA ile CAR ifadesini daha uzun süreli kılmak
Normal mRNA kısa ömürlü olduğundan, hücre terapilerinde kullanımı mühendislenmiş reseptörlerin hücre yüzeyinde kalma süresini sınırlayabilir. Bunu ele almak için yazarlar, bozulmaya doğal olarak daha dayanıklı kapalı halka biçimli bir RNA formatı olan dairesel RNA’ya yöneldi. CLMS10 tabanlı CAR’ı sirküler RNA olarak kodladılar ve interlökin‑21 RNA’sı ile birlikte NK hücrelerine aktardılar. Lineer mRNA ile karşılaştırıldığında, sirküler RNA birkaç gün boyunca daha dayanıklı CAR ekspresyonu sağladı ve hücre canlılığına zarar vermedi. Laboratuvarda tekrarlı tümör meydan okuma deneylerinde, sirküler RNA ile programlanmış NK hücreleri daha güçlü ve daha uzun süreli kanser hücresi öldürme sürdürdü, anahtar immün habercileri salgılamaya devam etti ve yüksek düzeyde dökülmüş mesotelin maruziyetinde bile etkili kaldı.
Zor bir tümör ortamında dökülmeye direnç kanıtlamak
Gerçek tümör ortamını taklit etmek için ekip, birçok katı tümörün etrafını saran ve mesotelin dökülmesini artırıp bağışıklık yanıtlarını bastırdığı bilinen kanser ilişkili fibroblastları kullandı. Pankreas kanseri hücreleri ile bu fibroblastların karışık kültürlerinde, standart mesotelin hedefli CAR‑NK hücreleri etkinliklerinin büyük kısmını kaybetti. Buna karşılık, CLMS10‑tabanlı sirküler RNA CAR‑NK hücreleri dökülmüş antijen artışına rağmen kanser hücrelerini öldürmeye devam etti. Fibroblastça zengin, mesotelin eksprese eden pankreas tümörü modeli taşıyan farelerde test edildiğinde, bu optimize CAR‑NK hücreleri, geleneksel lentivirüsle mühendislik yapılmış CAR‑NK hücreleri kadar tümörleri küçülttü ve hızlı, nonviral üretim için avantajları korudu. Hayvanlarda geçici interlökin‑21 desteğinden kaynaklanan belirgin bir toksisite belirtisine rastlanmadı.
Hastalar için anlamı
Bu araştırma, katı tümörlerin başlıca kaçış stratejilerinden birine dayanabilecek daha akıllı hücre terapileri oluşturmak için bir plan sunuyor. Mesotelinin hücre zarına yakın, stabil bir bölümünü yakalayan bir antikoru sirküler RNA platformuyla eşleştirerek, yazarlar NK hücrelerinde reseptörü daha uzun süre tutan dökülmeye dirençli, sürekli bir CAR‑NK ürünü yarattı ve bu ürün zorlu pankreas kanseri modellerinde iyi performans gösterdi. İnsan denemelerinden önce daha fazla çalışma gerekse de, yaklaşım zor tedavi edilen kanserler için raftaki (off‑the‑shelf) CAR‑NK terapilerinin tasarımını hızlandırabilir ve daha güvenilir, kalıcı immün tabanlı tedavilere giden bir yol sunabilir.
Atıf: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Anahtar kelimeler: CAR-NK hücre tedavisi, mesotelin dökülmesi, dairesel RNA, pankreas kanseri, antikor mühendisliği