Clear Sky Science · ja
迅速なCARスクリーニングと環状RNA駆動の持続的なシェッド耐性CAR-NK細胞による免疫療法
将来のがん治療にとって重要な理由
免疫系を再プログラムしてがんを攻撃させるCAR-T細胞療法を聞いたことがある人は多いでしょう。しかし、これらの治療は膵臓がんのような難治性の固形腫瘍に対して苦戦してきました。本研究は、別種の免疫細胞であるナチュラルキラー(NK)細胞を新たに設計する方法を示しており、腫瘍がしばしば用いる回避トリック――治療が認識すべき標的を切り離して失わせる(shed)こと――に対しても持続的に機能できることを示しています。また、こうした細胞療法の設計を迅速化し、製造を容易にする可能性を持つ新しいRNA技術も導入されています。
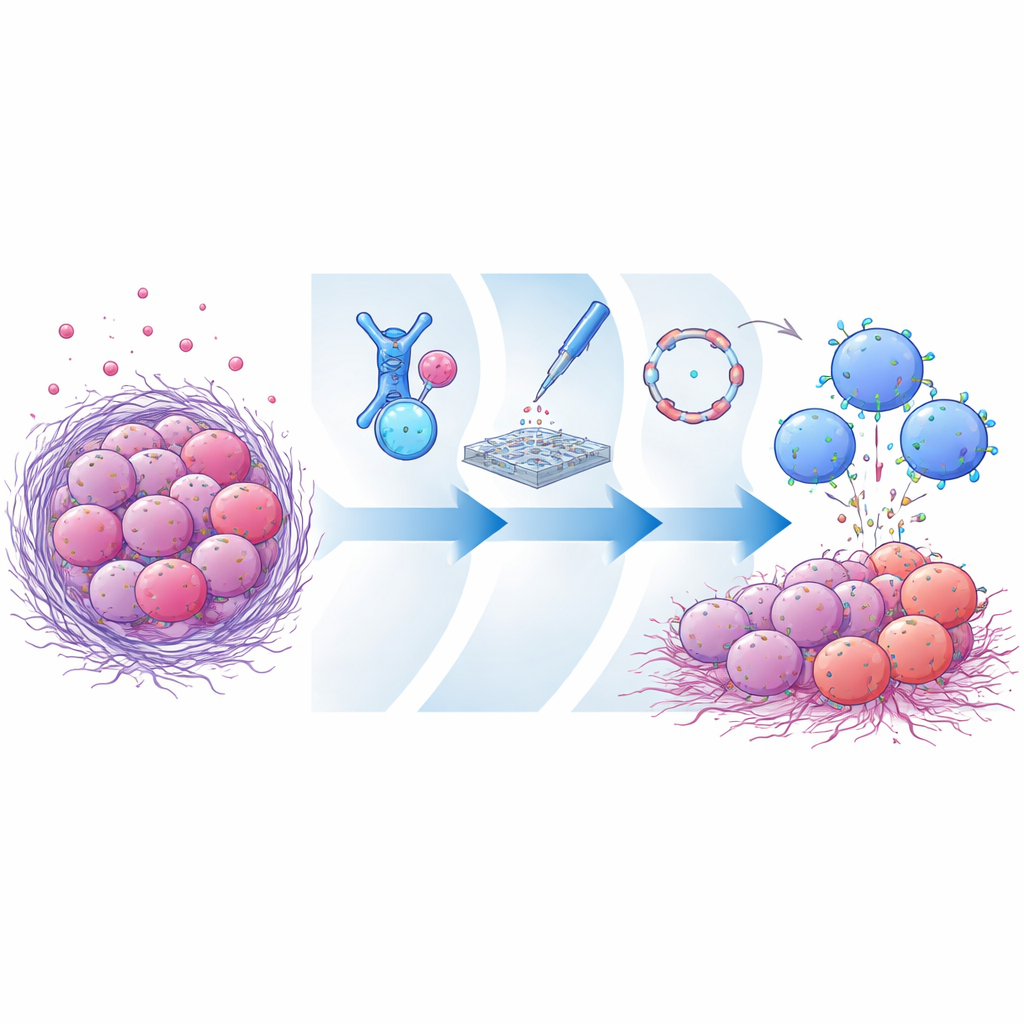
腫瘍が標的を消すトリック
多くの悪性腫瘍は細胞表面にメソセリンと呼ばれる分子を高発現しています。正常組織ではほとんど発現がないため、メソセリンは実験的薬剤や細胞療法の標的として人気がありました。しかし、腫瘍はメソセリンの外側部分を切り取って血流中に放出することができます。これらの遊離断片はデコイのように働き、治療用抗体やCAR受容体ががん細胞表面に到達する前に捕まってしまいます。従来の治療は切り離されやすい遠位領域に結合することが多く、このデコイ効果に特に弱点がありました。課題は、切断後も細胞膜上に残る結合部位を見つけつつ、免疫細胞が腫瘍と確実で効果的な接触を形成できるようにすることです。
がん細胞をより確実につかむために
研究者たちはまず、メソセリンを認識する抗体断片の巨大なライブラリを作成し、それらを酵母細胞上に表示しました。複数回の選別を通じて、膜に結合した(切断されていない)メソセリンには強く結合する一方で、可溶性の切断形にはほとんど結合しない候補を濃縮しました。その中で際立った抗体断片CLMS10は、切断後にも細胞膜に残るメソセリンの部分、非常に膜近傍に付着しました。コンピューターモデリングは、この位置が切断部位自体と重なり、メソセリンを切り離す酵素を物理的に妨げるか、少なくとも膜結合型を有利にすることを示唆しました。CLMS10をCAR設計に組み込み、ヒトの一次NK細胞で試験したところ、これらの細胞はメソセリン陽性のがん細胞を効率よく殺し、高レベルの可溶性メソセリンの存在下でもほとんど影響を受けませんでした。これはいくつかのベンチマークCARとは対照的です。
ヒトNK細胞での迅速な直接評価
遅いウイルス法や代替の細胞株を使う代わりに、チームはドナー由来ヒトNK細胞で直接行うエンジニアリング様式の迅速評価プラットフォームを採用しました。彼らは異なるCAR設計を線状メッセンジャーRNAとしてコード化し、エレクトロポレーションで導入して、NK細胞に各候補受容体を一過性に発現させました。これにより、不死化された代替細胞ではなく現実的なNK細胞内で、さまざまな抗体断片、シグナルドメイン、追加の免疫ブースターがどれほど機能するかを迅速に比較できました。これらの並列機能試験を通じて、CLMS10をOX40とCD3ζドメインを含む内在性シグナルモジュールと組み合わせると、腫瘍殺傷、NK細胞の顆粒放出、代謝的な健全性が著しく向上することが分かりました。さらにサイトカインのインターロイキン21を共導入すると、栄養が乏しく抑制的な腫瘍様環境下でもNK細胞が活動を維持するのに役立ちました。
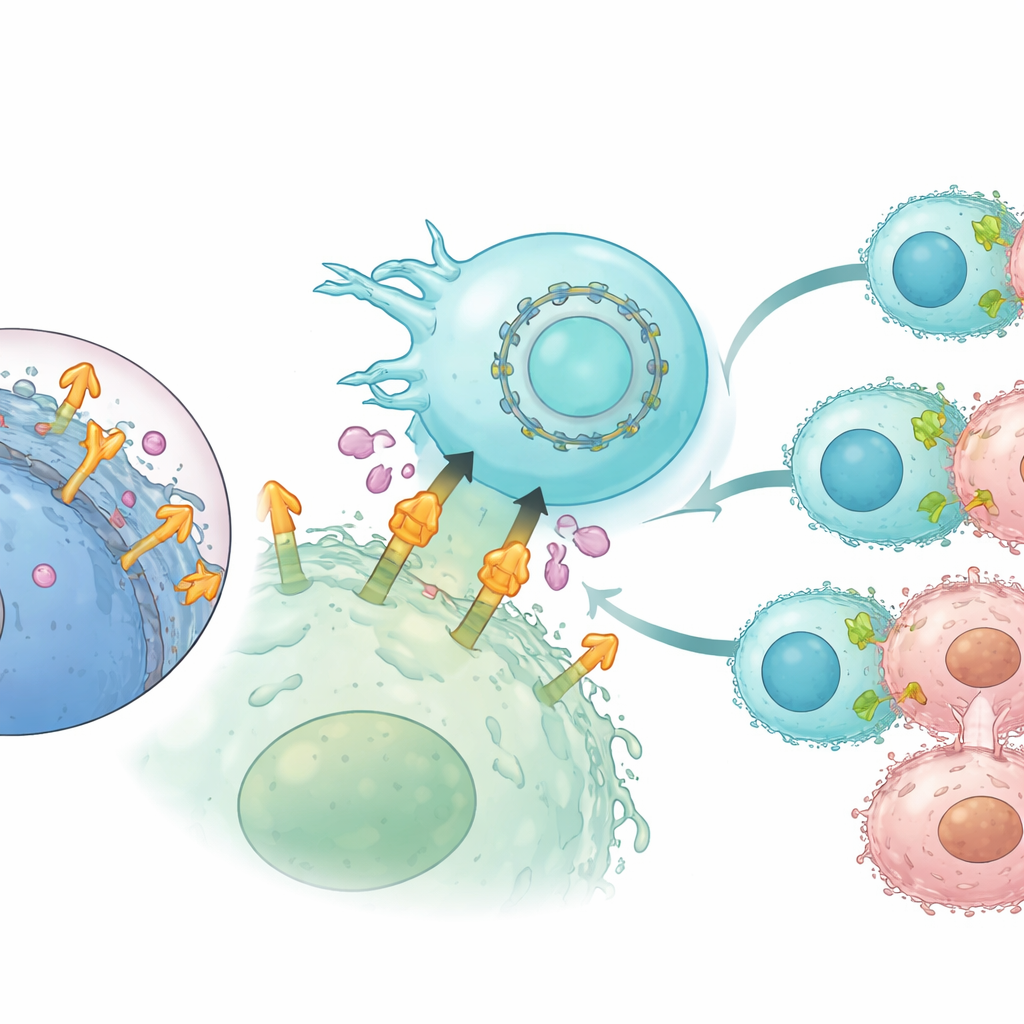
環状RNAでCAR発現を長持ちさせる
通常のmRNAは寿命が短いため、細胞療法における改変受容体の表面発現期間を制限します。これに対処するために著者らは環状RNA(閉ループ構造で分解に強い形式)に目を向けました。CLMS10ベースのCARを環状RNAでコード化し、インターロイキン21のRNAとともにNK細胞に導入しました。線状mRNAと比較して、環状RNAは数日にわたりより持続的なCAR発現を促し、細胞生存率を損なうことはありませんでした。ラボ内での繰り返し腫瘍チャレンジ実験では、環状RNAでプログラムしたNK細胞はより強力で長続きするがん細胞殺傷を維持し、重要な免疫分子の分泌を続け、高レベルの切り離されたメソセリンに曝露されても有効性を保ちました。
厳しい腫瘍環境でのシェッド耐性の証明
実際の腫瘍環境を模倣するために、チームはがんに伴う線維芽細胞(多くの固形腫瘍を取り囲み、メソセリンの切断を亢進し免疫応答を抑えることで知られる支持細胞)を用いました。膵臓がん細胞とこれらの線維芽細胞を混合した共培養では、標準的なメソセリン標的CAR-NK細胞の効力は大きく低下しました。対照的に、CLMS10ベースの環状RNA CAR-NK細胞は増加した遊離抗原にもかかわらずがん細胞の殺傷を維持しました。線維芽細胞が豊富でメソセリン発現のある膵臓腫瘍モデルを移植したマウスで試験したところ、最適化されたこれらのCAR-NK細胞は従来のレンチウイルスで設計されたCAR-NK細胞と同等に腫瘍を縮小させつつ、迅速かつ非ウイルス的な製造の利点を保持しました。動物には一時的なインターロイキン21の増強による明らかな毒性は見られませんでした。
患者にとっての意義
本研究は、固形腫瘍の主要な回避戦略の一つに耐えうるスマートな細胞療法を構築するための設計図を示しています。膜近傍で安定しているメソセリンの部分をつかむ抗体と、受容体をNK細胞上に長く維持する環状RNAプラットフォームを組み合わせることで、著者らはシェッドに強く持続性のあるCAR-NK製品を作り上げ、厳しい膵臓がんモデルで良好な性能を示しました。人での試験に至る前にさらに検討が必要ですが、このアプローチは難治がんに対する既製(off-the-shelf)CAR-NK療法の設計を加速し、より信頼性が高く持続的な免疫療法への道を開く可能性があります。
引用: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
キーワード: CAR-NK細胞療法, メソセリンの切断(shed), 環状RNA, 膵臓がん, 抗体エンジニアリング