Clear Sky Science · pl
Szybkie przesiewanie CAR i komórki CAR-NK napędzane circRNA dla trwałej immunoterapii odpornej na odcinanie antygenu
Dlaczego to ma znaczenie dla przyszłych terapii przeciwnowotworowych
Wiele osób słyszało o terapiach CAR‑T, które przeprogramowują układ odpornościowy do rozpoznawania i eliminowania nowotworów. Jednak te terapie mają trudności z twardymi guzami litymi, takimi jak rak trzustki. Badanie pokazuje nowy sposób zaprojektowania innego typu komórek odpornościowych — komórek NK (natural killers), aby mogły działać nawet wtedy, gdy guzy stosują jedną ze swoich sztuczek unikania ataku: odcinanie samego celu, który terapia ma rozpoznawać. Praca wprowadza też nową technologię RNA, która może przyspieszyć projektowanie takich terapii komórkowych i ułatwić ich produkcję.
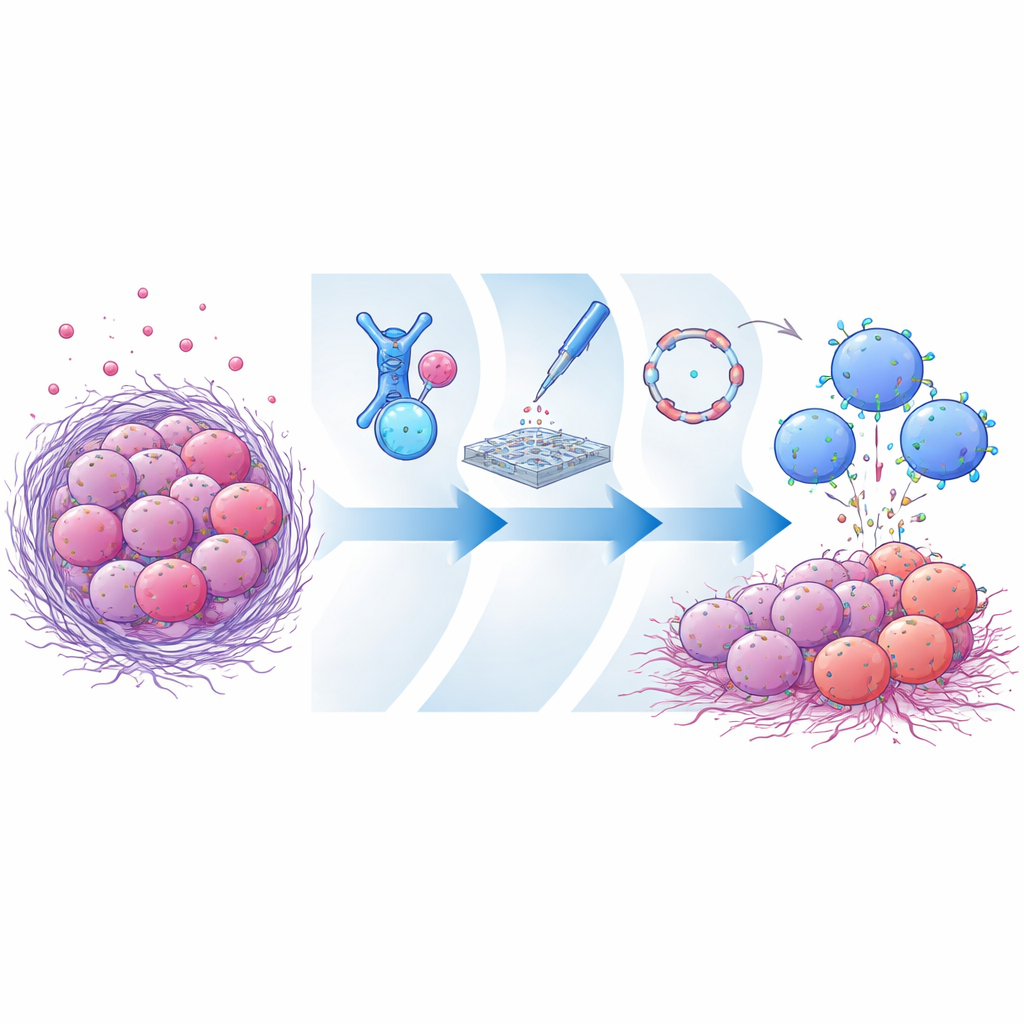
Sztuczka znikającego celu guza
Wiele agresywnych nowotworów ma wysokie poziomy cząsteczki powierzchniowej zwanej mesoteliną. Ponieważ tkanki zdrowe mają jej znacznie mniej, mesotelina stała się atrakcyjnym celem dla eksperymentalnych leków i terapii komórkowych. Guzy potrafią jednak odcinać zewnętrzną część mesoteliny i uwalniać ją do krwiobiegu. Te wolne fragmenty działają jak wabiki, wychwytując terapeutyczne przeciwciała lub receptory CAR, zanim dotrą do powierzchni komórki nowotworowej. Wcześniejsze terapie przeważnie wiązały odległe regiony mesoteliny, które łatwo ulegają odcinaniu, co czyniło je szczególnie podatnymi na efekt wabika. Wyzwaniem jest znalezienie miejsca wiążącego, które pozostaje na powierzchni komórki po odcięciu, a jednocześnie umożliwia komórkom odpornościowym nawiązanie zwartego, skutecznego kontaktu z guzem.
Znalezienie lepszego uchwytu na komórce nowotworowej
Naukowcy najpierw stworzyli ogromną bibliotekę fragmentów przeciwciał rozpoznających mesotelinę i wyeksponowali je na komórkach drożdżowych. Poprzez kilka rund selekcji wzbogacili kandydatów, które mocno wiążą natywną, błonowo zakotwiczoną wersję mesoteliny, a niemal wcale jej rozpuszczalną, odcinaną formę. Jeden wyróżniający się fragment przeciwciała, nazwany CLMS10, przyłączał się w pobliżu części mesoteliny, która pozostaje zakotwiczona po przecięciu — bardzo blisko błony komórkowej. Modelowanie komputerowe sugerowało, że to położenie pokrywa się z samym miejscem cięcia, fizycznie blokując enzymy odcinające mesotelinę lub przynajmniej faworyzując formę związana z błoną. Gdy CLMS10 wbudowano w konstrukcje CAR i przetestowano w pierwotnych ludzkich komórkach NK, komórki te efektywnie zabijały komórki nowotworowe z ekspresją mesoteliny i były w dużej mierze niewrażliwe na wysokie poziomy rozpuszczalnej mesoteliny, w przeciwieństwie do kilku referencyjnych CAR‑ów.
Szybkie testy bezpośrednio w ludzkich komórkach NK
Zamiast polegać na wolnych metodach wirusowych lub zastępczych liniach komórkowych, zespół zastosował platformę szybkiego testowania w stylu inżynieryjnym bezpośrednio w ludzkich komórkach NK od dawców. Zakodowali różne projekty CAR jako liniowe mRNA i dostarczyli je metodą elektroporacji, co pozwoliło komórkom NK przejściowo ekspresjonować każdy kandydacki receptor. Umożliwiło to szybkie porównanie, jak różne fragmenty przeciwciał, domeny sygnalizacyjne i dodatkowe wzmacniacze immunologiczne działają w realistycznych komórkach NK, a nie w unieśmiertelnionych substytutach. Dzięki tym równoległym testom funkcjonalnym stwierdzili, że połączenie CLMS10 z wewnętrznym modułem sygnałowym zawierającym domeny OX40 i CD3ζ znacznie zwiększało zabijanie guza, degranulację komórek NK i ich kondycję metaboliczną. Wspólne dostarczenie cytokiny interleukiny‑21 dodatkowo poprawiło wydajność, pomagając komórkom NK utrzymać aktywność w warunkach ubogich w składniki odżywcze i tłumiących, przypominających mikrośrodowisko guza.
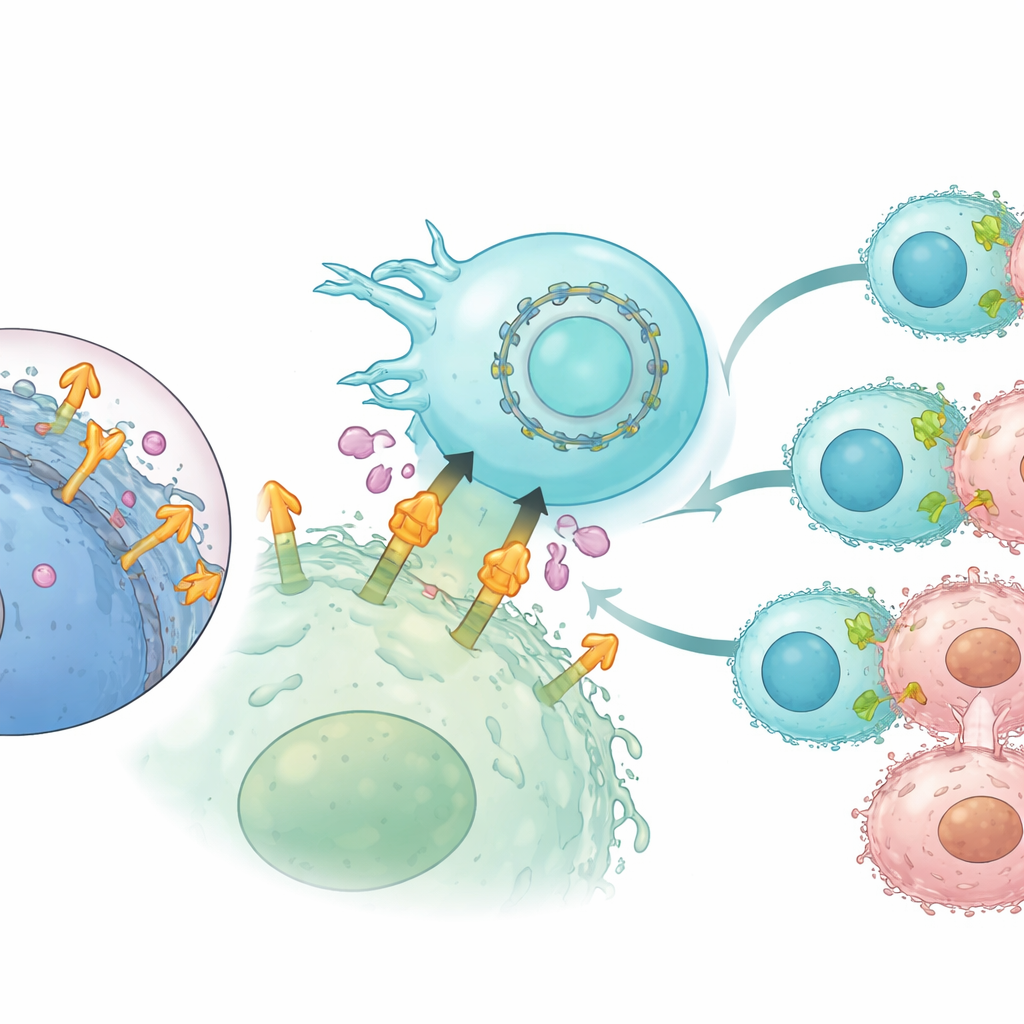
Wydłużenie ekspresji CAR dzięki RNA kolistemu
Ponieważ zwykłe mRNA jest krótkotrwałe, jego użycie w terapiach komórkowych może ograniczać czas obecności zaprojektowanych receptorów na powierzchni komórek. Aby temu zaradzić, autorzy sięgnęli po RNA koliste (circRNA), zamkniętą pętlę RNA naturalnie odporną na degradację. Zakodowali CAR oparty na CLMS10 w circRNA i wprowadzili go do komórek NK, ponownie razem z RNA interleukiny‑21. W porównaniu z liniowym mRNA, circRNA napędzało trwalszą ekspresję CAR przez kilka dni bez uszczerbku dla witalności komórek. W powtarzanych eksperymentach z wyzwaniem nowotworowym in vitro, komórki NK zaprogramowane circRNA zachowały silniejsze i dłużej trwające zabijanie komórek nowotworowych, nadal wydzielały kluczowe mediatory immunologiczne i pozostawały skuteczne nawet w obecności wysokich poziomów odciętej mesoteliny.
Udowodnienie odporności na odcinanie w trudnym środowisku guza
Aby odwzorować rzeczywiste warunki guza, zespół użył fibroblastów związanych z rakiem — komórek wspierających, które otaczają wiele guzów litych i są znane ze zwiększania odcinania mesoteliny oraz tłumienia odpowiedzi immunologicznej. W mieszaninach hodowlanych komórek raka trzustki i tych fibroblastów standardowe CAR‑NK skierowane przeciw mesotelinie traciły dużą część swojej siły. W przeciwieństwie do tego, komórki CAR‑NK oparte na CLMS10 i utrzymane przez circRNA nadal zabijały komórki nowotworowe mimo wzrostu stężenia odciętego antygenu. Testy na myszach z guzem trzustki bogatym w fibroblasty i ekspresyjnym dla mesoteliny wykazały, że zoptymalizowane komórki CAR‑NK zmniejszały guzy równie skutecznie jak tradycyjnie konstruowane komórki CAR‑NK wytworzone za pomocą lentivirusów, zachowując przy tym zalety szybkiej, niewirusowej produkcji. U zwierząt nie zaobserwowano wyraźnych oznak toksyczności związanej z tymczasowym wzmocnieniem interleukiną‑21.
Co to oznacza dla pacjentów
Badanie przedstawia wzorzec budowy „mądrzejszych” terapii komórkowych, które potrafią wytrzymać jedną z kluczowych strategii ucieczkowych guzów litych. Poprzez sparowanie przeciwciała chwytającego stabilny, błonie bliski fragment mesoteliny z platformą circRNA, utrzymującą receptor na komórkach NK dłużej, autorzy stworzyli produkt CAR‑NK odporny na odcinanie i długotrwały, który dobrze sprawdza się w wymagających modelach raka trzustki. Chociaż potrzebne są dalsze badania przed próbami u ludzi, podejście może przyspieszyć projektowanie gotowych do użycia terapii CAR‑NK przeciw trudnym do leczenia nowotworom, torując drogę do bardziej niezawodnych i trwalszych terapii immunologicznych.
Cytowanie: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Słowa kluczowe: terapia komórkami CAR‑NK, odcinanie mesoteliny, RNA koliste (circRNA), rak trzustki, inżynieria przeciwciał