Clear Sky Science · it
Screening rapido dei CAR e cellule CAR-NK guidate da circRNA per un’immunoterapia persistente resistente al shedding
Perché questo è importante per le terapie oncologiche future
Molti hanno sentito parlare delle terapie CAR-T che riprogrammano il sistema immunitario per cercare i tumori. Tuttavia, questi trattamenti hanno faticato contro tumori solidi ostici come il cancro del pancreas. Questo studio mostra un nuovo modo per ingegnerizzare un diverso tipo di cellula immunitaria — le cellule natural killer (NK) — così da conservarne l’efficacia anche quando i tumori usano uno dei loro trucchi preferiti per eludere l’attacco: il rilascio del bersaglio che la terapia dovrebbe riconoscere. Il lavoro introduce inoltre una nuova tecnologia RNA che potrebbe rendere queste terapie cellulari più rapide da progettare e più semplici da produrre.
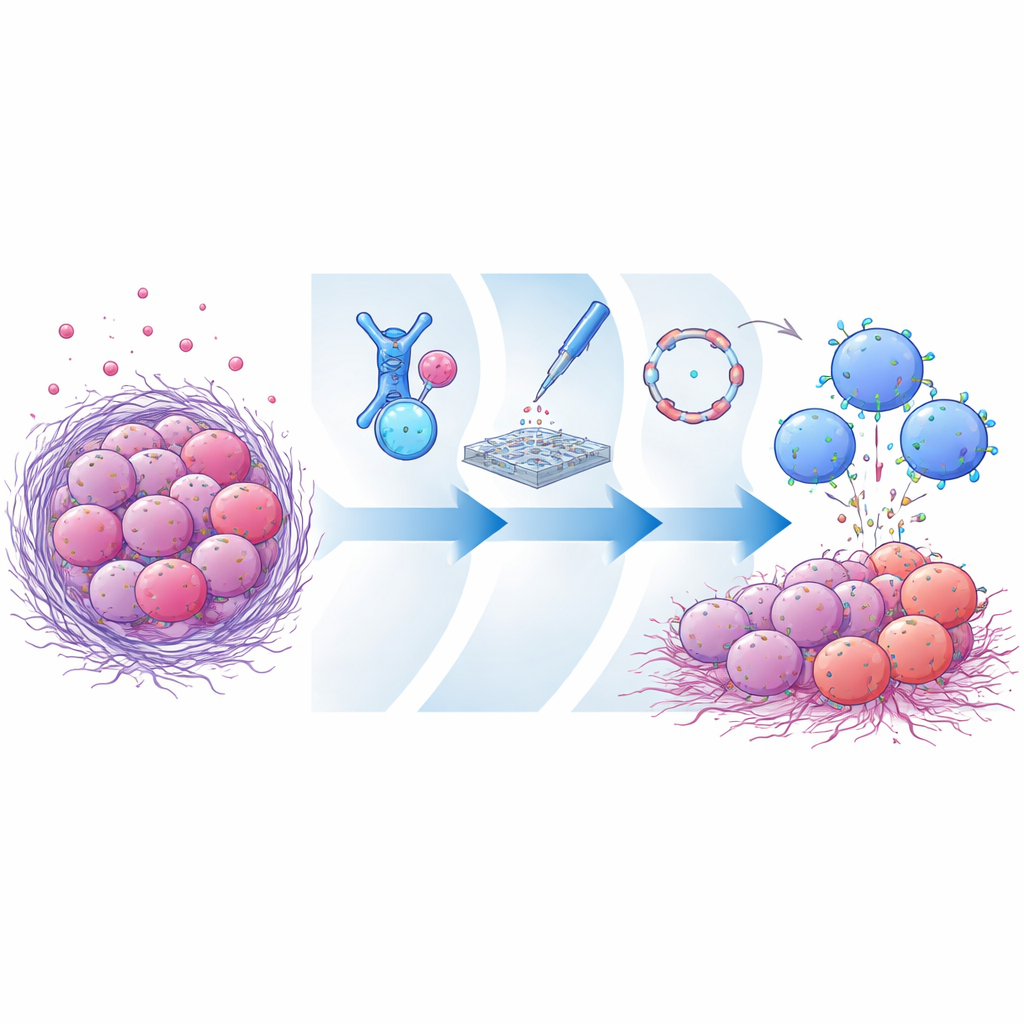
Il trucco del tumore: far scomparire il bersaglio
Molti tumori aggressivi esprimono alti livelli di una molecola di superficie chiamata mesotelina. Poiché i tessuti sani la esprimono molto meno, la mesotelina è stata un bersaglio popolare per farmaci sperimentali e terapie cellulari. Tuttavia, i tumori possono tagliare la porzione esterna della mesotelina e rilasciarla nel flusso sanguigno. Questi frammenti liberi funzionano come esche, assorbendo anticorpi terapeutici o recettori CAR prima che raggiungano la superficie della cellula tumorale. Le terapie precedenti si legavano per lo più a regioni distali della mesotelina facilmente sheddate, rendendole particolarmente vulnerabili a questo effetto esca. La sfida è trovare un sito di legame che rimanga sulla superficie cellulare dopo il taglio, pur consentendo alle cellule immunitarie di stabilire un contatto stretto ed efficace con il tumore.
Trovare una presa migliore sulla cellula tumorale
I ricercatori hanno prima creato una vastissima libreria di frammenti di anticorpi che riconoscono la mesotelina e li hanno espressi su cellule di lievito. Attraverso diverse fasi di selezione, hanno arricchito candidati che si legavano fortemente alla versione intatta e ancorata alla membrana della mesotelina ma poco alla sua forma solubile rilasciata. Un frammento anticorpale di spicco, chiamato CLMS10, si legava vicino alla porzione di mesotelina che resta ancorata dopo il clivaggio — molto vicino alla membrana cellulare. La modellazione al computer suggeriva che questa posizione sovrappone il sito di taglio, bloccando fisicamente gli enzimi che recidono la mesotelina o, almeno, favorendo la forma legata alla membrana. Quando CLMS10 è stato inserito in progettazioni CAR e testato in cellule NK umane primarie, queste uccidevano efficacemente cellule tumorali positive per mesotelina e risultavano per lo più non influenzate da alti livelli di mesotelina solubile, a differenza di diversi CAR di riferimento.
Test rapidi direttamente nelle cellule NK umane
Invece di usare metodi virali lenti o linee cellulari surrogate, il team ha adottato una piattaforma di test rapidi in stile ingegneristico direttamente nelle cellule NK di donatori umani. Hanno codificato diversi disegni di CAR come RNA messaggeri lineari e li hanno consegnati tramite elettroporazione, consentendo alle NK di esprimere temporaneamente ogni recettore candidato. Questo ha reso possibile confrontare rapidamente quanto funzionassero diversi frammenti anticorpali, domini di segnalazione e potenziatori immunitari in NK realistiche, anziché in surrogati immortalizzati. Attraverso questi test funzionali comparativi hanno scoperto che combinare CLMS10 con un modulo di segnalazione interno contenente i domini OX40 e CD3ζ aumentava significativamente la capacità citotossica, la degranulazione delle NK e la loro efficienza metabolica. La co-somministrazione della citochina interleuchina-21 ha ulteriormente migliorato le prestazioni, aiutando le NK a sostenere la loro attività in condizioni tumorali suppressive e povere di nutrienti.
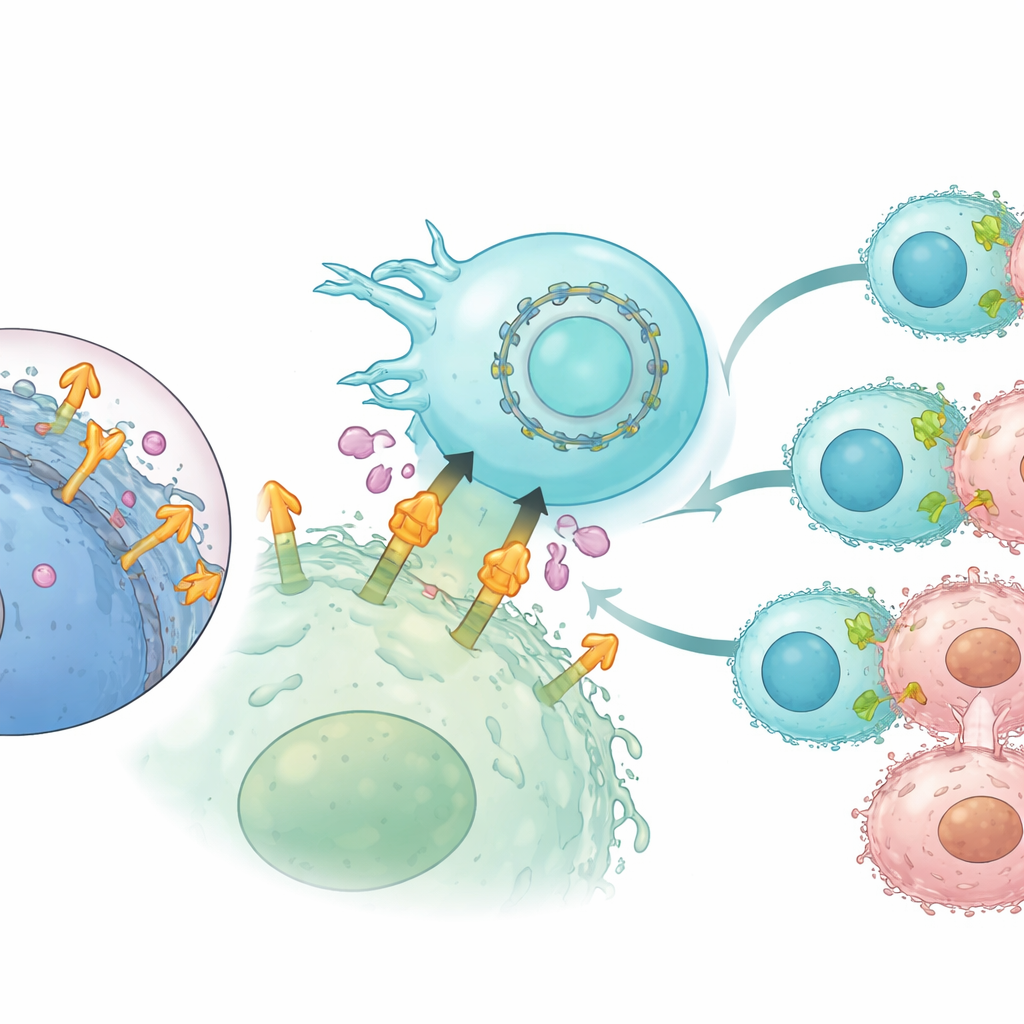
Rendere l’espressione del CAR più duratura con l’RNA circolare
Poiché l’RNA messaggero lineare è di breve durata, il suo uso nelle terapie cellulari può limitare quanto a lungo i recettori ingegnerizzati rimangono sulla superficie cellulare. Per affrontare questo problema, gli autori hanno utilizzato l’RNA circolare, una forma ad anello chiuso naturalmente più resistente alla degradazione. Hanno codificato il CAR basato su CLMS10 in RNA circolare e lo hanno introdotto nelle NK, insieme all’RNA per l’interleuchina-21. Rispetto all’mRNA lineare, l’RNA circolare ha prodotto un’espressione del CAR più duratura per diversi giorni senza danneggiare la vitalità cellulare. In esperimenti ripetuti di sfida tumorale in vitro, le NK programmate con RNA circolare hanno mantenuto un’uccisione delle cellule tumorali più forte e duratura, hanno continuato a secernere mediatori immunitari chiave e sono rimaste efficaci anche esposte ad alti livelli di mesotelina rilasciata.
Dimostrare la resistenza al shedding in un contesto tumorale difficile
Per imitare l’ambiente tumorale reale, il team ha usato fibroblasti associati al cancro — cellule di supporto che circondano molti tumori solidi e sono note per aumentare il rilascio di mesotelina e attenuare le risposte immunitarie. In colture miste di cellule del cancro pancreatico e questi fibroblasti, le CAR-NK standard mirate alla mesotelina perdevano gran parte della loro potenza. Al contrario, le CAR-NK a RNA circolare basate su CLMS10 continuavano a uccidere le cellule tumorali nonostante l’aumento dell’antigene rilasciato. Testate in topi portatori di un modello tumorale pancreatico ricco di fibroblasti ed espressore di mesotelina, queste CAR-NK ottimizzate hanno ridotto i tumori con efficacia paragonabile alle CAR-NK ingegnerizzate con lentivirus tradizionali, mantenendo però vantaggi per la produzione rapida e non virale. Negli animali non sono emersi segni evidenti di tossicità dovuti al potenziamento temporaneo con interleuchina-21.
Cosa significa per i pazienti
Questa ricerca delinea un progetto per costruire terapie cellulari più intelligenti in grado di resistere a una delle principali strategie di fuga dei tumori solidi. Abbinando un anticorpo che afferra una porzione stabile e vicina alla membrana della mesotelina con una piattaforma di RNA circolare che mantiene il recettore più a lungo sulle NK, gli autori hanno creato un prodotto CAR-NK resistente al shedding e persistente che funziona bene in modelli difficili di cancro pancreatico. Pur richiedendo ulteriori studi prima dei trial umani, l’approccio potrebbe accelerare la progettazione di terapie CAR-NK pronti-all’uso per tumori difficili da trattare, offrendo una via verso trattamenti immunitari più affidabili e duraturi.
Citazione: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Parole chiave: Terapia con cellule CAR-NK, shedding della mesotelina, RNA circolare, cancro del pancreas, ingegneria degli anticorpi