Clear Sky Science · ru
Быстрая скрининговая система CAR и CAR‑NK клетки на основе circRNA для устойчивой терапии, нечувствительной к сбриванию антигена
Почему это важно для будущих методов лечения рака
Многие слышали о CAR‑T терапиях, которые перенастраивают иммунную систему на поимку раковых клеток. Однако эти подходы испытывают трудности с агрессивными солидными опухолями, такими как рак поджелудочной железы. В этом исследовании показан новый способ инженерии другого типа иммунных клеток — естественных киллеров (NK) — чтобы они продолжали действовать даже тогда, когда опухоль использует один из своих любимых трюков уклонения: отщепляет ту самую мишень, которую терапия должна распознавать. Работа также представляет новую РНК‑технологию, которая может сделать разработку таких клеточных терапий быстрее и их производство проще.
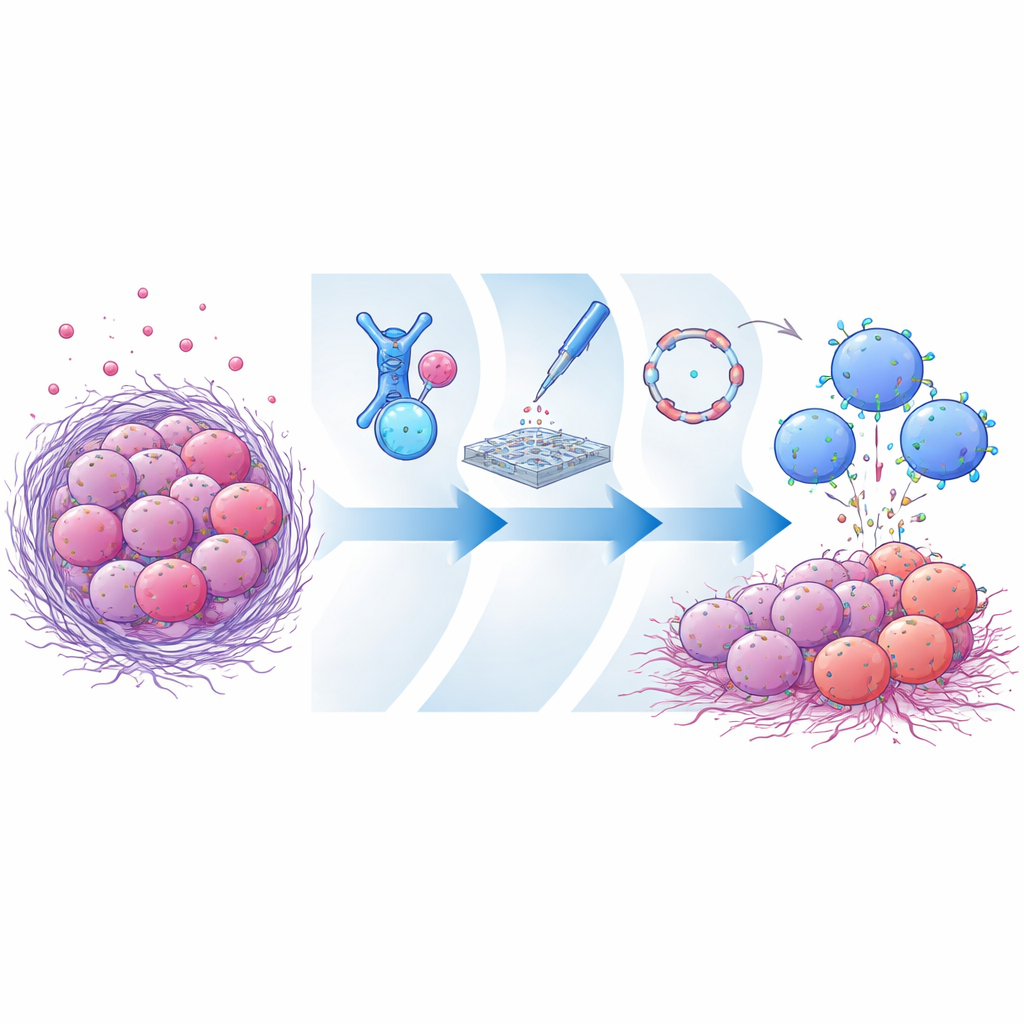
Трюк опухоли с исчезающей мишенью
Во многих агрессивных опухолях высоко экспрессируется поверхностный белок мезотелин. Поскольку в здоровых тканях его значительно меньше, мезотелин давно рассматривают как привлекательную мишень для экспериментальных препаратов и клеточных терапий. Однако опухоли могут срезать внешнюю часть мезотелина и выпускать её в кровоток. Эти свободные фрагменты действуют как приманка, связывая терапевтические антитела или рецепторы CAR до того, как те доберутся до поверхности раковой клетки. Ранние терапии в основном нацеливались на удалённые участки мезотелина, которые легко отрываются, поэтому они особенно уязвимы к такому эффекту‑«приманки». Задача состоит в том, чтобы найти сайт связывания, который остаётся на клеточной поверхности после сбривания, но при этом позволяет иммунным клеткам образовывать плотный и эффективный контакт с опухолью.
Поиск лучшей «ручки» на раковой клетке
Исследователи сначала создали огромную библиотеку фрагментов антител, распознающих мезотелин, и экспонировали их на дрожжевых клетках. Через несколько раундов отбора они обогатили кандидатов, которые сильно связывались с целым, мембранно‑связанным вариантом мезотелина, но почти не связывались с его растворимой, сбритой формой. Один выдающийся фрагмент антитела, названный CLMS10, прикреплялся рядом с участком мезотелина, остающимся у мембраны после расщепления — очень близко к клеточной мембране. Моделирование на компьютере показало, что эта позиция перекрывает сам сайт разреза, физически мешая ферментам, которые отрезают мезотелин, или, по крайней мере, предпочитает мембранную форму. Когда CLMS10 встроили в конструкции CAR и протестировали в первичных человеческих NK‑клетках, эти клетки эффективно убивали мезотелин‑положительные раковые клетки и в значительной степени не реагировали на высокие уровни растворимого мезотелина, в отличие от нескольких опорных CAR.
Быстрая проверка напрямую в человеческих NK‑клетках
Вместо медленных вирусных методов или использования суррогатных клеточных линий команда применила инженерный быстрый тест-платформу непосредственно в донорских человеческих NK‑клетках. Они кодировали разные конструкции CAR в виде линейных мРНК и доставляли их электропорацией, что позволяло NK‑клеткам временно экспрессировать каждую кандидат‑версию рецептора. Это дало возможность быстро сравнить, насколько хорошо разные фрагменты антител, сигнальные домены и дополнительные иммунные усилители работают в реалистичных NK‑клетках, а не в бессмертных суррогатах. Через такие параллельные функциональные тесты они обнаружили, что сочетание CLMS10 с внутренним сигнальным модулем, содержащим домены OX40 и CD3ζ, существенно повышает уничтожение опухолей, де грануляцию NK‑клеток и их метаболическую жизнеспособность. Совместная доставка цитокина интерлейкина‑21 дополнительно улучшала характеристики, помогая NK‑клеткам поддерживать активность в бедных питательными веществами и иммуносупрессивных условиях, имитирующих опухолевую среду.
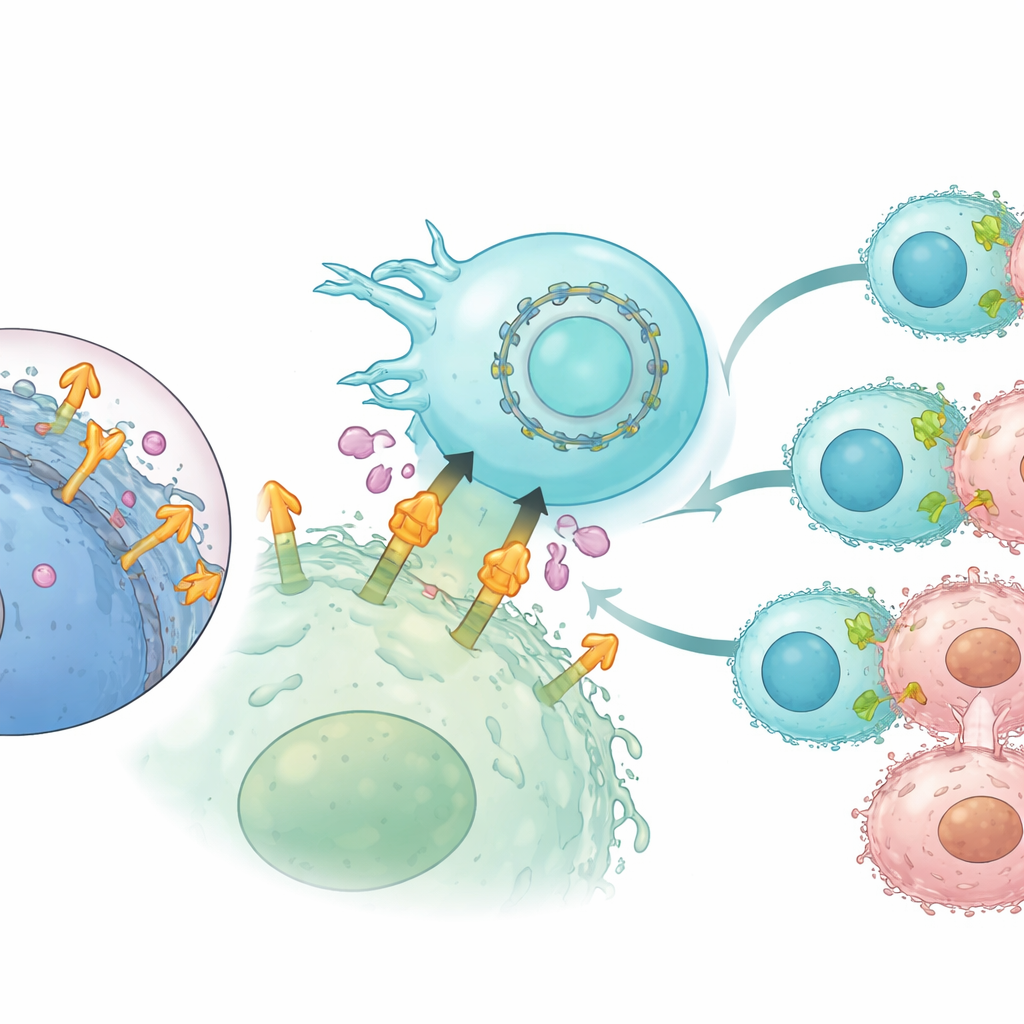
Удлинение экспрессии CAR с помощью круговой РНК
Поскольку обычная мРНК быстро разрушается, её применение в клеточных терапиях ограничивает время пребывания инженерных рецепторов на поверхности клетки. Чтобы решить эту проблему, авторы обратились к круговой РНК — формату замкнутой петлевой РНК, который естественно более устойчив к деградации. Они закодировали CAR на основе CLMS10 в круговой РНК и ввели её в NK‑клетки, снова вместе с РНК интерлейкина‑21. По сравнению с линейной мРНК круговая РНК обеспечивала более длительную экспрессию CAR в течение нескольких дней, не вредя жизнеспособности клеток. В повторных экспериментах с вызовом опухоли в лаборатории NK‑клетки, запрограммированные круговой РНК, сохраняли более сильное и длительное уничтожение раковых клеток, продолжали выделять ключевые иммунные медиаторы и оставались эффективными даже при высоких уровнях сбритого мезотелина.
Демонстрация устойчивости к сбриванию в жесткой опухолевой среде
Чтобы смоделировать реальную опухолевую среду, команда использовала ассоциированные с опухолью фибробласты — поддерживающие клетки, окружающие многие солидные опухоли, которые известны тем, что усиливают сбривание мезотелина и подавляют иммунный ответ. В смешанных культурах клеток рака поджелудочной железы и этих фибробластов стандартные CAR‑NK клетки, направленные против мезотелина, теряли большую часть своей эффективности. Напротив, CAR‑NK клетки на основе CLMS10 в формате круговой РНК продолжали убивать раковые клетки несмотря на выбросы сбритого антигена. При тестировании в мышах с фибробласт‑богатой моделируемой мезотелин‑выражающей опухолью поджелудочной железы эти оптимизированные CAR‑NK клетки сокращали опухоли так же эффективно, как традиционно созданные с помощью лентивируса CAR‑NK клетки, при этом сохраняя преимущества быстрой невирусной технологии производства. Животные не показали очевидных признаков токсичности от временного усиления интерлейкином‑21.
Что это значит для пациентов
Это исследование очерчивает план по созданию более умных клеточных терапий, способных выдерживать одну из ключевых стратегий уклонения солидных опухолей. Сочетая антитело, захватывающее стабильный участок мезотелина близко у мембраны, с платформой круговой РНК, которая дольше удерживает рецептор на NK‑клетках, авторы создали продукт CAR‑NK, устойчивый к сбриванию и обладающий длительной активностью в сложных моделях рака поджелудочной железы. Хотя до клинических испытаний на людях ещё далеко, подход может ускорить разработку готовых к применению CAR‑NK терапий для трудноизлечимых опухолей, проложив путь к более надёжным и долговременным иммунным методам лечения.
Цитирование: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Ключевые слова: Терапия CAR‑NK клетками, сбривание мезотелина, круговая РНК, рак поджелудочной железы, инженерия антител