Clear Sky Science · fr
Dépistage rapide des CAR et cellules CAR-NK à ARNc circulaire pour une immunothérapie persistante résistante au détachement
Pourquoi cela compte pour les futurs traitements du cancer
Beaucoup de personnes ont entendu parler des thérapies CAR-T qui reprogramment le système immunitaire pour traquer les cancers. Mais ces traitements ont peiné face aux tumeurs solides difficiles comme le cancer du pancréas. Cette étude présente une nouvelle manière d’ingénier un autre type de cellule immunitaire — les cellules tueuses naturelles (NK) — afin qu’elles puissent continuer à agir même lorsque les tumeurs utilisent l’une de leurs ruses favorites pour échapper à l’attaque : détacher la cible que la thérapie est censée reconnaître. Le travail introduit aussi une nouvelle technologie ARN susceptible d’accélérer la conception de telles thérapies cellulaires et d’en faciliter la fabrication.
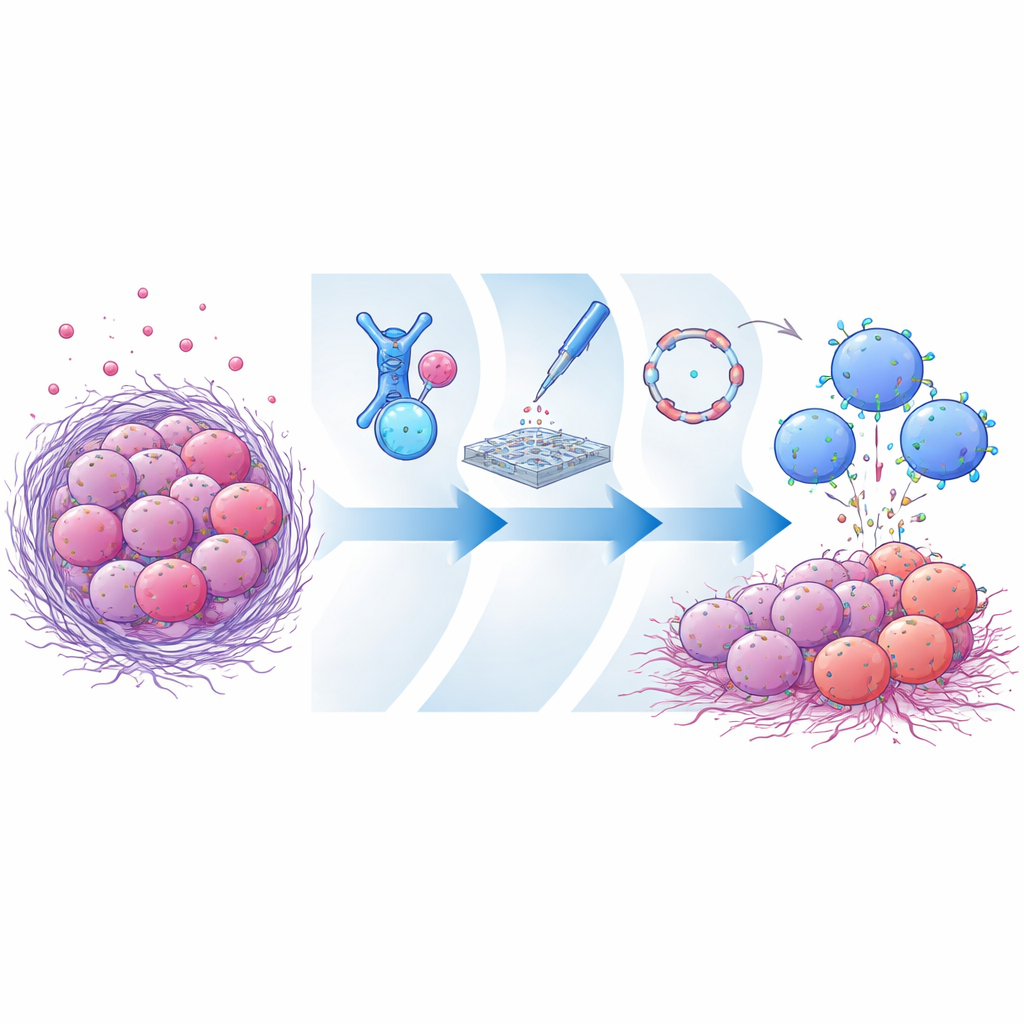
La ruse de la cible qui disparaît
De nombreux cancers agressifs présentent des niveaux élevés d’une molécule de surface appelée mésothéline. Parce que les tissus sains en possèdent beaucoup moins, la mésothéline a été une cible populaire pour des médicaments expérimentaux et des thérapies cellulaires. Cependant, les tumeurs peuvent sectionner la portion externe de la mésothéline et la libérer dans la circulation sanguine. Ces fragments libres agissent comme des leurres, absorbant les anticorps thérapeutiques ou les récepteurs CAR avant qu’ils n’atteignent la surface des cellules cancéreuses. Les thérapies antérieures se liaient principalement à des régions distales de la mésothéline qui sont facilement détachées, les rendant particulièrement vulnérables à cet effet de leurre. Le défi est de trouver un site de liaison qui reste ancré à la membrane cellulaire après le détachement tout en permettant aux cellules immunitaires d’établir un contact étroit et efficace avec la tumeur.
Trouver une meilleure prise sur la cellule cancéreuse
Les chercheurs ont d’abord créé une vaste bibliothèque de fragments d’anticorps reconnaissant la mésothéline et les ont affichés sur des cellules de levure. Après plusieurs cycles de sélection, ils ont enrichi des candidats qui se lient fortement à la version intacte et ancrée à la membrane de la mésothéline mais peu à sa forme soluble détachée. Un fragment d’anticorps remarquable, nommé CLMS10, se fixait près de la portion de la mésothéline qui reste ancrée après la coupure — très proche de la membrane cellulaire. La modélisation informatique a suggéré que cette position chevauche le site de clivage lui-même, bloquant physiquement les enzymes qui sectionnent la mésothéline ou, à tout le moins, favorisant la forme liée à la membrane. Lorsqu’on a intégré CLMS10 dans des constructions CAR et testé celles-ci dans des cellules NK humaines primaires, ces cellules ont efficacement tué des cellules cancéreuses positives pour la mésothéline et ont été largement indifférentes à des niveaux élevés de mésothéline soluble, contrairement à plusieurs CAR de référence.
Tests rapides directement dans des cellules NK humaines
Plutôt que d’utiliser des méthodes virales lentes ou des lignées cellulaires substitutives, l’équipe a adopté une plate-forme de test rapide de type ingénierie directement dans des cellules NK de donneurs humains. Ils ont encodé différentes constructions CAR sous forme d’ARNm linéaire et les ont délivrées par électroporation, permettant aux cellules NK d’exprimer transitoirement chaque récepteur candidat. Cela a permis de comparer rapidement la performance de divers fragments d’anticorps, domaines de signalisation et stimulateurs immunitaires additionnels dans des cellules NK réalistes plutôt que dans des modèles immortalisés. Grâce à ces tests fonctionnels comparatifs, ils ont constaté que la combinaison de CLMS10 avec un module de signalisation interne contenant les domaines OX40 et CD3ζ augmentait sensiblement la cytotoxicité tumorale, la dégranulation des NK et la forme métabolique. La co-administration de la cytokine interleukine-21 a ensuite affiné encore les performances, aidant les NK à maintenir leur activité dans des conditions tumorales pauvres en nutriments et suppressives.
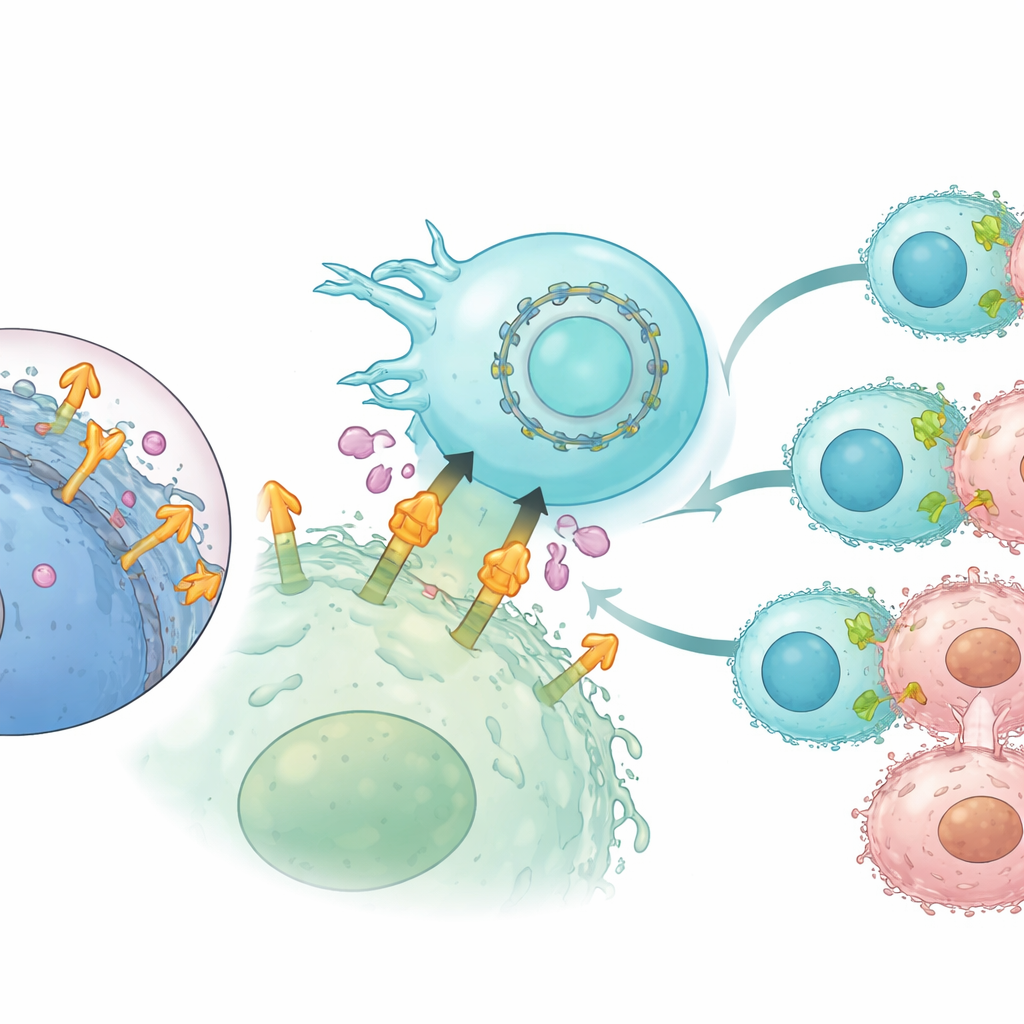
Prolonger l’expression des CAR avec de l’ARN circulaire
Parce que l’ARNm classique est de courte durée, son utilisation dans les thérapies cellulaires peut limiter le temps pendant lequel les récepteurs modifiés restent à la surface cellulaire. Pour y remédier, les auteurs se sont tournés vers l’ARN circulaire, un format d’ARN en boucle fermée qui résiste naturellement mieux à la dégradation. Ils ont encodé le CAR basé sur CLMS10 dans de l’ARN circulaire et l’ont introduit dans les cellules NK, accompagné à nouveau de l’ARN codant l’interleukine-21. Par rapport à l’ARNm linéaire, l’ARN circulaire a permis une expression plus durable du CAR sur plusieurs jours sans nuire à la viabilité cellulaire. Dans des expériences répétées de défi tumoral en laboratoire, les NK programmés avec de l’ARN circulaire ont maintenu une capacité de tuer les cellules cancéreuses plus forte et plus durable, ont continué à sécréter des messagers immunitaires clés et sont restés efficaces même exposés à des niveaux élevés de mésothéline détachée.
Montrer la résistance au détachement dans un contexte tumoral difficile
Pour reproduire l’environnement tumoral réel, l’équipe a utilisé des fibroblastes associés au cancer — des cellules de soutien qui entourent de nombreuses tumeurs solides et sont connues pour augmenter le détachement de la mésothéline et atténuer les réponses immunitaires. Dans des cultures mixtes de cellules de cancer du pancréas et de ces fibroblastes, les CAR-NK ciblant la mésothéline standard perdaient une grande partie de leur puissance. En revanche, les CAR-NK à ARNc basés sur CLMS10 ont continué à éliminer les cellules cancéreuses malgré l’augmentation de l’antigène détaché. Testées chez des souris porteuses d’un modèle de tumeur pancréatique riche en fibroblastes et exprimant la mésothéline, ces cellules CAR-NK optimisées ont réduit les tumeurs aussi efficacement que des CAR-NK classiques conçus par lentivirus, tout en conservant les avantages d’une fabrication rapide et non virale. Les animaux n’ont montré aucun signe évident de toxicité lié au renforcement temporaire par l’interleukine-21.
Ce que cela signifie pour les patients
Cette recherche propose une feuille de route pour construire des thérapies cellulaires plus intelligentes capables de résister à l’une des principales stratégies d’évasion des tumeurs solides. En associant un anticorps qui saisit une portion stable et proche de la membrane de la mésothéline à une plate-forme d’ARN circulaire qui maintient plus longtemps le récepteur sur les NK, les auteurs ont créé un produit CAR-NK résistant au détachement et persistant, performant dans des modèles difficiles de cancer du pancréas. Bien que des travaux supplémentaires soient nécessaires avant des essais humains, l’approche pourrait accélérer la conception de thérapies CAR-NK prêtes à l’emploi pour des cancers difficiles à traiter, offrant une voie vers des traitements immunitaires plus fiables et durables.
Citation: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Mots-clés: thérapie par cellules CAR-NK, détachement de la mésothéline, ARN circulaire, cancer du pancréas, ingénierie des anticorps