Clear Sky Science · ar
فحص CAR سريع وخلايا CAR-NK المدفوعة بـ circRNA لعلاج مناعي دائم ومقاوم للانفصال
لماذا هذا مهم لعلاجات السرطان المستقبلية
يعرف الكثيرون علاجات CAR-T التي تعيد برمجة الجهاز المناعي لصيد السرطانات. لكن هذه العلاجات واجهت صعوبة ضد الأورام الصلبة الصعبة مثل سرطان البنكرياس. تظهر هذه الدراسة طريقة جديدة لهندسة نوع مختلف من الخلايا المناعية — خلايا القتل الطبيعية (NK) — بحيث تظل فعالة حتى عندما تستخدم الأورام إحدى حيلها المفضلة للتهرب: اقتطاع الهدف الذي يفترض بالعلاج التعرف عليه. كما يقدم العمل تقنية RNA جديدة قد تجعل تصميم وتصنيع مثل هذه العلاجات الخلوية أسرع وأسهل.
خدعة الهدف الذي يختفي من الورم
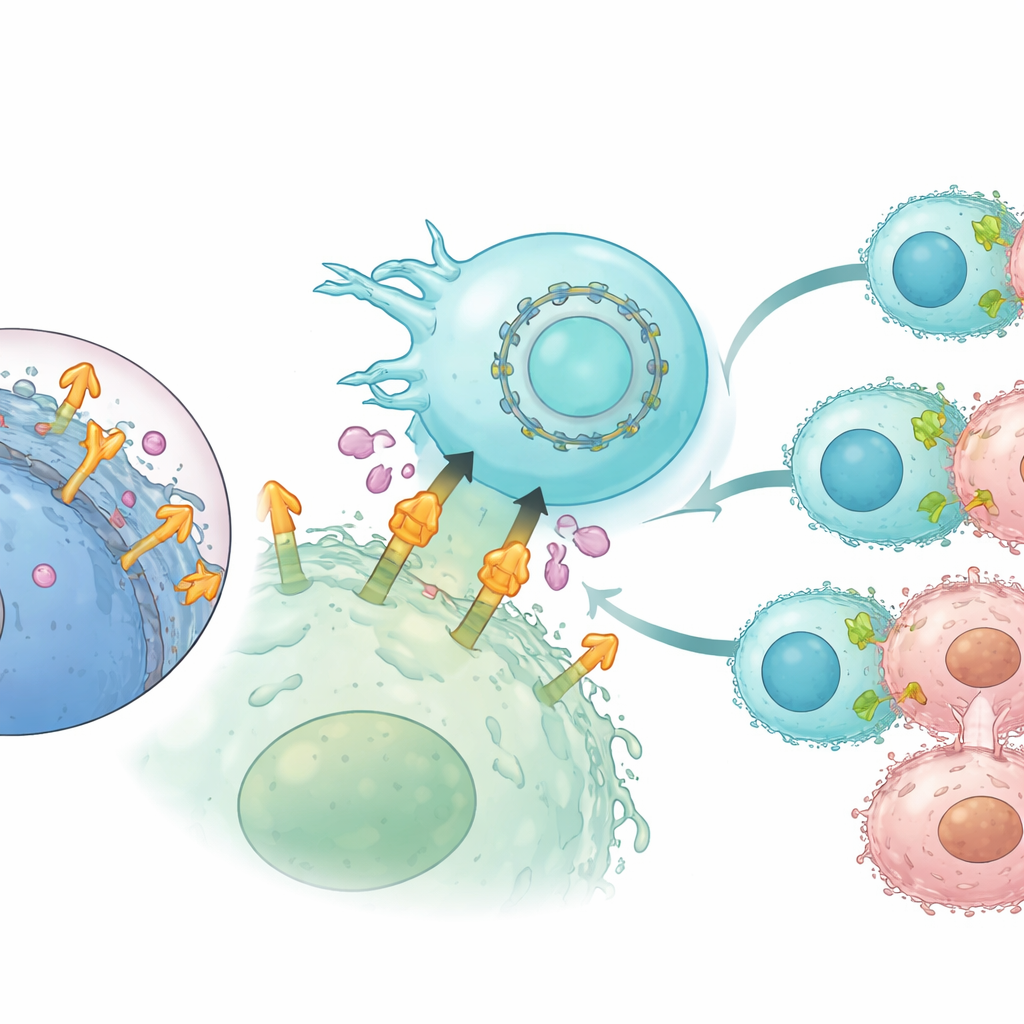
تحمل العديد من السرطانات العدائية مستويات عالية من جزيء سطحي يُدعى الميسوثيلين. وبما أن الأنسجة الصحية تمتلك كمية أقل بكثير منه، فقد كان الميسوثيلين هدفًا شائعًا للأدوية التجريبية والعلاجات الخلوية. ومع ذلك، يمكن للأورام أن تقص الجزء الخارجي من الميسوثيلين وتطلقه في مجرى الدم. تعمل هذه الشظايا الطافية كطُعم، حيث تمتص الأجسام المضادة العلاجية أو مستقبلات CAR قبل أن تصل إلى سطح الخلية السرطانية. كانت العلاجات السابقة ترتبط في الغالب بأجزاء بعيدة من الميسوثيلين يسهل اقتطاعها، لذا كانت عرضة لتأثير الطعم هذا. التحدي هو إيجاد موقع ارتباط يبقى على سطح الخلية بعد الاقتطاع وفي الوقت نفسه يسمح للخلايا المناعية بتشكيل اتصال محكم وفعال مع الورم.
البحث عن مقبض أفضل على خلية السرطان
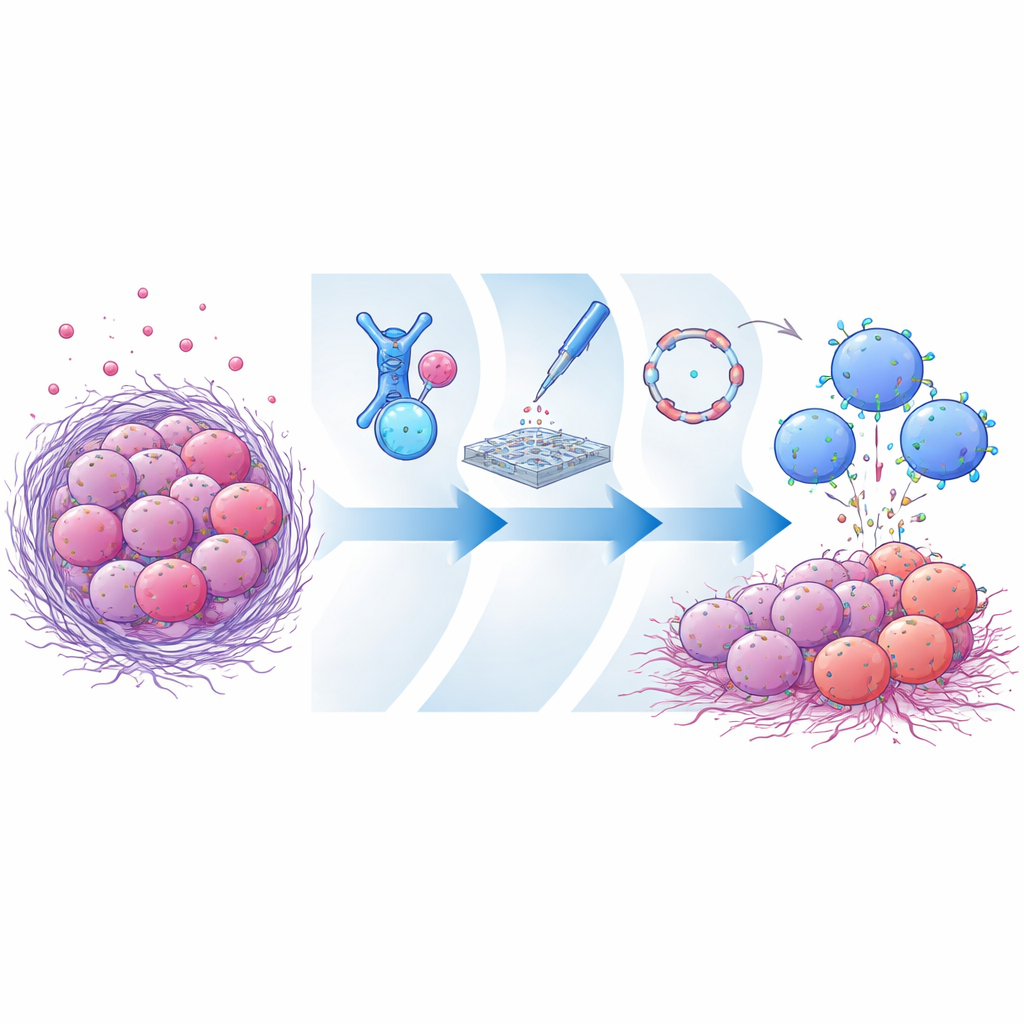
أنشأ الباحثون أولاً مكتبة ضخمة من شظايا الأجسام المضادة التي تتعرف على الميسوثيلين وعرضوها على خلايا الخميرة. من خلال عدة جولات من الانتقاء، ركزوا على المرشحين الذين يرتبطون بقوة بالإصدار السليم المرتبط بالغشاء من الميسوثيلين لكن بالكاد يرتبطون بالشكل القابل للذوبان والمقتطع. أحدى شظايا الأجسام المضادة البارزة، المسماة CLMS10، ارتبطت بالقرب من الجزء من الميسوثيلين الذي يبقى مثبتًا بعد القص — قريبًا جدًا من غشاء الخلية. اقترحت النمذجة الحاسوبية أن هذا الموضع يتداخل مع موقع القص نفسه، مما يحجب الإنزيمات التي تقص الميسوثيلين أو على الأقل يفضل الشكل المرتبط بالغشاء. عندما تمت بناء CLMS10 ضمن تصاميم CAR واختبر في خلايا NK بشرية أولية، قتلت هذه الخلايا خلايا السرطان الإيجابية للميسوثيلين بكفاءة وكانت إلى حد كبير غير متأثرة بمستويات عالية من الميسوثيلين القابل للذوبان، على عكس عدة CAR معيارية.
اختبار سريع مباشرة في خلايا NK بشرية
بدلاً من استخدام طرق فيروسية بطيئة أو خطوط خلوية بديلة، اعتمد الفريق منصة اختبار سريعة على طراز هندسي مباشرة في خلايا NK البشرية المانحة. رمّزوا تصميمات CAR المختلفة كرنا رسول خطي وادخلوه عبر النيلي الكهربائي، مما سمح لخلايا NK بالتعبير المؤقت عن كل مستقبل مرشح. مكّن هذا من المقارنة بسرعة كيف تعمل شظايا الأجسام المضادة المختلفة، ومجالات الإشارة، والمعززات المناعية المضافة في خلايا NK واقعية بدلًا من الخلايا الخالدة. من خلال هذه الاختبارات الوظيفية المتوازية، وجدوا أن الجمع بين CLMS10 ووحدة إشارة داخلية تحتوي على مجالات OX40 وCD3ζ زاد بشكل ملحوظ من قتل الورم، وإفراز حبيبات خلايا NK، والمرونة الأيضية. وساعد التوصيل المشترك للسيتوكين إنترلوكين-21 في تعزيز الأداء، مما مكن خلايا NK من الحفاظ على نشاطها في ظروف مفيدة للفقر الغذائي وكبتية شبيهة بالورم.
إطالة عمر تعبير CAR باستخدام الحمض النووي الريبي الدائري
نظرًا لأن الرنا الرسول الخطي قصير العمر، فقد يحد استخدامه في العلاجات الخلوية من مدة بقاء المستقبلات الهندسية على سطح الخلية. ولمعالجة ذلك، لجأ المؤلفون إلى الحمض النووي الريبي الدائري، وهو صيغة حلقيّة مقاومة طبيعيًا للتحلل. رمّزوا CAR المبني على CLMS10 في RNA دائري وأدخلوه إلى خلايا NK، مرة أخرى مع RNA لإنترلوكين-21. مقارنة بالرنا الرسول الخطي، أدى RNA الدائري إلى تعبير أكثر ديمومة لـ CAR على مدى عدة أيام دون الإضرار بسلامة الخلايا. في تجارب تحدي الورم المتكررة في المختبر، حافظت خلايا NK المبرمجة بالرنا الدائري على قدرة قتل أقوى وأطول أمداً للخلايا السرطانية، وواصلت إفراز رُسل مناعية رئيسية، وبقيت فعالة حتى عند تعرضها لمستويات عالية من الميسوثيلين المقتطع.
إثبات المقاومة للانفصال في بيئة ورمية قاسية
لمحاكاة بيئة الورم الحقيقية، استخدم الفريق الأرومات الليفية المرتبطة بالسرطان — خلايا داعمة تحيط بالعديد من الأورام الصلبة ومعروفة بتعزيز اقتطاع الميسوثيلين وكبت الاستجابات المناعية. في مزارع مختلطة من خلايا سرطان البنكرياس وهذه الأرومات الليفية، فقدت خلايا CAR-NK المستهدفة للميسوثيلين التقليدية الكثير من فعاليتها. بالمقابل، استمرت خلايا CAR-NK المبنية على CLMS10 ومرمزة بالرنا الدائري في قتل الخلايا السرطانية رغم الارتفاع في مستويات المستضد المقتطع. عند اختبارها في فئران تحمل نموذج ورم بنكرياسي غني بالأرومات الليفية ويعبر عن الميسوثيلين، قلصت خلايا CAR-NK المحسَّنة هذه الأورام بفعالية مماثلة لخلايا CAR-NK المصنعة بالعدوى باللنتيفيروس التقليدية، مع احتفاظها بمزايا التصنيع السريع وغير الفيروسي. ولم تظهر الحيوانات علامات واضحة لسُمية ناجمة عن الدفع المؤقت لإنترلوكين-21.
ماذا يعني هذا للمرضى
توضح هذه الدراسة خطة لبناء علاجات خلوية أذكى قادرة على الصمود أمام إحدى استراتيجيات الهرب الرئيسية للأورام الصلبة. بدمج جسم مضاد يمسك بجزء مستقر وقريب من الغشاء من الميسوثيلين مع منصة RNA دائرية تبقي المستقبل على خلايا NK لفترة أطول، أنشأ المؤلفون منتج CAR-NK مقاوم للانفصال ودائم الأداء في نماذج صعبة لسرطان البنكرياس. وبينما يلزم المزيد من العمل قبل التجارب البشرية، قد تُسرّع هذه المقاربة تصميم علاجات CAR-NK جاهزة للتطبيق ضد سرطانات يصعب معالجتها، مما يفتح طريقًا نحو علاجات مناعية أكثر موثوقية وطول أمد.
الاستشهاد: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
الكلمات المفتاحية: علاج خلايا CAR-NK, انفصال الميسوثيلين, الحمض النووي الريبي الدائري, سرطان البنكرياس, هندسة الأجسام المضادة