Clear Sky Science · nl
Snelle CAR-screening en circRNA-gestuurde CAR-NK-cellen voor persistente, shed-resistente immunotherapie
Waarom dit belangrijk is voor toekomstige kankerbehandelingen
Veel mensen hebben gehoord van CAR-T-celtherapieën die het immuunsysteem herprogrammeren om kankercellen op te sporen. Deze behandelingen kampen echter met hardnekkige solide tumoren zoals pancreaskanker. Deze studie toont een nieuwe manier om een ander type immuuncel — natural killer (NK)-cellen — te ontwerpen zodat ze actief blijven, zelfs wanneer tumoren een veelgebruikte truc toepassen om aanvallen te ontwijken: het afknippen van het doelmolecuul dat de therapie moet herkennen. Het werk introduceert ook een nieuwe RNA-technologie die zulke celtherapieën mogelijk sneller te ontwerpen en eenvoudiger te produceren maakt.
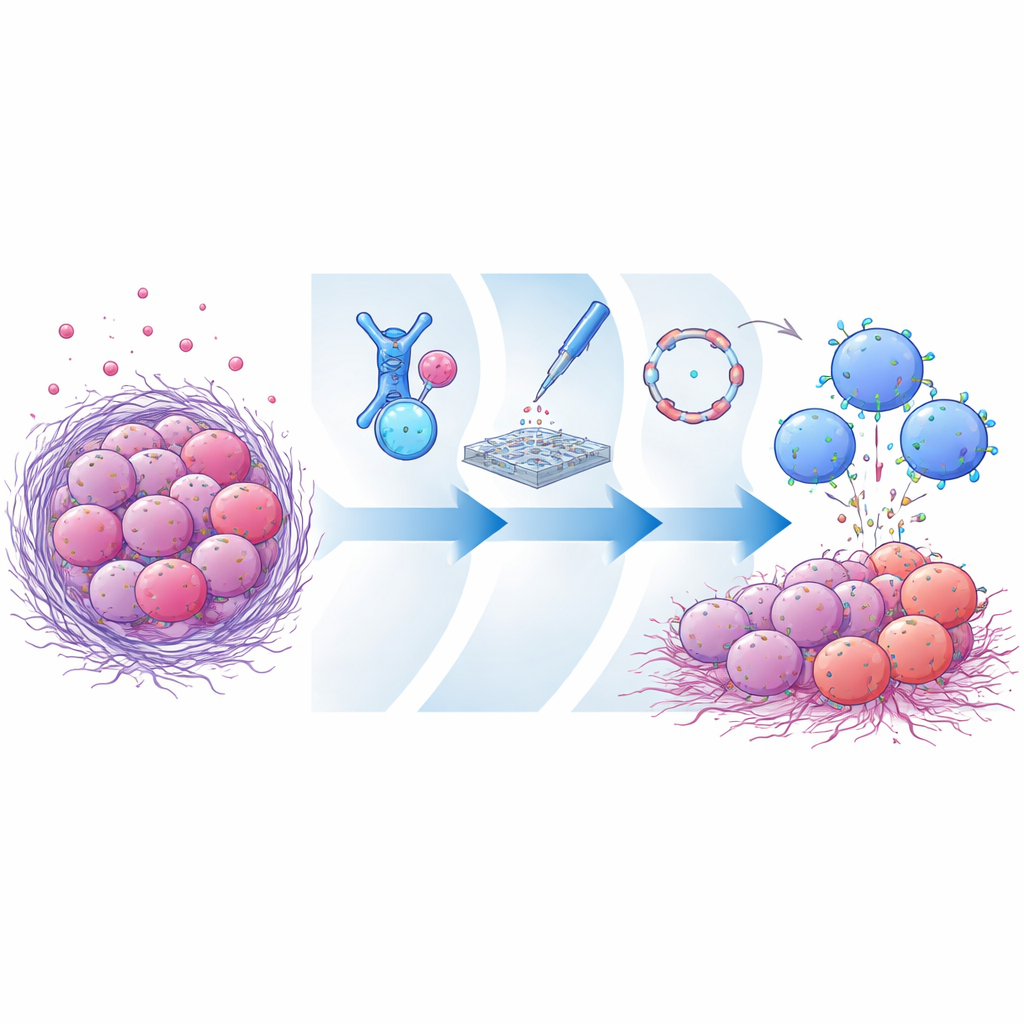
De verdwijntruc van het tumor-doelwit
Veel agressieve kankers hebben hoge niveaus van een oppervlaktemolecuul dat mesothelin heet. Omdat gezonde weefsels veel minder van dit molecuul hebben, is mesothelin een populair mikpunt voor experimentele geneesmiddelen en celtherapieën. Tumoren kunnen echter het buitenste deel van mesothelin afknippen en het in de bloedbaan loslaten. Deze vrije fragmenten fungeren als lokstoffen en binden therapeutische antilichamen of CAR-receptoren voordat die het tumoroppervlak bereiken. Eerdere therapieën richtten zich vaak op gedeelten van mesothelin die gemakkelijk worden afgesplitst, waardoor ze extra kwetsbaar waren voor dit decoy-effect. De uitdaging is een bindingsplaats te vinden die op het celoppervlak blijft na afsplitsing en die toch immuuncellen toestaat een nauwe, effectieve interactie met de tumor aan te gaan.
Een betere greep op de kankercel vinden
De onderzoekers creëerden eerst een enorme bibliotheek van antilichaamfragmenten die mesothelin herkennen en toonden die op gistcellen. Door meerdere selectierondes verrijkten ze kandidaten die sterk binden aan de intacte, membraan-gebonden versie van mesothelin maar nauwelijks aan de oplosbare, afgesplitste vorm. Eén opvallend antilichaamfragment, CLMS10 genoemd, hechtte dicht bij het deel van mesothelin dat na knippen aan het membraan verankerd blijft — zeer dicht bij het celmembraan. Computermodellen suggereerden dat deze positie overlapt met het knipgebied zelf, waardoor de enzymen die mesothelin afscheuren fysiek worden geblokkeerd of ten minste de voorkeur wordt gegeven aan de membraan-gebonden vorm. Toen CLMS10 in CAR-ontwerpen werd ingebouwd en getest in primair humane NK-cellen, doodden deze cellen efficiënt mesothelin-positieve kankercellen en werden ze grotendeels niet beïnvloed door hoge niveaus van oplosbaar mesothelin, in tegenstelling tot verschillende referentie-CARs.
Snel testen direct in menselijke NK-cellen
In plaats van trage virale methoden of surrogate cellijnen te gebruiken, hanteerde het team een engineering-achtige, snelle testplatform direct in menselijke donor-NK-cellen. Ze codeerden verschillende CAR-ontwerpen als lineaire boodschapper-RNA's en leverden deze via elektroporatie, waardoor de NK-cellen elk kandidaatreceptor tijdelijk konden tot expressie brengen. Dit maakte het mogelijk snel te vergelijken hoe goed verschillende antilichaamfragmenten, signaalmodules en aanvullende immuunversterkers werkten in realistische NK-cellen in plaats van in geïmmortaliseerde proefmodellen. Via deze zij-aan-zij functionele tests vonden ze dat het combineren van CLMS10 met een intern signaalmodule dat OX40- en CD3ζ-domeinen bevatte, de tumordoding, NK-cel degranulatie en metabolische fitheid aanzienlijk verhoogde. Het meegeven van het cytokine interleukine-21 verscherpte de prestaties verder en hielp NK-cellen hun activiteit vol te houden in voedingsarme, onderdrukkende tumorachtige omstandigheden.
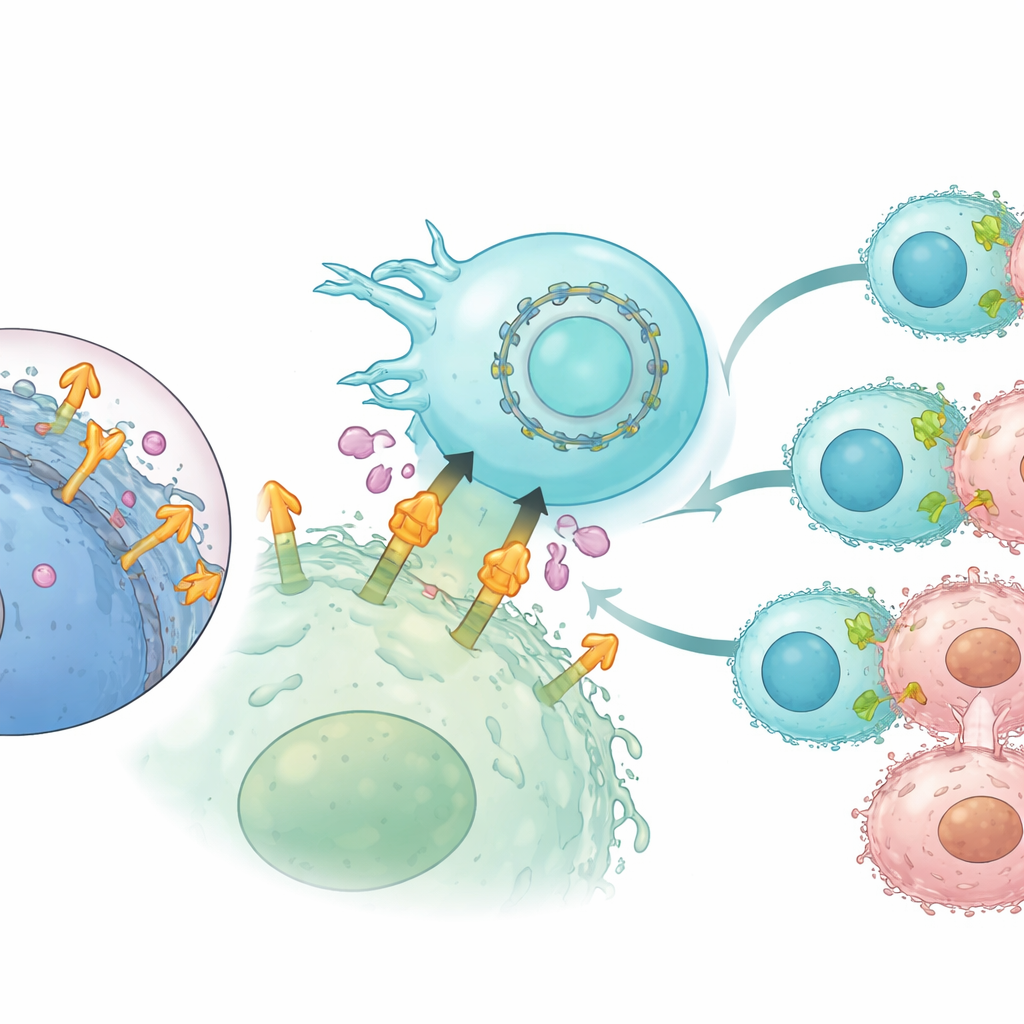
CAR-expressie langer laten aanhouden met circulair RNA
Aangezien regulier mRNA kortstondig is, kan het gebruik ervan in celtherapieën beperken hoe lang de ontworpen receptoren op het celoppervlak blijven. Om dit aan te pakken schakelden de auteurs over op circulair RNA, een gesloten-lus RNA-formaat dat van nature weerbaarder is tegen afbraak. Ze codeerden de CLMS10-gebaseerde CAR in circulair RNA en introduceerden dit in NK-cellen, opnieuw samen met interleukine-21 RNA. In vergelijking met lineair mRNA zorgde circulair RNA voor duurzamere CAR-expressie over meerdere dagen zonder de levensvatbaarheid van de cellen te schaden. In herhaalde tumor-uitdagingsexperimenten in het laboratorium behielden NK-cellen geprogrammeerd met circulair RNA sterkere en langduriger kankerceldoding, bleven ze sleutelimmuunboodschappers afscheiden en bleven ze effectief, zelfs bij blootstelling aan hoge niveaus van afgesplitst mesothelin.
Shed-resistentie bewijzen in een moeilijke tumorumgeving
Om de echte tumorumgeving na te bootsen, gebruikte het team kanker-geassocieerde fibroblasten — ondersteunende cellen die veel solide tumoren omringen en bekendstaan om het verhogen van mesothelin-afsplitsing en het dempen van immuunreacties. In gemengde kweek van pancreaskankercellen en deze fibroblasten verloor standaard mesothelin-gerichte CAR-NK-cellen veel van hun werking. In contrast bleven CLMS10-gebaseerde circulaire RNA CAR-NK-cellen kankercellen doden ondanks de toename van het afgesplitste antigeen. Getest in muizen met een fibroblast-rijke, mesothelin-expressieve pancreastumormodel, verkleinden deze geoptimaliseerde CAR-NK-cellen tumoren even effectief als traditionele lentivirus-geengineerde CAR-NK-cellen, terwijl ze voordelen behielden voor snelle, niet-virale productie. De dieren toonden geen duidelijke tekenen van toxiciteit door de tijdelijke interleukine-21-boost.
Wat dit betekent voor patiënten
Dit onderzoek schetst een blauwdruk voor het bouwen van slimere celtherapieën die bestand zijn tegen één van de belangrijkste ontsnappingsstrategieën van solide tumoren. Door een antilichaam te combineren dat een stabiel, membraan-dicht deel van mesothelin grijpt met een circulair RNA-platform dat de receptor langer op NK-cellen houdt, creëerden de auteurs een shed-resistent, persistent CAR-NK-product dat goed presteert in uitdagende pancreaskankermodellen. Hoewel er meer werk nodig is voordat menselijke proeven mogelijk zijn, kan de benadering het ontwerp van kant-en-klare CAR-NK-therapieën voor moeilijk te behandelen kankers versnellen en zo een pad bieden naar betrouwbaardere en duurzamere immuun-gebaseerde behandelingen.
Bronvermelding: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Trefwoorden: CAR-NK-celtherapie, mesothelinedegradatie, circulair RNA, pancreaskanker, antilichaamengineering