Clear Sky Science · de
Schnelles CAR-Screening und circRNA-getriebene CAR-NK-Zellen für anhaltende, gegen Shed-resistente Immuntherapie
Warum das für künftige Krebstherapien wichtig ist
Viele haben von CAR-T-Zelltherapien gehört, die das Immunsystem so umprogrammieren, dass es Krebszellen jagt. Gegen robuste solide Tumoren wie Pankreaskrebs hatten diese Therapien jedoch begrenzten Erfolg. Diese Studie stellt einen neuen Weg vor, eine andere Immunzellart – natürliche Killerzellen (NK-Zellen) – so zu konstruieren, dass sie wirksam bleiben, selbst wenn Tumoren einen ihrer bevorzugten Ausweichtricks einsetzen: das Abscheren des eigentlichen Zielmoleküls, das die Therapie erkennen soll. Die Arbeit führt außerdem eine neue RNA-Technologie ein, die solche Zelltherapien schneller zu entwerfen und leichter herzustellen machen könnte.
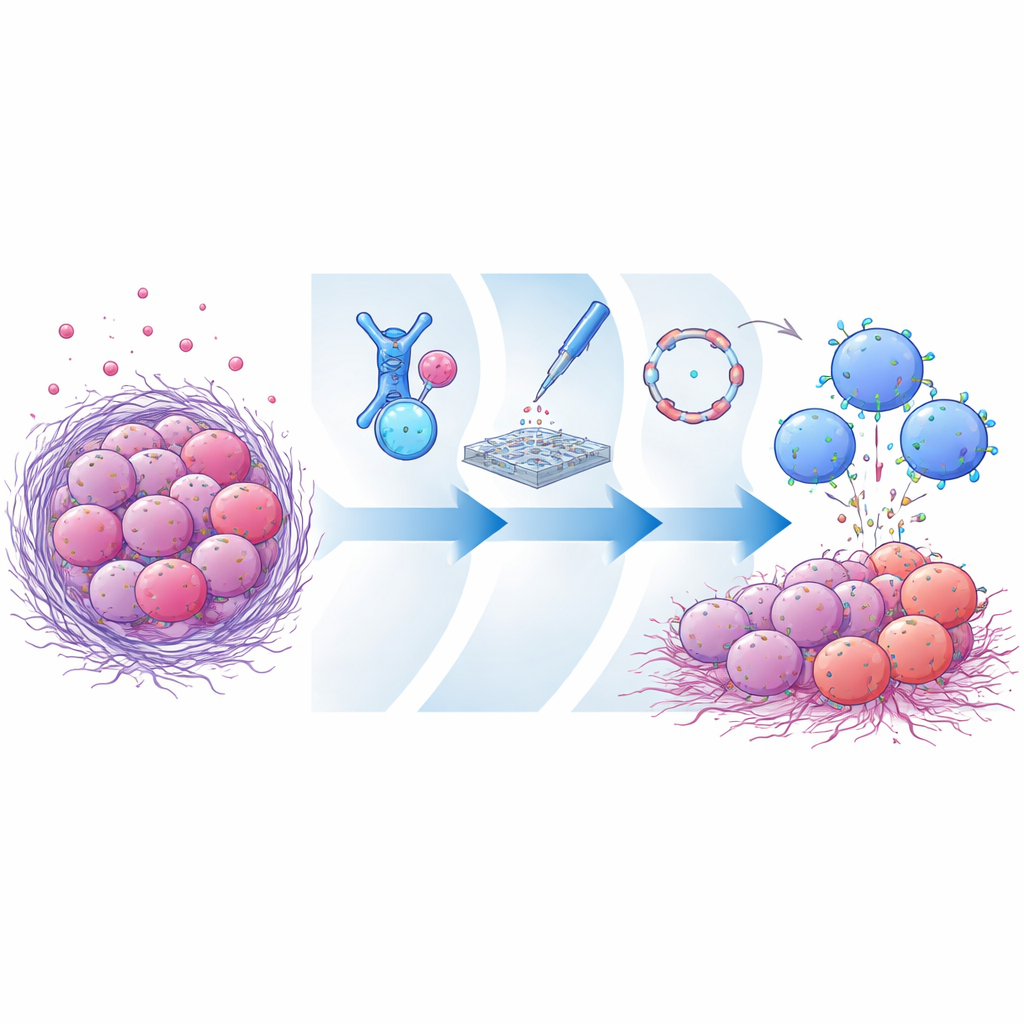
Der Trick: Das Ziel des Tumors verschwindet
Viele aggressive Tumoren tragen hohe Mengen eines Oberflächenmoleküls namens Mesothelin. Da gesunde Gewebe deutlich weniger davon haben, ist Mesothelin ein beliebtes Ziel für experimentelle Wirkstoffe und Zelltherapien. Tumoren können jedoch den äußeren Teil von Mesothelin abschneiden und ins Blut freisetzen. Diese frei zirkulierenden Fragmente wirken wie Köder, indem sie therapeutische Antikörper oder CAR-Rezeptoren binden, bevor diese die Tumorzelloberfläche erreichen. Frühere Therapien banden meist entfernte, leicht abschneidbare Bereiche von Mesothelin und waren daher besonders anfällig für diesen Ködereffekt. Die Herausforderung besteht darin, eine Bindungsstelle zu finden, die nach dem Abscheren an der Zelloberfläche verbleibt und gleichzeitig Immunscheren erlaubt, einen engen, effektiven Kontakt mit dem Tumor herzustellen.
Eine bessere Eintrittspforte an der Krebszelle finden
Die Forschenden erzeugten zunächst eine sehr große Bibliothek von Antikörperfragmenten, die Mesothelin erkennen, und präsentierten diese auf Hefezellen. Durch mehrere Selektionsrunden reichten sie Kandidaten heraus, die stark an die intakte, membrangebundene Form von Mesothelin binden, aber kaum an die lösliche, abgeschiedene Form. Ein herausragendes Antikörperfragment, CLMS10 genannt, heftete sich in der Nähe des Mesothelin-Abschnitts an, der nach der Abspaltung in der Zellmembran verankert bleibt – sehr nahe an der Zellmembran. Computermodelle deuteten darauf hin, dass diese Position mit der Schnittstelle selbst überlappt und somit die Enzyme, die Mesothelin abtrennen, physikalisch blockiert oder zumindest die membrangebundene Form bevorzugt. Als CLMS10 in CAR-Designs eingebaut und in primären menschlichen NK-Zellen getestet wurde, töteten diese Zellen mesothelin-positive Krebszellen effizient und blieben weitgehend unbeeinflusst von hohen Konzentrationen löslichen Mesothelins – im Gegensatz zu mehreren Vergleichs-CARs.
Schnelles Testen direkt in menschlichen NK-Zellen
Statt langsame virale Methoden oder Ersatzzelllinien zu verwenden, nutzte das Team eine engineering-orientierte Schnelltestplattform direkt in NK-Zellen von Spendern. Sie kodierten verschiedene CAR-Designs als lineare mRNAs und lieferten diese per Elektroporation, sodass die NK-Zellen die jeweiligen Rezeptoren vorübergehend exprimieren konnten. Das ermöglichte einen schnellen Vergleich, wie gut verschiedene Antikörperfragmente, Signaldomänen und zusätzliche Immunverstärker in realistischen NK-Zellen wirkten, statt in unsterblichen Stellvertretern. Durch diese direkten Funktionsvergleiche fanden sie, dass die Kombination von CLMS10 mit einem internen Signalmodule, das OX40- und CD3ζ-Domänen enthielt, die Tumorzellabtötung, NK-Zell-Degranulation und den metabolischen Fitnessgrad deutlich erhöhte. Die gleichzeitige Zugabe des Zytokins Interleukin-21 verbesserte die Leistung weiter und half NK-Zellen, ihre Aktivität in nährstoffarmen, suppressiven tumorähnlichen Bedingungen aufrechtzuerhalten.
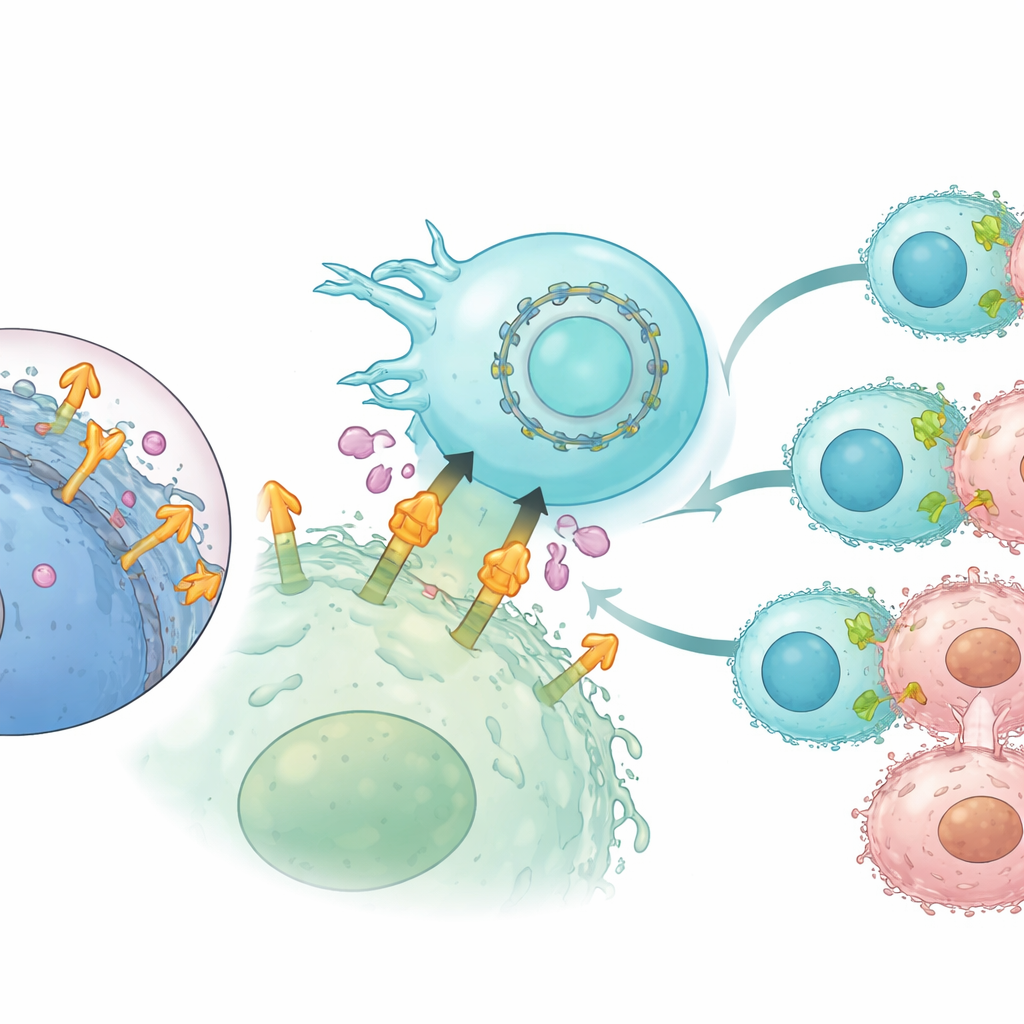
CAR-Expression mit zirkulärer RNA länger aufrechterhalten
Da reguläre mRNA kurzlebig ist, kann ihr Einsatz in Zelltherapien die Dauer begrenzen, in der konstruierte Rezeptoren auf der Zelloberfläche verbleiben. Um dies zu umgehen, wandten sich die Autorinnen und Autoren zirkulärer RNA zu, einem geschlossenen Ring-RNA-Format, das natürlicherweise resistenter gegen Abbau ist. Sie kodierten den CLMS10-basierten CAR in zirkulärer RNA und brachten ihn zusammen mit Interleukin-21-RNA in NK-Zellen ein. Im Vergleich zur linearen mRNA führte zirkuläre RNA zu einer länger anhaltenden CAR-Expression über mehrere Tage, ohne die Zellviabilität zu beeinträchtigen. In wiederholten Tumor-Herausforderungsexperimenten im Labor behielten NK-Zellen, die mit zirkulärer RNA programmiert waren, eine stärkere und länger anhaltende Krebszellabtötung bei, setzten weiterhin wichtige Immunbotenstoffe frei und blieben wirksam, selbst wenn sie hohen Konzentrationen abgeschiedenen Mesothelins ausgesetzt wurden.
Shedding-Resistenz in einem harten Tumorumfeld nachweisen
Um das reale Tumorumfeld nachzubilden, nutzte das Team tumorassoziierte Fibroblasten – Stützzellen, die viele solide Tumoren umgeben und dafür bekannt sind, das Mesothelin-Shedding zu verstärken und Immunantworten zu dämpfen. In Mischkulturen aus Pankreaskrebszellen und diesen Fibroblasten verloren standardmäßige, auf Mesothelin zielende CAR-NK-Zellen einen Großteil ihrer Potenz. Im Gegensatz dazu setzten CLMS10-basierte, zirkuläre-RNA-CAR-NK-Zellen die Abtötung von Krebszellen fort, trotz des Anstiegs des abgeschiedenen Antigens. In Tests an Mäusen mit einem fibroblastenreichen, mesothelin-exprimierenden Pankreastumormodell verkleinerten diese optimierten CAR-NK-Zellen Tumoren ebenso effektiv wie traditionelle, lentiviral hergestellte CAR-NK-Zellen, während sie Vorteile für eine schnelle, nichtvirale Herstellung behielten. Die Tiere zeigten keine offensichtlichen Toxizitätszeichen durch die vorübergehende Interleukin-21-Unterstützung.
Was das für Patientinnen und Patienten bedeutet
Diese Forschung skizziert ein Konzept zum Bau intelligenterer Zelltherapien, die einer der zentralen Fluchtstrategien solider Tumoren standhalten können. Durch die Kombination eines Antikörpers, der einen stabilen, membrannahen Abschnitt von Mesothelin greift, mit einer zirkulären-RNA-Plattform, die den Rezeptor länger auf NK-Zellen hält, schufen die Autorinnen und Autoren ein shed-resistentes, persistentes CAR-NK-Produkt, das in herausfordernden Pankreaskrebsmodellen gut abschneidet. Obwohl weitere Arbeit vor klinischen Studien nötig ist, könnte der Ansatz die Entwicklung von sofort verfügbaren CAR-NK-Therapien für schwer behandelbare Krebsarten beschleunigen und einen Weg zu verlässlicheren und dauerhafteren immunbasierten Behandlungen eröffnen.
Zitation: Chung, JY., Hong, J., Yee, SM. et al. Rapid CAR screening and circRNA-driven CAR-NK cells for persistent shed-resistant immunotherapy. Sig Transduct Target Ther 11, 129 (2026). https://doi.org/10.1038/s41392-026-02623-6
Schlüsselwörter: CAR-NK-Zelltherapie, Mesothelin-Shedding, zirkuläre RNA, Pankreaskrebs, Antikörper-Engineering