Clear Sky Science · sv
Biobildanalys för multiplexade FUCCI-inspelningar med djupinlärning
Att iaktta celler i deras vardag
Varje levande cell går ständigt igenom faser av tillväxt, kopiering av DNA och delning. Biologer har nu fluorescerande verktyg som får cellcykelns olika stadier att lysa i olika färger, vilket gör det möjligt att följa processen i realtid. Men när för många signaler registreras samtidigt blir bilderna brusiga och svåra att tolka — även för datorer. Denna artikel presenterar en metod baserad på djupinlärning som rensar upp dessa komplexa filmer, spårar individuella celler och avgör var i cykeln varje cell befinner sig, vilket ger nytt kraftfullt verktyg för cancerforskning, stamcellsstudier och läkemedelstester.
Glödande tidtagare inne i levande celler
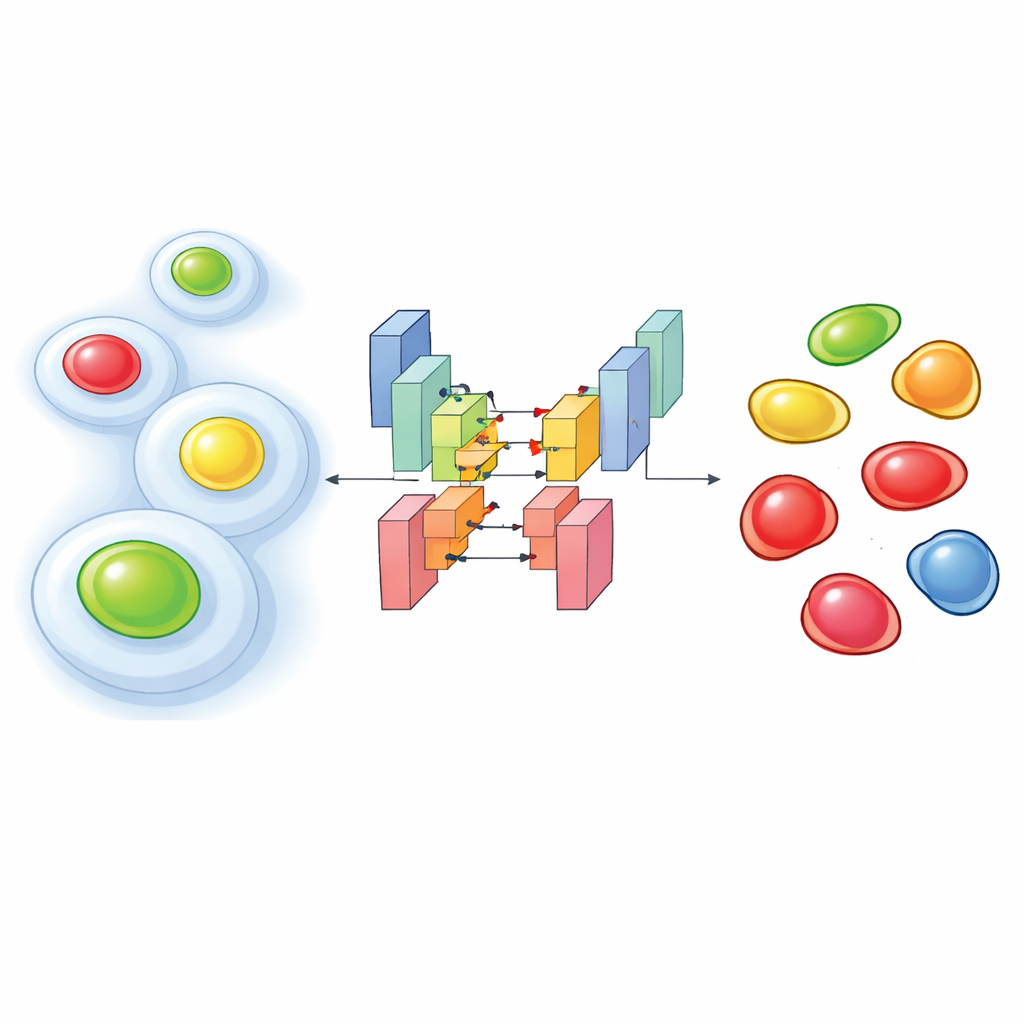
För att se hur celler går igenom sin livscykel använder forskare ofta ett molekylärt verktyg kallat FUCCI, som får cellkärnan att lysa i en färg under de tidiga stadierna och i en annan färg senare, med kombinationer däremellan. Nyare experiment går ett steg längre: de spelar in FUCCI tillsammans med ytterligare fluorescerande markörer som framhäver cellens inre skelett eller andra strukturer. Denna ”multiplexning” hjälper till att koppla vad en cell gör strukturellt till var den befinner sig i sin livscykel. Nackdelen är att för att undvika att skada levande celler måste forskarna belysa dem försiktigt, vilket ger svaga, brusiga bilder där färger läcker över i varandra. Under sådana förhållanden misslyckas ofta standardprogram för bildanalys med att korrekt hitta varje kärna eller tilldela rätt cellcykelfas.
Att lära en algoritm se igenom bruset
Författarna tog itu med problemet genom att träna specialanpassade djupinlärningsnätverk på tusentals noggrant annoterade bilder från två humana cellinjer. Deras metod matar flera kanaler in i en segmenteringsmodell baserad på StarDist-arkitekturen, som är särskilt bra på att rita upp enskilda kärnor. De testade tre inmatningsupplägg: en som bara använder den cytoplasmatiska markören (ett fluorescerande märkt strukturellt protein), en som bara använder de två FUCCI-färgerna och en som kombinerar alla tre. Trots de brusiga förhållandena uppnådde två- och trekanalsversionerna mycket hög noggrannhet i att hitta kärnor och överträffade tydligt populära förtränade verktyg när signalen var svag. Förvånande nog kunde även modellen som bara använde den cytoplasmatiska markören ofta sluta sig till var kärnorna låg, eftersom det omgivande skelettet lämnar ett karakteristiskt ”hål” där kärnan sitter.
Från färgade prickar till cellcykellabels
Att hitta kärnor är bara halva arbetet; forskare behöver också veta i vilken fas av cellcykeln varje kärna befinner sig. Traditionellt görs detta genom att sätta intensitetströsklar på FUCCI-färgerna, en enkel metod som lätt kan luras av läckage från andra kanaler. Teamet utvidgade sitt nätverk så att det inte bara ritar upp varje kärna utan också märker den som tillhörande en av flera cellcykelfaser baserat på färgmönstren. När de jämförde denna metod med den klassiska intensitetströskelmetoden var djupinlärningsklassificeraren mer exakt, särskilt i brusiga data. Den generaliserade till och med till en annan version av FUCCI-systemet från ett annat laboratorium, efter att författarna enkelt ommappar vilka färgkombinationer som motsvarar vilka faser — ingen ny träning krävdes.
Att rekonstruera en cells resa genom tiden
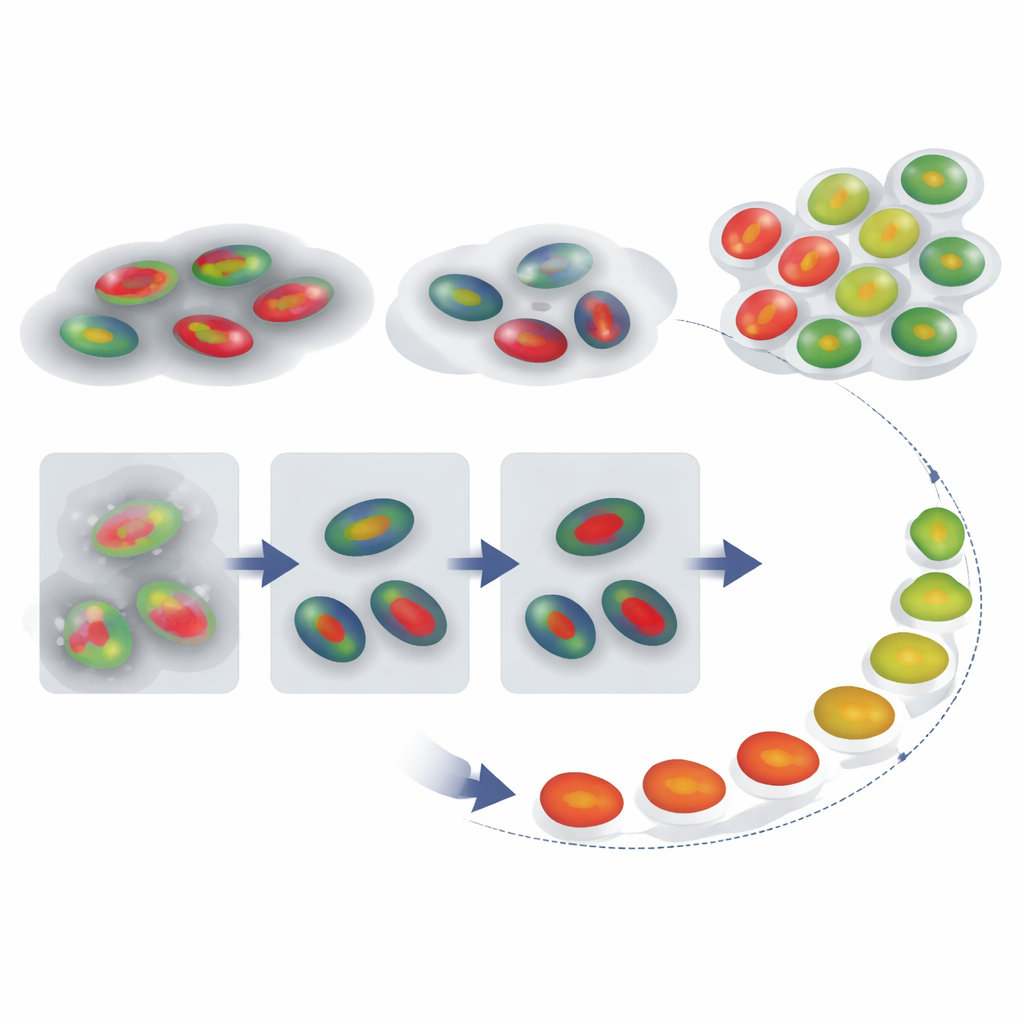
Med tillförlitliga kärnkonturer och fasetiketter kunde författarna sedan undersöka om de kunde rekonstruera hur enskilda celler rör sig genom cykeln över tid, även när en inspelning inte fångar en hel sekvens från delning till delning. De spårade FUCCI-signaler från enstaka celler och jämförde varje intensitetsspår med ett referensmönster för en typisk cykel med en teknik kallad dynamisk tidssträckning (dynamic time warping), som flexibelt sträcker och komprimerar tidsaxeln för att hitta bästa matchning. Detta gav varje cell en ”cellcykelprocent” som fungerar som ett pseudotid — en uppskattning av hur långt den har kommit. Lika viktigt är att mängden tidssträckning som krävs fungerar som en varningssignal: celler vars spår måste kraftigt förvrängas för att matcha referensen beter sig sannolikt abnormt, exempelvis celler som sitter fast länge i en fas.
Varför detta spelar roll för hälsa och sjukdom
Genom att kombinera multiplexad fluorescerande avbildning med skräddarsydda djupinlärningsverktyg levererar detta arbete en slut-till-slut-pipeline: den segmenterar svaga, brusiga bilder, märker varje kärna med en cellcykelfas, spårar celler över tid och flaggar de som avviker från ett standardmönster. För icke-experter är huvudbudskapet att forskare nu kan följa tusentals levande celler mer pålitligt och med mindre manuellt arbete, även vid skonsamma avbildningsförhållanden som bevarar cellernas hälsa. Detta öppnar dörren för mer precisa studier av hur cancerläkemedel stoppar celldelning, hur stamceller bestämmer sitt öde och hur mekaniska krafter i vävnader påverkar när celler väljer att dela sig eller pausa.
Citering: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Nyckelord: avbildning av cellcykeln, djupinlärningsmikroskopi, FUCCI-sensor, cellspårning, biobildanalys