Clear Sky Science · fr
Analyse bioimage pour acquisitions FUCCI multiplexées propulsée par l’apprentissage profond
Observer les cellules vivre leur quotidien
Chaque cellule vivante parcourt en continu des étapes de croissance, de copie de l’ADN et de division. Les biologistes disposent désormais d’outils fluorescents qui font briller ces phases du cycle cellulaire en couleurs distinctes, leur permettant d’observer ce processus en temps réel. Mais lorsqu’un trop grand nombre de signaux est enregistré simultanément, les images deviennent bruitées et difficiles à interpréter — même pour les ordinateurs. Cet article présente une méthode basée sur l’apprentissage profond qui nettoie ces films complexes, suit les cellules individuelles et détermine la phase du cycle de chacune, offrant de nouvelles capacités pour la recherche sur le cancer, les études sur les cellules souches et les tests pharmacologiques.
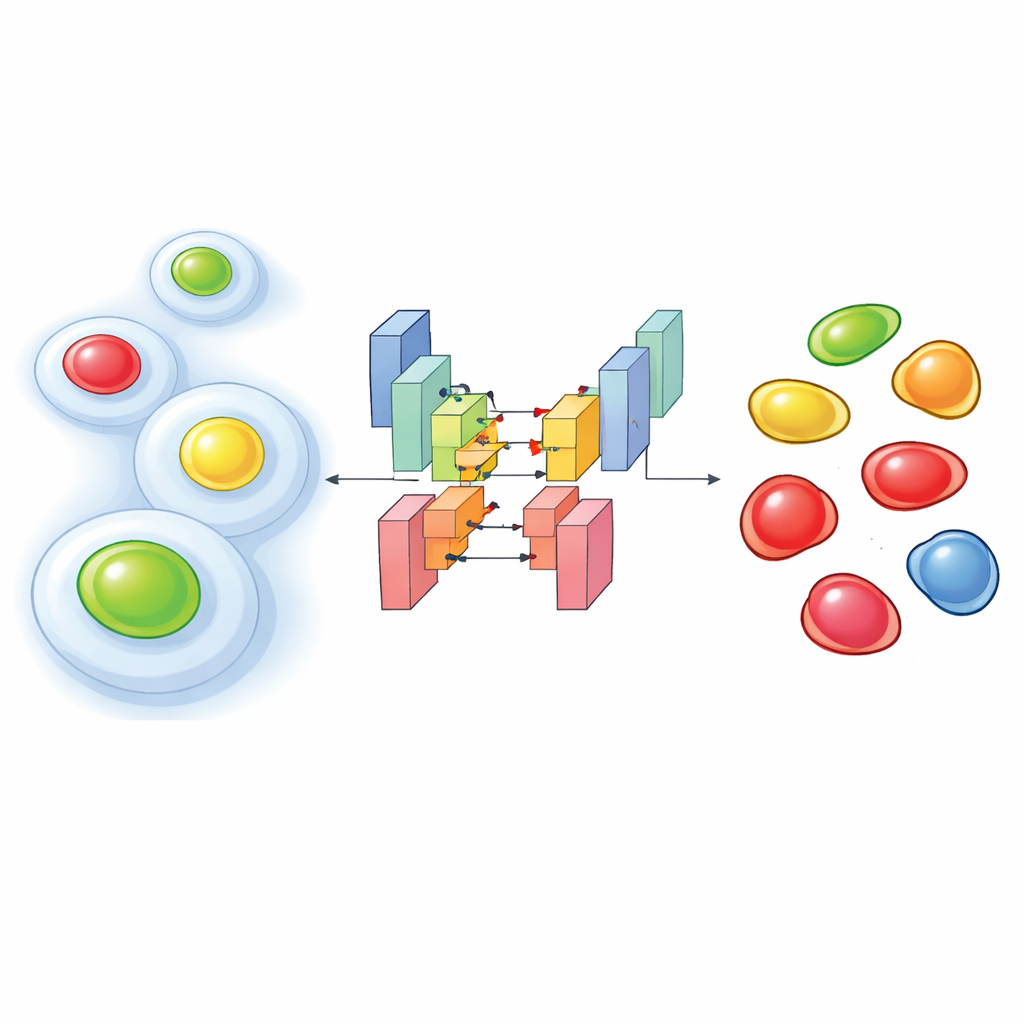
Des minuteries lumineuses à l’intérieur des cellules vivantes
Pour suivre la progression des cellules dans leur cycle de vie, les chercheurs utilisent souvent un outil moléculaire appelé FUCCI, qui fait briller le noyau de la cellule d’une couleur pendant les premières phases et d’une autre couleur plus tard, avec des combinaisons intermédiaires. Les expériences récentes vont plus loin : elles enregistrent FUCCI conjointement à des marqueurs fluorescents supplémentaires qui mettent en évidence l’ossature intracellulaire ou d’autres structures. Ce « multiplexage » permet de relier l’activité structurale d’une cellule à sa position dans le cycle. L’inconvénient est que, pour éviter d’endommager les cellules vivantes, il faut les illuminer faiblement, ce qui produit des images peu lumineuses, bruitées et avec des recouvrements de couleur. Dans ces conditions, les logiciels d’analyse d’images classiques échouent souvent à détecter correctement chaque noyau ou à assigner la bonne phase du cycle.
Apprendre à un algorithme à voir à travers le bruit
Les auteurs ont abordé ce problème en entraînant des réseaux d’apprentissage profond personnalisés sur des milliers d’images soigneusement annotées provenant de deux lignées cellulaires humaines. Leur approche alimente plusieurs canaux dans un modèle de segmentation basé sur l’architecture StarDist, particulièrement efficace pour délimiter les noyaux individuels. Ils ont testé trois configurations d’entrée : une n’utilisant que le marqueur cytoplasmique (une protéine structurelle marquée par fluorescence), une n’utilisant que les deux couleurs FUCCI, et une combinant les trois. Malgré les conditions bruyantes, les versions à deux et trois canaux ont atteint une très grande précision dans la détection des noyaux, surpassant nettement des outils pré-entraînés populaires lorsque le signal était faible. Fait surprenant, même le modèle utilisant uniquement le marqueur cytoplasmique pouvait souvent inférer la position des noyaux, car le réseau environnant laisse un « trou » caractéristique à l’emplacement du noyau.
Des points colorés aux étiquettes de phase du cycle
Détecter les noyaux ne suffit pas ; il faut aussi savoir dans quelle phase du cycle se trouve chaque noyau. Traditionnellement, on procède en appliquant des seuils d’intensité sur les couleurs FUCCI, une méthode simple qui peut être trompée par le recouvrement des canaux. L’équipe a étendu son réseau pour qu’il ne se contente pas de délimiter chaque noyau, mais qu’il l’étiquette également comme appartenant à l’une des phases du cycle en fonction des motifs de couleur. En comparant cette approche à la méthode classique par seuil d’intensité, le classificateur par apprentissage profond s’est révélé plus précis, surtout sur des données bruitées. Il s’est même généralisé à une version différente du système FUCCI provenant d’un autre laboratoire, après que les auteurs eurent simplement remappé quelles combinaisons de couleurs correspondaient à quelles phases — sans réentraînement.
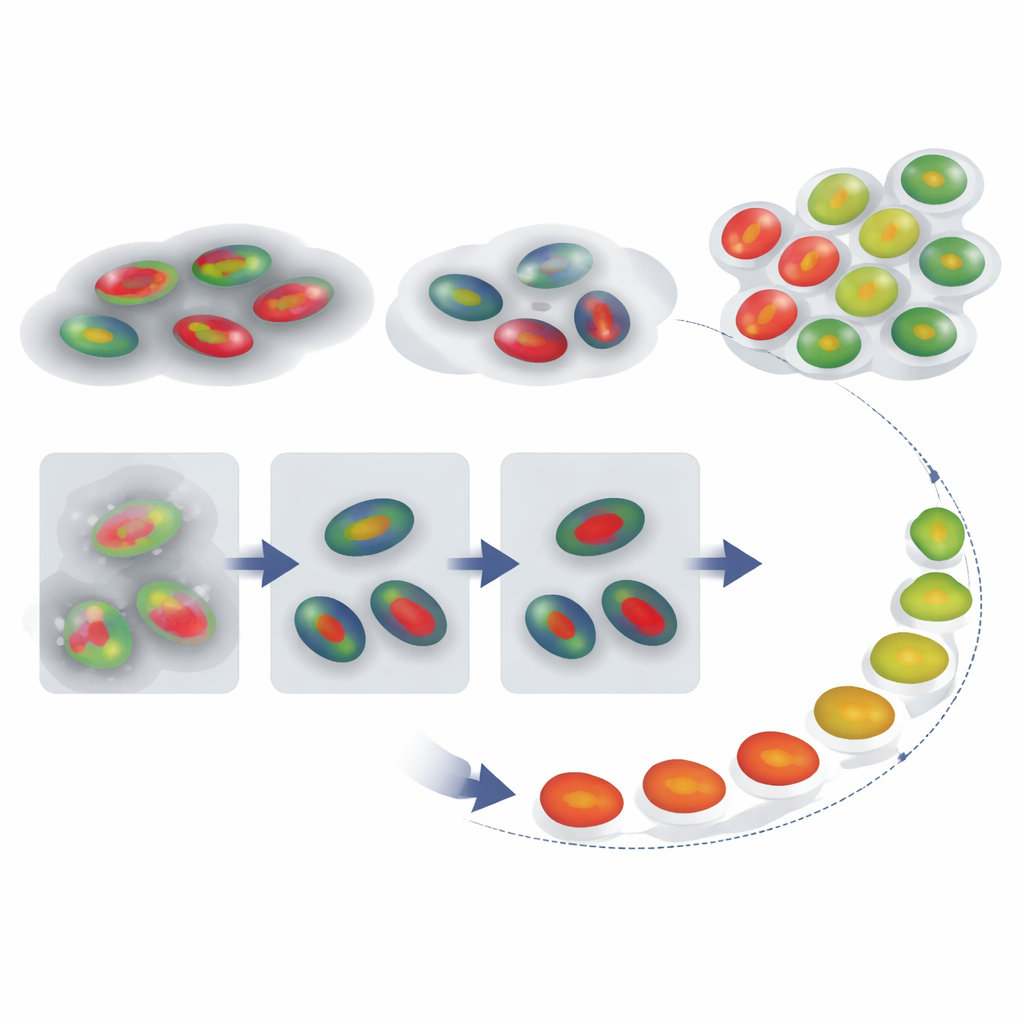
Reconstruire le parcours temporel d’une cellule
Avec des contours nucléaires et des étiquettes de phase fiables, les auteurs se sont ensuite demandé s’ils pouvaient reconstruire comment des cellules individuelles traversent le cycle au fil du temps, même lorsqu’un enregistrement ne capture pas une séquence complète division-à-division. Ils ont suivi les signaux FUCCI de cellules uniques et comparé chaque trace d’intensité à un motif de référence pour un cycle typique en utilisant une technique appelée dynamic time warping, qui étire et compresse de manière flexible l’axe temporel pour trouver le meilleur alignement. Cela a fourni à chaque cellule un « pourcentage de cycle cellulaire » agissant comme un pseudotemps — une estimation de son avancement. Autre point important : l’amplitude de l’étirement temporel nécessaire fait office d’alerte : les cellules dont les traces doivent être fortement déformées pour correspondre à la référence se comportent probablement de façon anormale, par exemple en restant longtemps bloquées dans une phase.
Pourquoi cela compte pour la santé et la maladie
En combinant l’imagerie fluorescente multiplexée avec des outils d’apprentissage profond adaptés, ce travail propose une chaîne complète : il segmente des images faibles et bruitées, étiquette chaque noyau selon une phase du cycle, suit les cellules dans le temps et signale celles qui dévient du modèle standard. Pour les non-spécialistes, le message clé est que les chercheurs peuvent désormais suivre des milliers de cellules vivantes de façon plus fiable et avec moins d’effort manuel, même avec des conditions d’imagerie douces qui préservent la santé cellulaire. Cela ouvre la voie à des études plus précises sur la manière dont les médicaments anticancéreux arrêtent la division cellulaire, sur les décisions de destin des cellules souches et sur l’influence des forces mécaniques dans les tissus sur le moment où les cellules choisissent de se diviser ou de faire une pause.
Citation: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Mots-clés: imagerie du cycle cellulaire, microscopie par apprentissage profond, capteur FUCCI, suivi cellulaire, analyse bioimage