Clear Sky Science · de
Biobildanalyse für multiplexe FUCCI-Aufnahmen mit Deep Learning
Zellen bei ihrem täglichen Leben beobachten
Jede lebende Zelle durchläuft ständig Phasen von Wachstum, DNA-Vervielfältigung und Teilung. Biologen verfügen heute über fluoreszierende Werkzeuge, die diese Zellzyklusphasen in unterschiedlichen Farben leuchten lassen, sodass sie diesen Prozess in Echtzeit verfolgen können. Wenn jedoch zu viele Signale gleichzeitig aufgezeichnet werden, werden die Bilder verrauscht und schwer zu interpretieren — selbst für Computer. Diese Arbeit stellt eine Deep-Learning-basierte Methode vor, die solche komplexen Filme entrauscht, einzelne Zellen verfolgt und den jeweiligen Zyklusstatus jeder Zelle bestimmt. Das eröffnet neue Möglichkeiten für Krebsforschung, Stammzellstudien und Wirkstofftests.
Leuchtende Zeitmesser innerhalb lebender Zellen
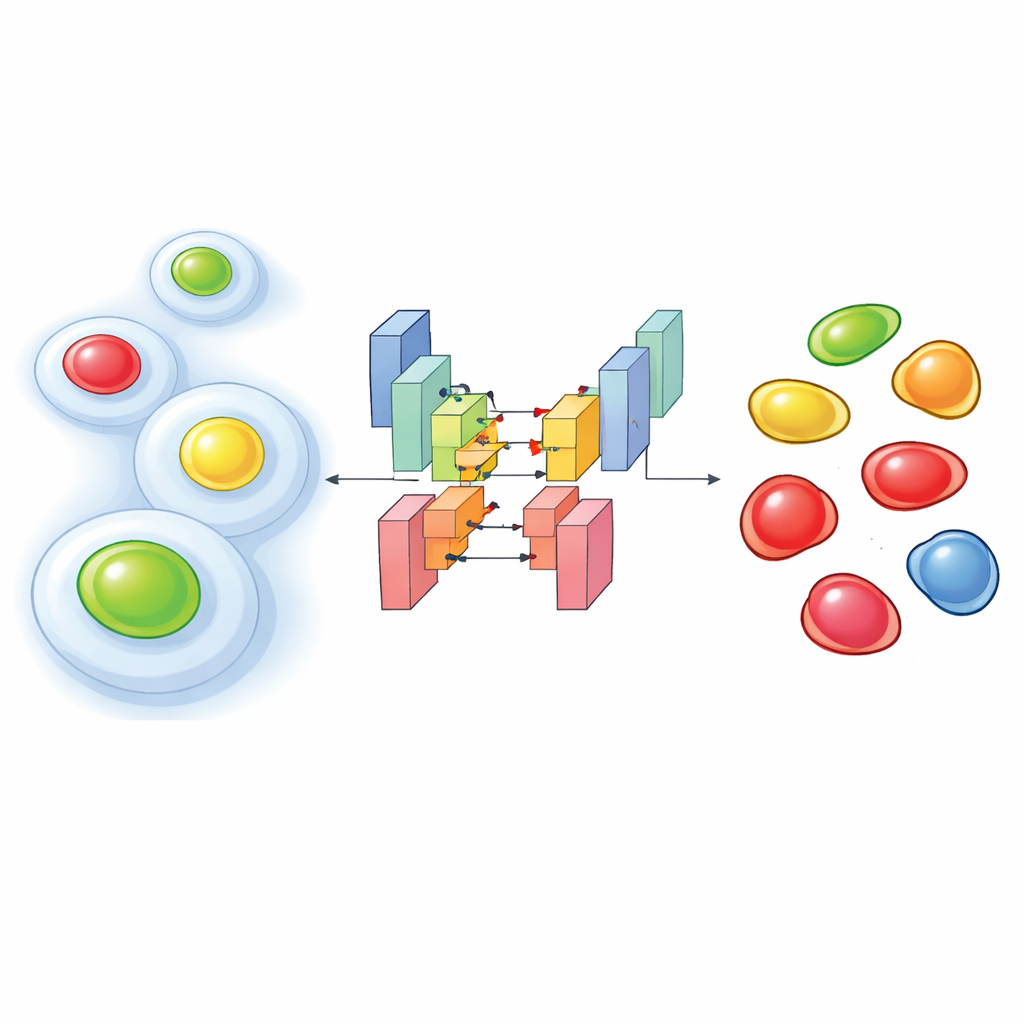
Um zu sehen, wie Zellen ihren Lebenszyklus durchlaufen, verwenden Forscher häufig ein molekulares Werkzeug namens FUCCI, das den Zellkern in frühen Stadien in einer Farbe und in späteren Stadien in einer anderen Farbe leuchten lässt, mit Mischfarben dazwischen. Neuere Experimente gehen einen Schritt weiter: Sie zeichnen FUCCI zusammen mit zusätzlichen fluoreszierenden Markern auf, die das innere Gerüst der Zelle oder andere Strukturen hervorheben. Dieses „Multiplexing“ hilft, die strukturellen Aktivitäten einer Zelle mit ihrem Zyklusstatus zu verknüpfen. Der Nachteil ist, dass man, um lebende Zellen nicht zu schädigen, nur schwach beleuchten darf, was dunkle, verrauschte Bilder erzeugt, in denen Farben ineinander überlaufen. Unter diesen Bedingungen versagt Standard-Bildanalyse-Software häufig darin, jeden Kern korrekt zu finden oder den richtigen Zellzyklusstatus zuzuweisen.
Ein Algorithmus, der durchs Rauschen blickt
Die Autoren gingen dieses Problem an, indem sie maßgeschneiderte Deep-Learning-Netzwerke an Tausenden sorgfältig annotierter Bilder aus zwei menschlichen Zelllinien trainierten. Ihr Ansatz speist mehrere Kanäle in ein Segmentierungsmodell auf Basis der StarDist-Architektur ein, das besonders gut darin ist, einzelne Zellkerne zu umreißen. Sie testeten drei Eingabesetups: eines, das nur den zytoplasmatischen Marker (ein fluoreszenzmarkiertes Strukturprotein) verwendete, eines mit nur den beiden FUCCI-Farben und eines mit allen drei Kanälen kombiniert. Trotz der verrauschten Bedingungen erreichten die Zwei- und Drei-Kanal-Versionen sehr hohe Genauigkeit beim Auffinden der Kerne und übertrafen klar beliebte vortrainierte Werkzeuge, wenn das Signal schwach war. Überraschenderweise konnte oft sogar das Modell, das nur den zytoplasmatischen Marker nutzte, den Aufenthaltsort der Kerne ableiten, weil das umgebende Gerüst eine charakteristische „Lücke“ hinterlässt, in der der Kern sitzt.
Von farbigen Punkten zu Zellzyklus-Etiketten
Das Finden der Kerne ist nur die halbe Miete; Forscher müssen auch wissen, in welcher Phase des Zellzyklus sich jeder Kern befindet. Traditionell wird dies durch Setzen von Intensitätsschwellen auf die FUCCI-Farben erreicht, eine einfache Methode, die durch Übersprechen von Kanälen leicht täuschbar ist. Das Team erweiterte sein Netzwerk so, dass es nicht nur jeden Kern umreißt, sondern ihn auch basierend auf den Farbmuster einem von mehreren Zellzyklusphasen zuordnet. Im Vergleich zur klassischen Intensitätsschwellen-Methode war der Deep-Learning-Klassifikator genauer, besonders bei verrauschten Daten. Er generalisierte sogar auf eine andere Version des FUCCI-Systems aus einem anderen Labor, nachdem die Autoren lediglich neu zuordneten, welche Farbkombinationen welchen Phasen entsprechen — ohne erneutes Training.
Die Reise einer Zelle durch die Zeit rekonstruieren
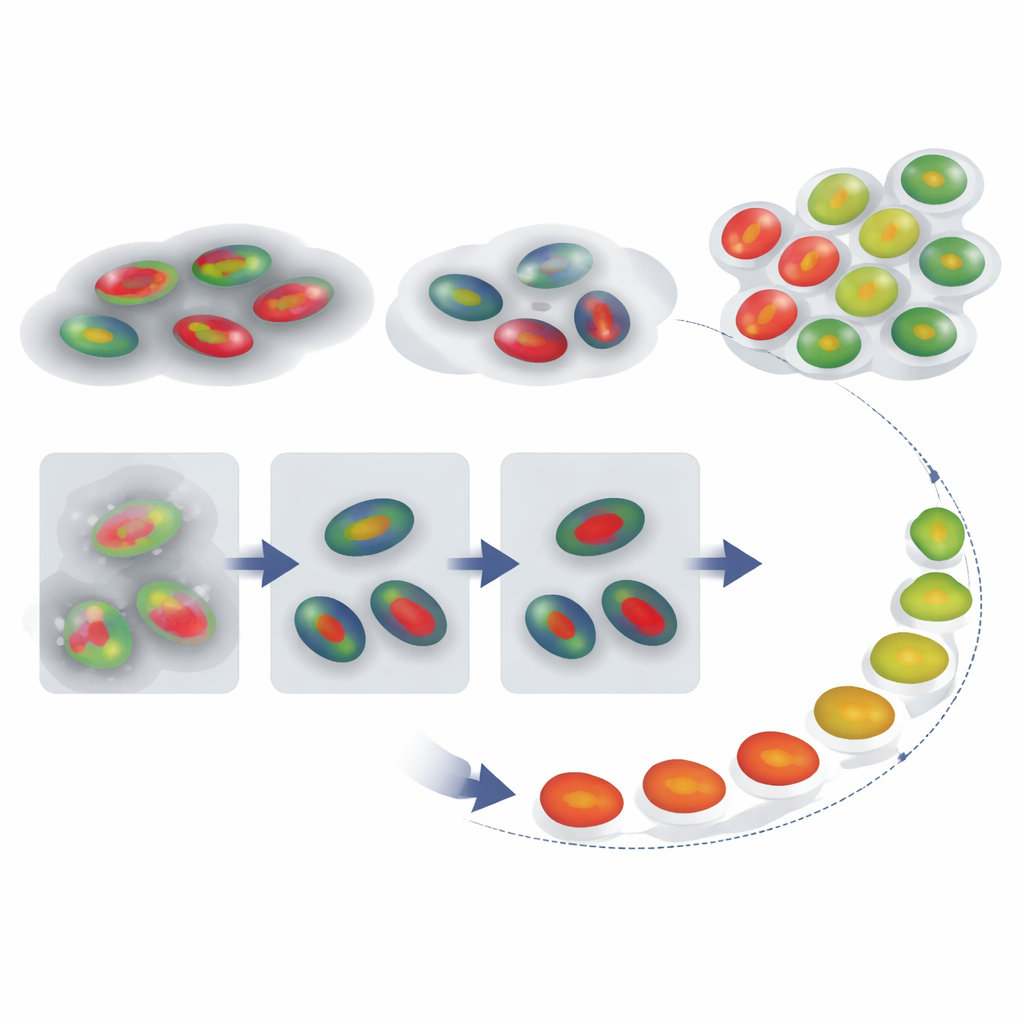
Mit verlässlichen Kernumrissen und Phasenlabels fragten die Autoren als Nächstes, ob sie rekonstruieren können, wie einzelne Zellen sich im Zeitverlauf durch den Zyklus bewegen, selbst wenn eine Aufnahme keine vollständige Division-zu-Division-Abfolge erfasst. Sie verfolgten FUCCI-Signale einzelner Zellen und verglichen jede Intensitätskurve mit einem Referenzmuster für einen typischen Zyklus mithilfe einer Technik namens Dynamic Time Warping, die die Zeitachse flexibel dehnt und staucht, um die beste Übereinstimmung zu finden. Das ergab für jede Zelle einen „Zellzyklus-Prozentsatz“, der wie eine Pseudotime wirkt — eine Schätzung, wie weit sie fortgeschritten ist. Ebenso wichtig ist, dass das Ausmaß der benötigten Zeitdehnung als Alarmzeichen dient: Zellen, deren Kurven stark verzerrt werden müssen, um mit der Referenz übereinzustimmen, verhalten sich wahrscheinlich abnormal, etwa weil sie lange in einer Phase festhängen.
Warum das für Gesundheit und Krankheit wichtig ist
Durch die Kombination von multiplexer Fluoreszenzbildgebung mit maßgeschneiderten Deep-Learning-Werkzeugen liefert diese Arbeit eine durchgängige Pipeline: Sie segmentiert dunkle, verrauschte Bilder, etikettiert jeden Kern mit einer Zellzyklusphase, verfolgt Zellen über die Zeit und markiert diejenigen, die vom Standardmuster abweichen. Für Nicht-Experten lautet die Kernbotschaft, dass Forscher nun Tausende lebender Zellen zuverlässiger und mit weniger manuellem Aufwand verfolgen können, selbst unter schonenden Bildgebungsbedingungen, die die Zellgesundheit erhalten. Das eröffnet präzisere Studien dazu, wie Krebsmedikamente die Zellteilung stoppen, wie Stammzellen ihr Schicksal entscheiden und wie mechanische Kräfte in Geweben beeinflussen, wann Zellen sich zur Teilung entschließen oder eine Pause einlegen.
Zitation: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Schlüsselwörter: Zellzyklus-Bildgebung, Deep-Learning-Mikroskopie, FUCCI-Sensor, Zellverfolgung, Biobildanalyse