Clear Sky Science · pl
Analiza bioobrazów dla wielokanałowych akwizycji FUCCI napędzana uczeniem głębokim
Obserwowanie komórek podczas ich codziennego życia
Każda żywa komórka nieustannie przechodzi przez etapy wzrostu, kopiowania DNA i podziału. Biolodzy dysponują dziś narzędziami fluorescencyjnymi, które sprawiają, że etapy cyklu komórkowego świecą w różnych kolorach, pozwalając obserwować ten proces na żywo. Gdy jednak rejestruje się zbyt wiele sygnałów naraz, obrazy stają się zaszumione i trudne do interpretacji — nawet dla komputerów. Artykuł przedstawia metodę opartą na uczeniu głębokim, która oczyszcza takie złożone sekwencje filmowe, śledzi pojedyncze komórki i odczytuje, na jakim etapie cyklu się znajdują, co daje nowe możliwości w badaniach nad rakiem, komórkach macierzystych i testowaniu leków.
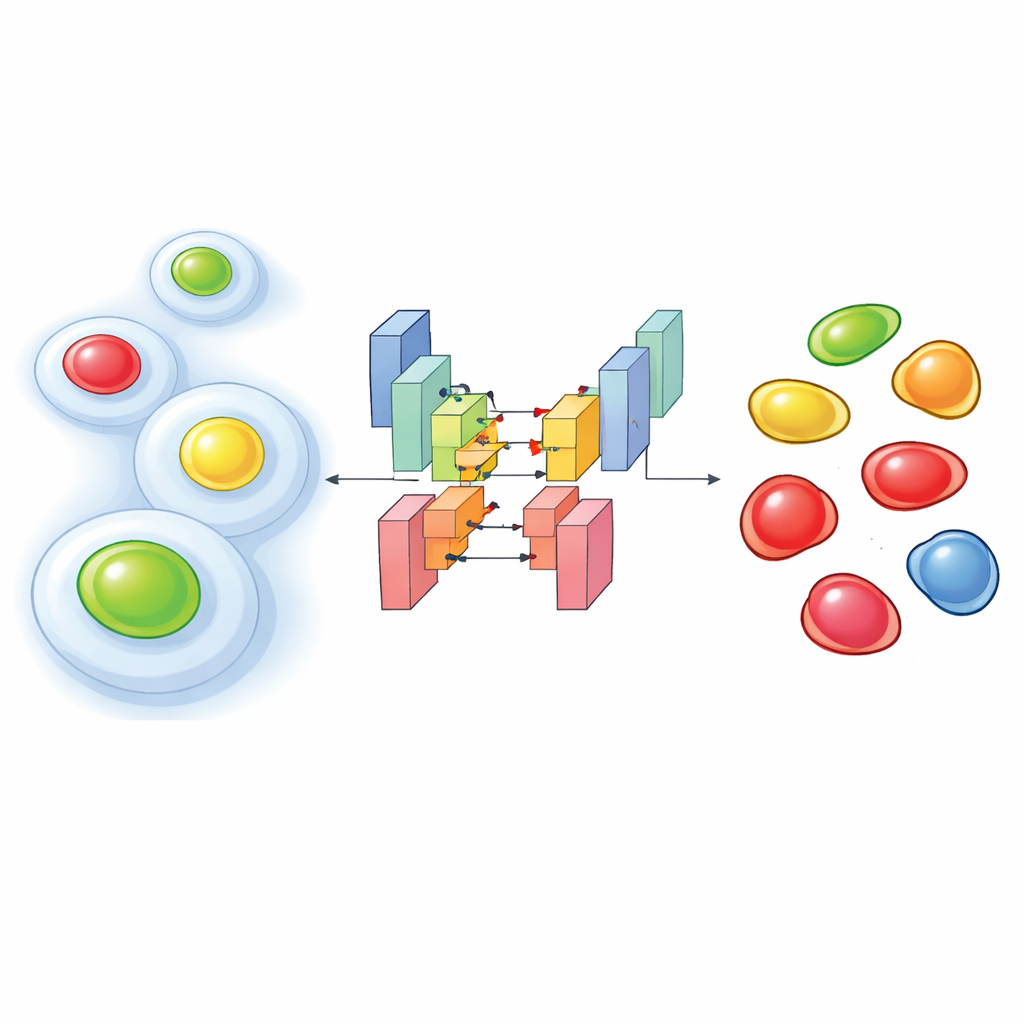
Świecące zegary wewnątrz żywych komórek
Aby śledzić postęp komórek w cyklu życiowym, badacze często używają molekularnego narzędzia zwanego FUCCI, które powoduje, że jądro komórkowe świeci w jednym kolorze we wczesnych etapach, a w innym później, z kombinacjami pośrednimi. Nowsze eksperymenty idą dalej: rejestrują FUCCI razem z dodatkowymi markerami fluorescencyjnymi, które uwidaczniają wewnętrzny szkielet komórki lub inne struktury. Taka „multiplikacja” kanałów łączy informacje o stanie strukturalnym komórki z jej miejscem w cyklu życiowym. Wadą jest to, że aby nie uszkodzić żywych komórek, trzeba je oświetlać delikatnie, co daje słabe, zaszumione obrazy, w których kolory się prześwitują. W takich warunkach standardowe oprogramowanie do analizy obrazów często nie potrafi poprawnie odnaleźć każdego jądra ani przypisać właściwego etapu cyklu.
Nauczanie algorytmu widzenia przez szum
Autorzy rozwiązali ten problem, trenując specjalne sieci głębokiego uczenia na tysiącach starannie opisanych obrazów z dwóch ludzkich linii komórkowych. Ich podejście wprowadza wiele kanałów do modelu segmentacji opartego na architekturze StarDist, która jest szczególnie dobra w wyznaczaniu obrysów pojedynczych jąder. Przetestowali trzy konfiguracje wejściowe: jedną używającą tylko markera cytoplazmatycznego (fluorescencyjnie znakowanego białka strukturalnego), jedną tylko z dwoma kolorami FUCCI i jedną łączącą wszystkie trzy. Pomimo zaszumionych warunków wersje dwukanałowa i trójkanałowa osiągnęły bardzo wysoką dokładność w wykrywaniu jąder, wyraźnie przewyższając popularne narzędzia wstępnie wytrenowane przy słabym sygnale. Co zaskakujące, nawet model korzystający tylko z markera cytoplazmatycznego często potrafił wnioskować położenie jąder, ponieważ otaczający szkielet pozostawia charakterystyczną „dziurę” tam, gdzie znajduje się jądro.
Od kolorowych punktów do etykiet faz cyklu
Wykrycie jąder to tylko połowa zadania; badacze muszą też wiedzieć, w jakiej fazie cyklu znajduje się każde jądro. Tradycyjnie robi się to, ustawiając progi intensywności dla kolorów FUCCI — prosta metoda, którą łatwo zmylić przepływem sygnału między kanałami. Zespół rozszerzył swoją sieć tak, by nie tylko obrysowywała każde jądro, lecz także przypisywała mu etykietę odpowiadającą jednej z faz cyklu na podstawie wzorców kolorów. W porównaniu z klasyczną metodą z progami intensywności, klasyfikator oparty na uczeniu głębokim był dokładniejszy, zwłaszcza przy zaszumionych danych. Działał też z inną wersją systemu FUCCI z innego laboratorium — wystarczyło jedynie przekodować, które kombinacje kolorów odpowiadają którym fazom, bez potrzeby ponownego treningu.
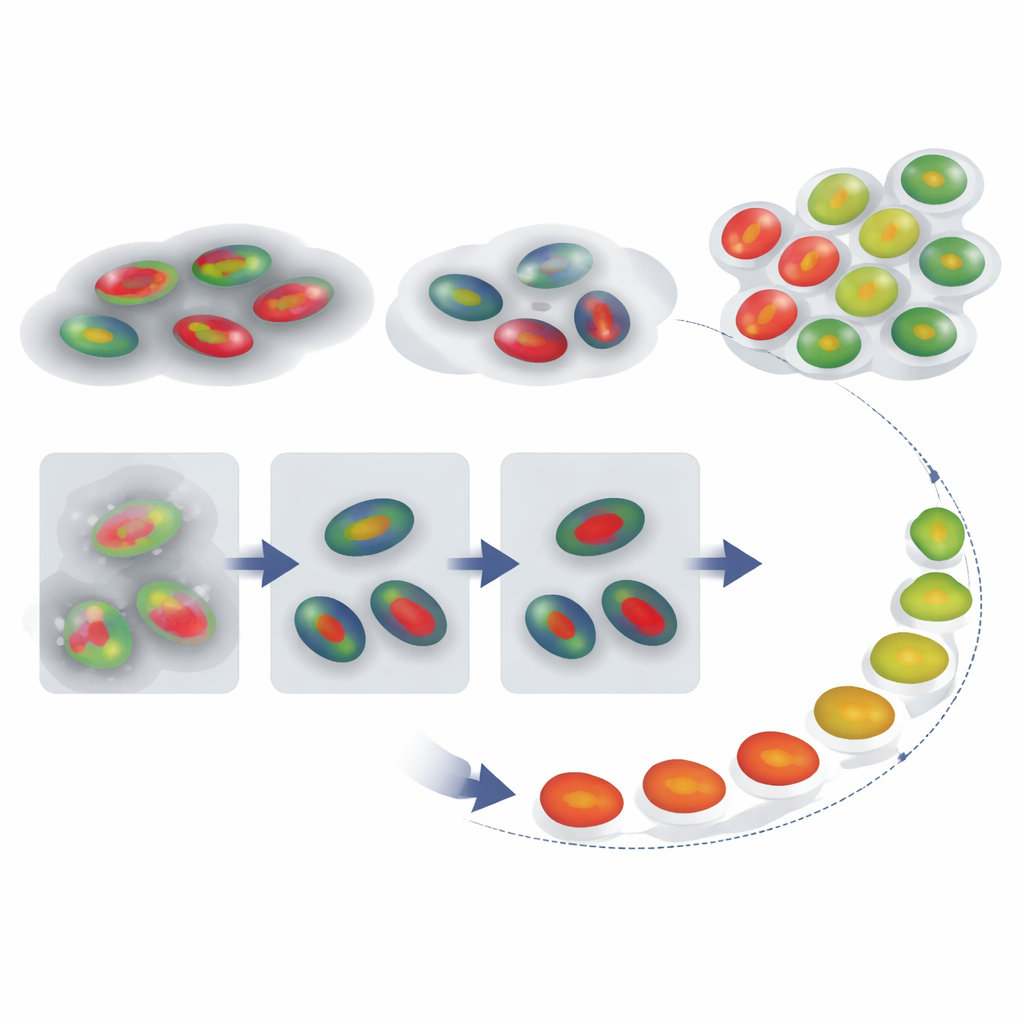
Odtwarzanie podróży komórki w czasie
Mając wiarygodne obrysy jąder i etykiety faz, autorzy sprawdzili, czy można odtworzyć, jak pojedyncze komórki przechodzą przez cykl w czasie, nawet gdy nagranie nie obejmuje pełnego cyklu od podziału do podziału. Śledzili sygnały FUCCI z pojedynczych komórek i porównywali każde śledzenie intensywności z referencyjnym wzorcem typowego cyklu, używając techniki zwanej dynamic time warping, która elastycznie rozciąga i ściska oś czasu, by znaleźć najlepsze dopasowanie. To przypisało każdej komórce „procent cyklu”, działający jak pseudoczas — szacowanie, jak daleko jest w cyklu. Równie ważne było to, że zakres rozciągnięcia czasu potrzebny do dopasowania służy jako sygnał ostrzegawczy: komórki, których przebiegi muszą być silnie zniekształcone, by dopasować się do wzorca, prawdopodobnie zachowują się nieprawidłowo, na przykład przez długie utkwienie w jednej fazie.
Dlaczego to ważne dla zdrowia i chorób
Łącząc wielokanałowe obrazowanie fluorescencyjne z dopasowanymi narzędziami uczenia głębokiego, praca dostarcza kompleksowy pipeline: segmentuje słabe, zaszumione obrazy, etykietuje każde jądro według fazy cyklu, śledzi komórki w czasie i wyłapuje te, które odbiegają od wzorca. Dla osób spoza dziedziny kluczowy wniosek jest taki, że badacze mogą teraz śledzić tysiące żywych komórek bardziej niezawodnie i z mniejszym nakładem ręcznej pracy, nawet przy łagodnych warunkach obrazowania, które chronią zdrowie komórek. Otwiera to drzwi do precyzyjniejszych badań nad tym, jak leki przeciwnowotworowe zatrzymują podziały komórek, jak komórki macierzyste podejmują decyzje o losie oraz jak siły mechaniczne w tkankach wpływają na to, kiedy komórki decydują się dzielić lub zatrzymać.
Cytowanie: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Słowa kluczowe: obrazowanie cyklu komórkowego, mikroskopia oparta na uczeniu głębokim, sensor FUCCI, śledzenie komórek, analiza bioobrazów