Clear Sky Science · it
Analisi bioimmagini per acquisizioni FUCCI multiplexate potenziata dall’apprendimento profondo
Osservare le cellule vivere la loro giornata
Ogni cellula vivente attraversa costantemente fasi di crescita, duplicazione del DNA e divisione. I biologi dispongono oggi di strumenti fluorescenti che fanno brillare in colori diversi queste fasi del ciclo cellulare, permettendo di osservare il processo in tempo reale. Ma quando vengono registrati troppi segnali contemporaneamente, le immagini diventano rumorose e difficili da interpretare—anche per i computer. Questo articolo presenta un metodo basato sull’apprendimento profondo che pulisce questi filmati complessi, traccia le singole cellule e determina in quale fase del ciclo si trova ciascuna, offrendo nuove possibilità per la ricerca sul cancro, gli studi sulle cellule staminali e i test farmacologici.
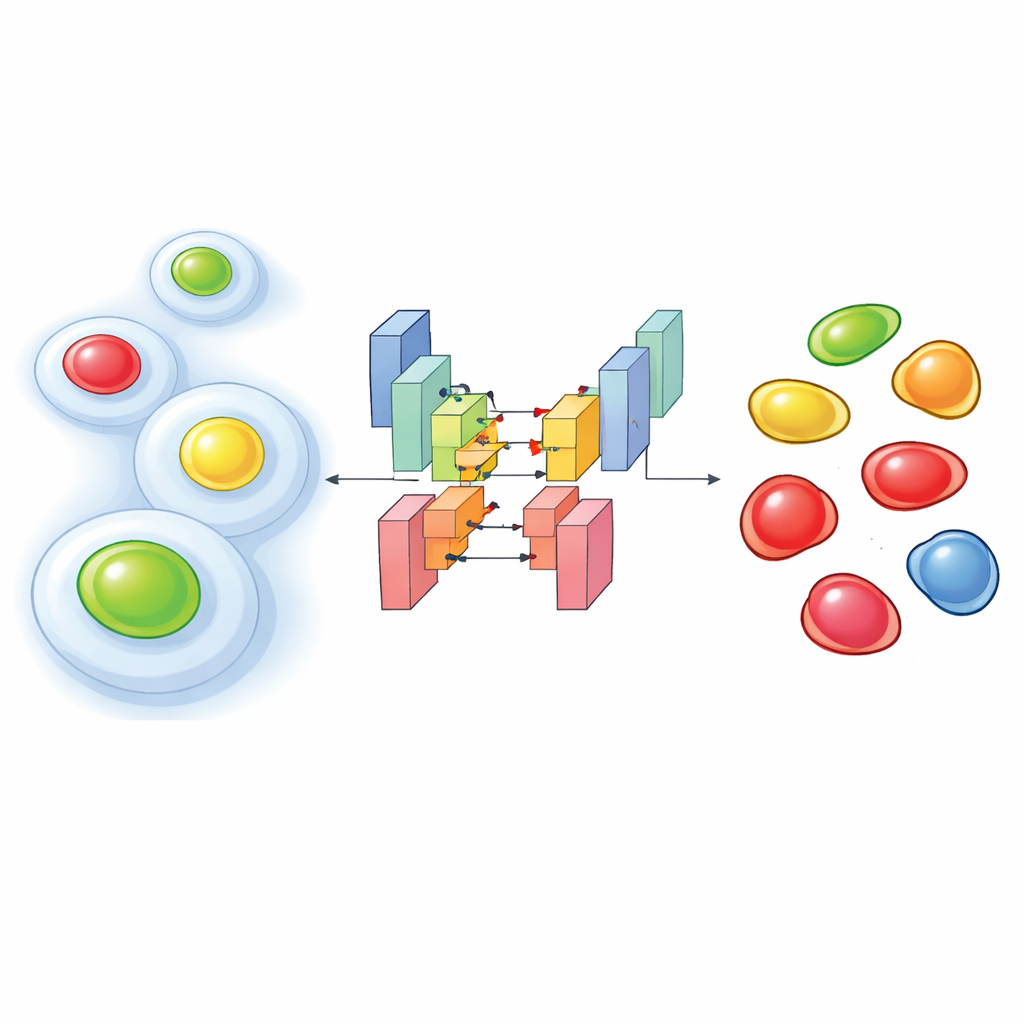
Timer luminosi all’interno delle cellule vive
Per vedere come le cellule progrediscono nel loro ciclo vitale, i ricercatori spesso usano uno strumento molecolare chiamato FUCCI, che fa sì che il nucleo cellulare brilli in un colore nelle fasi iniziali e in un altro colore nelle fasi successive, con combinazioni intermedie. Esperimenti più recenti vanno oltre: registrano FUCCI insieme ad altri marcatori fluorescenti che evidenziano il’impalcatura interna della cellula o altre strutture. Questo “multiplexing” aiuta a collegare ciò che la cellula sta facendo a livello strutturale con il suo stato nel ciclo vitale. Il rovescio della medaglia è che, per non danneggiare le cellule vive, gli scienziati devono illuminarle con moderazione, producendo immagini fioche e rumorose in cui i colori si sovrappongono. In queste condizioni, i software di analisi standard spesso non riescono a individuare correttamente ogni nucleo o ad assegnare la giusta fase del ciclo cellulare.
Insegnare a un algoritmo a vedere oltre il rumore
Gli autori hanno affrontato questo problema addestrando reti di apprendimento profondo personalizzate su migliaia di immagini accuratamente annotate provenienti da due linee cellulari umane. Il loro approccio immette più canali in un modello di segmentazione basato sull’architettura StarDist, particolarmente efficace nel delineare nuclei individuali. Hanno testato tre configurazioni di input: una usando solo il marcatore citoplasmatico (una proteina strutturale etichettata fluorescentemente), una usando soltanto i due colori FUCCI e una che combina tutti e tre. Nonostante le condizioni rumorose, le versioni a due e tre canali hanno raggiunto un’accuratezza molto elevata nell’individuazione dei nuclei, superando nettamente strumenti pre-addestrati popolari quando il segnale era debole. Sorprendentemente, anche il modello che usava solo il marcatore citoplasmatico spesso riusciva a inferire la posizione dei nuclei, perché l’impalcatura circostante lascia un caratteristico “vuoto” dove si trova il nucleo.
Dai puntini colorati alle etichette del ciclo cellulare
Individuare i nuclei è solo metà della sfida; i ricercatori devono anche sapere in quale fase del ciclo cellulare si trova ciascun nucleo. Tradizionalmente, questo si fa impostando soglie di intensità sui colori FUCCI, un metodo semplice che può essere facilmente ingannato dal bleed-through di altri canali. Il gruppo ha esteso la loro rete in modo che non solo delineasse ogni nucleo ma lo etichettasse anche come appartenente a una delle diverse fasi del ciclo cellulare basandosi sui pattern di colore. Confrontando questo approccio con il classico metodo a soglia di intensità, il classificatore basato sull’apprendimento profondo è risultato più accurato, specialmente nei dati rumorosi. Si è perfino generalizzato a una versione diversa del sistema FUCCI proveniente da un altro laboratorio, dopo che gli autori hanno semplicemente rimappato quali combinazioni di colori corrispondono a quali fasi—senza bisogno di riaddestramento.
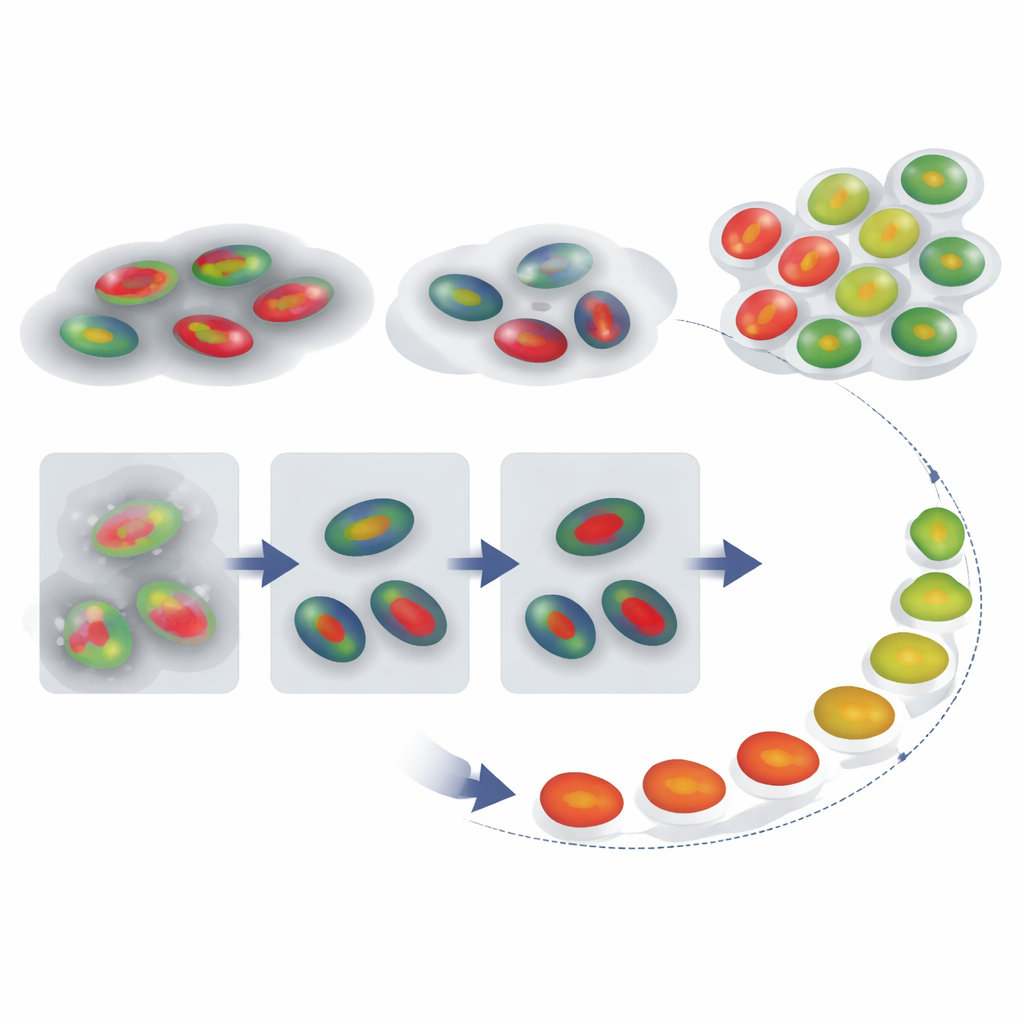
Ricostruire il viaggio temporale di una cellula
Con contorni nucleari affidabili e etichette di fase disponibili, gli autori si sono quindi chiesti se fosse possibile ricostruire come singole cellule percorrono il ciclo nel tempo, anche quando una registrazione non cattura una sequenza completa divisione-divisione. Hanno tracciato i segnali FUCCI di cellule singole e confrontato ogni traccia di intensità con un pattern di riferimento per un ciclo tipico usando una tecnica chiamata dynamic time warping, che allunga e comprime in modo flessibile l’asse temporale per trovare la migliore corrispondenza. Questo ha fornito a ogni cellula una “percentuale del ciclo cellulare” che funge da pseudotempo—una stima di quanto è avanzata. Altrettanto importante, la quantità di deformazione temporale richiesta funziona da segnale d’allarme: le cellule le cui tracce devono essere fortemente distorte per corrispondere al riferimento probabilmente si comportano in modo anomalo, ad esempio restando a lungo bloccate in una fase.
Perché è importante per salute e malattia
Combinando immagini fluorescenti multiplexate con strumenti di apprendimento profondo su misura, questo lavoro offre una pipeline end-to-end: segmenta immagini fioche e rumorose, etichetta ogni nucleo con una fase del ciclo cellulare, traccia le cellule nel tempo e segnala quelle che deviano dal modello standard. Per i non esperti, il messaggio chiave è che i ricercatori possono ora seguire migliaia di cellule vive in modo più affidabile e con meno intervento manuale, anche in condizioni di imaging delicate che preservano la salute cellulare. Ciò apre la strada a studi più precisi su come i farmaci antitumorali arrestano la divisione cellulare, su come le cellule staminali decidono il loro destino e su come le forze meccaniche nei tessuti influenzano il momento in cui le cellule scelgono di dividere o fermarsi.
Citazione: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Parole chiave: immagine del ciclo cellulare, microscopia con apprendimento profondo, sensore FUCCI, tracciamento cellulare, analisi bioimmagini