Clear Sky Science · pt
Análise de bioimagens para aquisições FUCCI multiplexadas potencializadas por aprendizado profundo
Observando as Células Viverem Seu Dia a Dia
Cada célula viva passa continuamente por estágios de crescimento, cópia do DNA e divisão. Biólogos hoje dispõem de ferramentas fluorescentes que fazem esses estágios do ciclo celular brilharem em cores diferentes, permitindo observar esse processo em tempo real. Mas quando muitos sinais são registrados ao mesmo tempo, as imagens ficam ruidosas e difíceis de interpretar — mesmo para computadores. Este artigo apresenta um método baseado em aprendizado profundo que limpa esses filmes complexos, rastreia células individuais e determina em que estágio do ciclo cada uma se encontra, oferecendo novo poder para pesquisas em câncer, estudos com células-tronco e testes de fármacos.
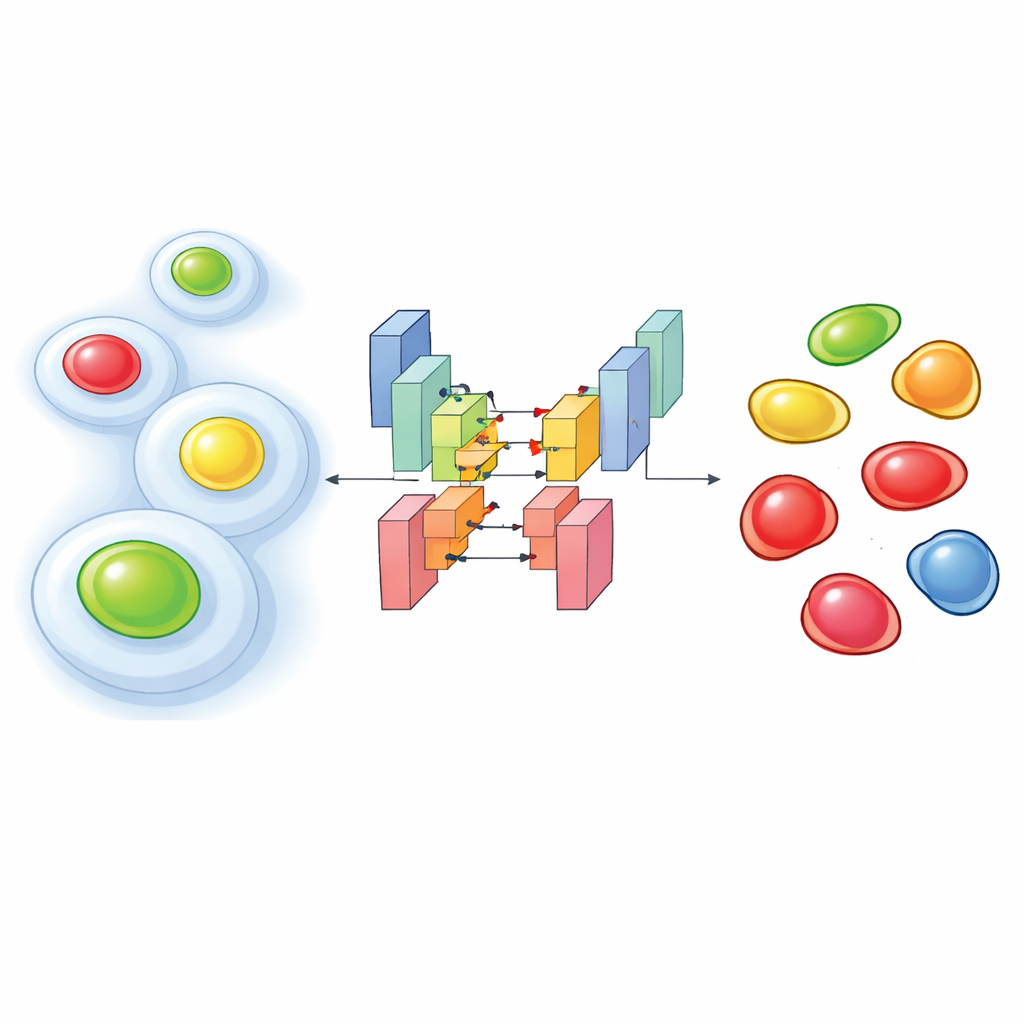
Temporizadores Luminosos Dentro de Células Vivas
Para ver como as células progridem durante seu ciclo de vida, pesquisadores costumam usar uma ferramenta molecular chamada FUCCI, que faz o núcleo celular brilhar em uma cor nos estágios iniciais e em outra cor nos estágios posteriores, com combinações intermediárias. Experimentos mais recentes vão além: gravam o FUCCI junto com marcadores fluorescentes adicionais que destacam o arcabouço interno da célula ou outras estruturas. Essa “multiplexação” ajuda a conectar o que a célula faz estruturalmente com onde ela está no ciclo de vida. A desvantagem é que, para evitar prejudicar células vivas, os cientistas devem iluminá-las com suavidade, o que produz imagens fracas e ruidosas onde as cores se misturam. Nestas condições, softwares padrão de análise de imagem frequentemente falham em localizar corretamente cada núcleo ou em atribuir o estágio correto do ciclo celular.
Ensinando um Algoritmo a Ver Através do Ruído
Os autores enfrentaram esse problema treinando redes de aprendizado profundo personalizadas com milhares de imagens cuidadosamente anotadas de duas linhagens celulares humanas. A abordagem deles alimenta múltiplos canais em um modelo de segmentação baseado na arquitetura StarDist, que é particularmente eficiente em contornar núcleos individuais. Testaram três configurações de entrada: uma usando apenas o marcador citoplasmático (uma proteína estrutural marcada com fluorescência), outra usando somente as duas cores do FUCCI, e uma combinando os três canais. Apesar das condições ruidosas, as versões com dois e três canais alcançaram precisão muito alta na detecção de núcleos, superando claramente ferramentas pré-treinadas populares quando o sinal era fraco. Surpreendentemente, mesmo o modelo que usava apenas o marcador citoplasmático podia frequentemente inferir onde estavam os núcleos, porque o arcabouço circundante deixa um “buraco” característico onde o núcleo se situa.
De Pontos Coloridos a Rótulos do Ciclo Celular
Encontrar núcleos é apenas metade da batalha; os pesquisadores também precisam saber em que estágio do ciclo cada núcleo se encontra. Tradicionalmente, isso é feito definindo limiares de intensidade nas cores do FUCCI, um método simples que pode ser facilmente enganado por sangramento entre canais. A equipe estendeu sua rede para que ela não apenas contornasse cada núcleo, mas também o classificasse como pertencente a uma de várias fases do ciclo celular com base nos padrões de cor. Quando compararam essa abordagem com o método clássico de limiar de intensidade, o classificador por aprendizado profundo foi mais preciso, especialmente em dados ruidosos. Ele até se generalizou para uma versão diferente do sistema FUCCI de outro laboratório, depois que os autores simplesmente remapearam quais combinações de cores correspondiam a quais fases — sem necessidade de novo treinamento.
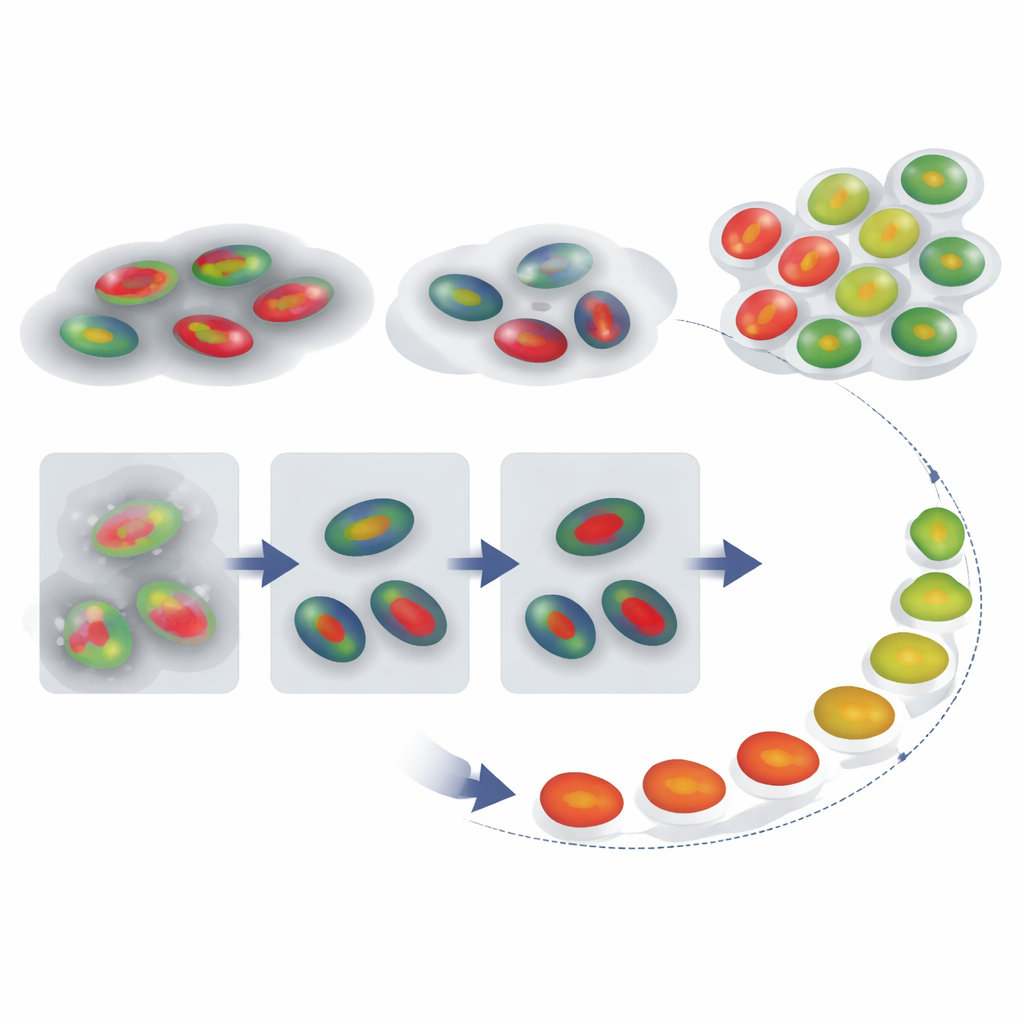
Reconstruindo a Jornada Temporal de uma Célula
Com contornos nucleares e rótulos de fase confiáveis em mãos, os autores perguntaram se era possível reconstruir como células individuais progridem pelo ciclo ao longo do tempo, mesmo quando uma gravação não captura uma sequência completa de divisão a divisão. Eles rastrearam sinais FUCCI de células isoladas e compararam cada traço de intensidade com um padrão de referência para um ciclo típico usando uma técnica chamada dynamic time warping, que estica e comprime flexivelmente o eixo do tempo para encontrar a melhor correspondência. Isso deu a cada célula uma “percentagem do ciclo celular” que funciona como um pseudotempo — uma estimativa de quão avançada ela está. Igualmente importante, a quantidade de esticamento temporal necessária serve como um sinal de alerta: células cujos traços precisam ser fortemente distorcidos para coincidir com a referência provavelmente estão se comportando anormalmente, como células presas por longos períodos em uma fase.
Por Que Isso Importa para Saúde e Doença
Ao combinar imageamento fluorescente multiplexado com ferramentas de aprendizado profundo sob medida, este trabalho entrega um fluxo completo: segmenta imagens fracas e ruidosas, rotula cada núcleo com uma fase do ciclo celular, rastreia células ao longo do tempo e sinaliza aquelas que se desviam de um padrão padrão. Para não especialistas, a mensagem-chave é que os pesquisadores agora podem acompanhar milhares de células vivas com mais confiabilidade e com menos esforço manual, mesmo sob condições de imageamento suaves que preservam a saúde celular. Isso abre caminho para estudos mais precisos de como medicamentos contra o câncer interrompem a divisão celular, como células-tronco decidem seu destino e como forças mecânicas em tecidos influenciam quando as células escolhem dividir-se ou pausar.
Citação: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Palavras-chave: imagem do ciclo celular, microscopia com aprendizado profundo, sensor FUCCI, rastreamento de células, análise de bioimagens