Clear Sky Science · es
Análisis de bioimágenes para adquisiciones FUCCI multiplexadas potenciadas por aprendizaje profundo
Observar a las células vivir su vida cotidiana
Cada célula viva pasa constantemente por fases de crecimiento, replicación del ADN y división. Los biólogos disponen hoy de herramientas fluorescentes que hacen que estas etapas del ciclo celular brillen en distintos colores, lo que permite ver este proceso en tiempo real. Pero cuando se registran demasiadas señales a la vez, las imágenes se vuelven ruidosas y difíciles de interpretar, incluso para los ordenadores. Este artículo presenta un método basado en aprendizaje profundo que limpia estas películas complejas, rastrea células individuales y determina en qué fase del ciclo se encuentra cada una, ofreciendo un nuevo potencial para la investigación del cáncer, los estudios con células madre y las pruebas de fármacos.
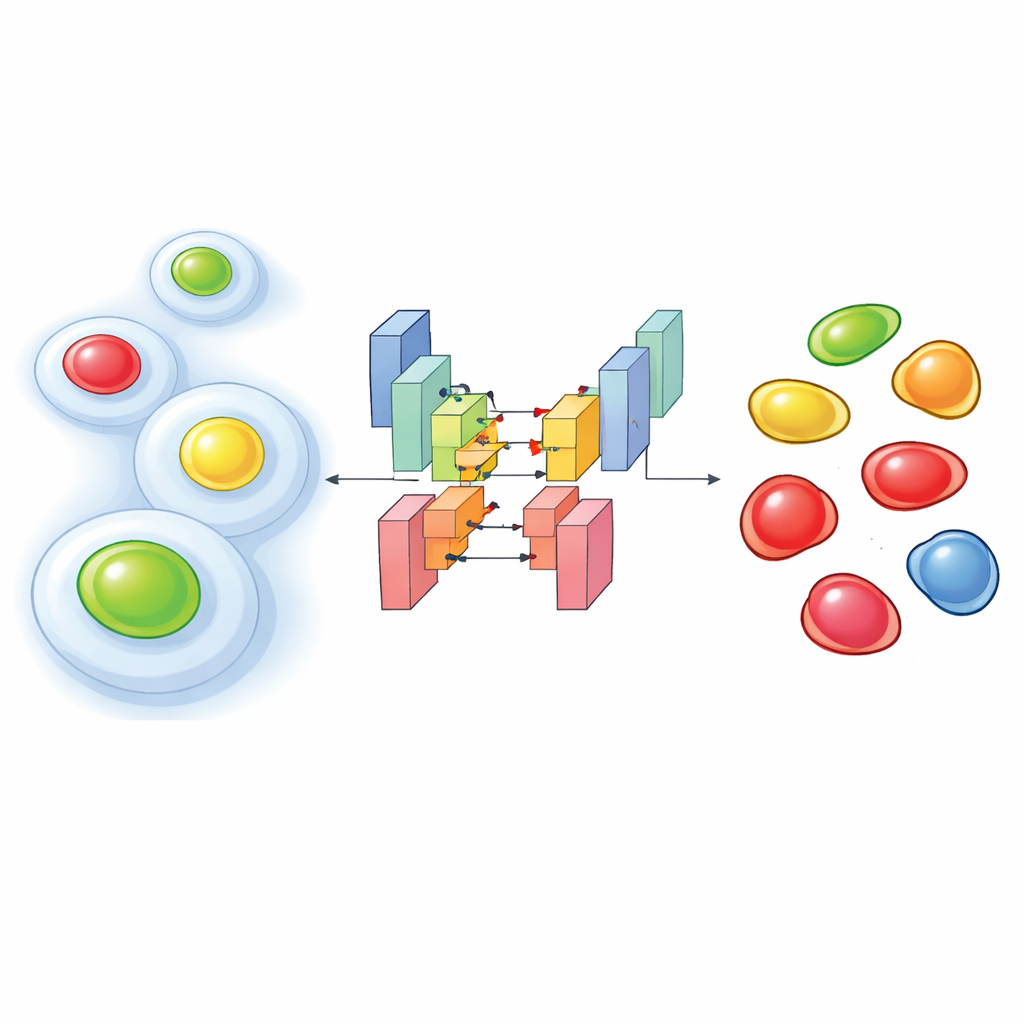
Temporizadores luminosos dentro de células vivas
Para ver cómo progresan las células a lo largo de su ciclo vital, los investigadores suelen usar una herramienta molecular llamada FUCCI, que hace que el núcleo celular brille en un color durante las primeras etapas y en otro color en etapas posteriores, con combinaciones intermedias. Experimentos más recientes van un paso más allá: registran FUCCI junto con marcadores fluorescentes adicionales que resaltan el armazón interno de la célula u otras estructuras. Esta "multiplexación" ayuda a vincular lo que hace estructuralmente una célula con en qué punto de su ciclo se encuentra. La contrapartida es que, para no dañar las células vivas, los científicos deben iluminarlas con suavidad, lo que produce imágenes tenues y ruidosas donde los colores se solapan. En estas condiciones, el software estándar de análisis de imágenes suele fallar al localizar cada núcleo o asignar correctamente la fase del ciclo celular.
Enseñar a un algoritmo a ver a través del ruido
Los autores abordaron este problema entrenando redes de aprendizaje profundo personalizadas con miles de imágenes cuidadosamente anotadas de dos líneas celulares humanas. Su enfoque introduce múltiples canales en un modelo de segmentación basado en la arquitectura StarDist, particularmente eficaz para delinear núcleos individuales. Probaron tres configuraciones de entrada: una usando solo el marcador citoplasmático (una proteína estructural etiquetada con fluorescencia), otra usando solo los dos colores FUCCI y una combinando los tres. A pesar de las condiciones ruidosas, las versiones de dos y tres canales alcanzaron una precisión muy alta en la detección de núcleos, superando claramente a herramientas preentrenadas populares cuando la señal era débil. Sorprendentemente, incluso el modelo que usaba únicamente el marcador citoplasmático a menudo pudo inferir la posición de los núcleos, porque el armazón circundante deja un "vacío" característico donde se sitúa el núcleo.
De puntos coloreados a etiquetas del ciclo celular
Localizar núcleos es solo la mitad de la tarea; los investigadores también necesitan saber en qué fase del ciclo celular se encuentra cada núcleo. Tradicionalmente, esto se hace fijando umbrales de intensidad sobre los colores FUCCI, un método simple que puede verse engañado por el solapamiento de señal entre canales. El equipo amplió su red para que no solo delineara cada núcleo, sino que también lo etiquetara como perteneciente a una de varias fases del ciclo celular según los patrones de color. Al comparar este enfoque con el método clásico de umbral de intensidad, el clasificador por aprendizaje profundo resultó más preciso, especialmente con datos ruidosos. Incluso se generalizó a una versión diferente del sistema FUCCI de otro laboratorio, después de que los autores simplemente reasignaran qué combinaciones de colores correspondían a qué fases—sin necesidad de reentrenamiento.
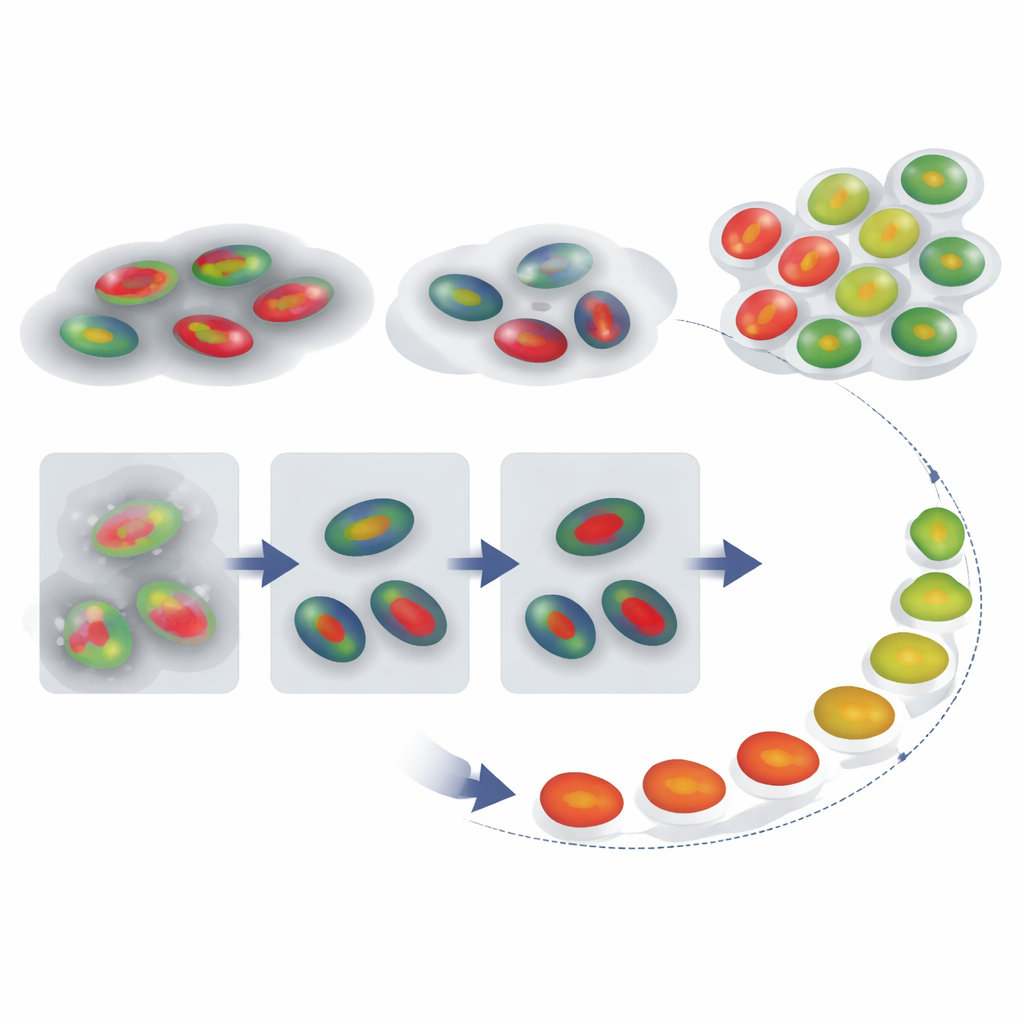
Reconstruir el recorrido temporal de una célula
Con contornos nucleares fiables y etiquetas de fase en mano, los autores se preguntaron si podían reconstruir cómo las células individuales avanzan a través del ciclo en el tiempo, incluso cuando una grabación no captura una secuencia completa de división a división. Rastrearon las señales FUCCI de células individuales y compararon cada traza de intensidad con un patrón de referencia para un ciclo típico usando una técnica llamada dynamic time warping, que estira y comprime de forma flexible el eje temporal para encontrar la mejor coincidencia. Esto proporcionó a cada célula un "porcentaje del ciclo celular" que actúa como un pseudotiempo—una estimación de cuánto ha avanzado. Igualmente importante, la cantidad de estiramiento temporal necesaria sirve como señal de alerta: las células cuyas trazas deben distorsionarse mucho para coincidir con la referencia probablemente se comportan de forma anómala, por ejemplo al quedar estancadas largo tiempo en una fase.
Por qué esto importa para la salud y la enfermedad
Al combinar imágenes fluorescentes multiplexadas con herramientas de aprendizaje profundo a medida, este trabajo ofrece una canalización completa: segmenta imágenes tenues y ruidosas, etiqueta cada núcleo con una fase del ciclo celular, rastrea células en el tiempo y detecta aquellas que se desvían del patrón estándar. Para quienes no son expertos, el mensaje clave es que los investigadores pueden ahora seguir miles de células vivas con mayor fiabilidad y con menos esfuerzo manual, incluso en condiciones de imagen suaves que preservan la salud celular. Esto abre la puerta a estudios más precisos sobre cómo los fármacos contra el cáncer detienen la división celular, cómo las células madre deciden su destino y cómo las fuerzas mecánicas en los tejidos influyen en cuándo las células eligen dividirse o detenerse.
Cita: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Palabras clave: imagen del ciclo celular, microscopía con aprendizaje profundo, sensor FUCCI, seguimiento celular, análisis de bioimágenes