Clear Sky Science · nl
Biobeeldanalyse voor multiplex FUCCI-acquisities aangedreven door deep learning
Cellen live hun dagelijkse leven zien leiden
Elke levende cel doorloopt voortdurend fasen van groei, DNA-replicatie en deling. Biologen hebben nu fluorescerende hulpmiddelen waarmee deze celcyclusfasen in verschillende kleuren oplichten, zodat ze dit proces in realtime kunnen volgen. Maar wanneer te veel signalen tegelijk worden opgenomen, worden de beelden ruisig en moeilijk te interpreteren—even voor computers. Dit artikel introduceert een deep learning–gebaseerde methode die deze complexe films opschoont, individuele cellen volgt en uitleest waar elke cel zich in de cyclus bevindt, waarmee nieuwe mogelijkheden ontstaan voor kankeronderzoek, stamcelstudies en geneesmiddeltesten.
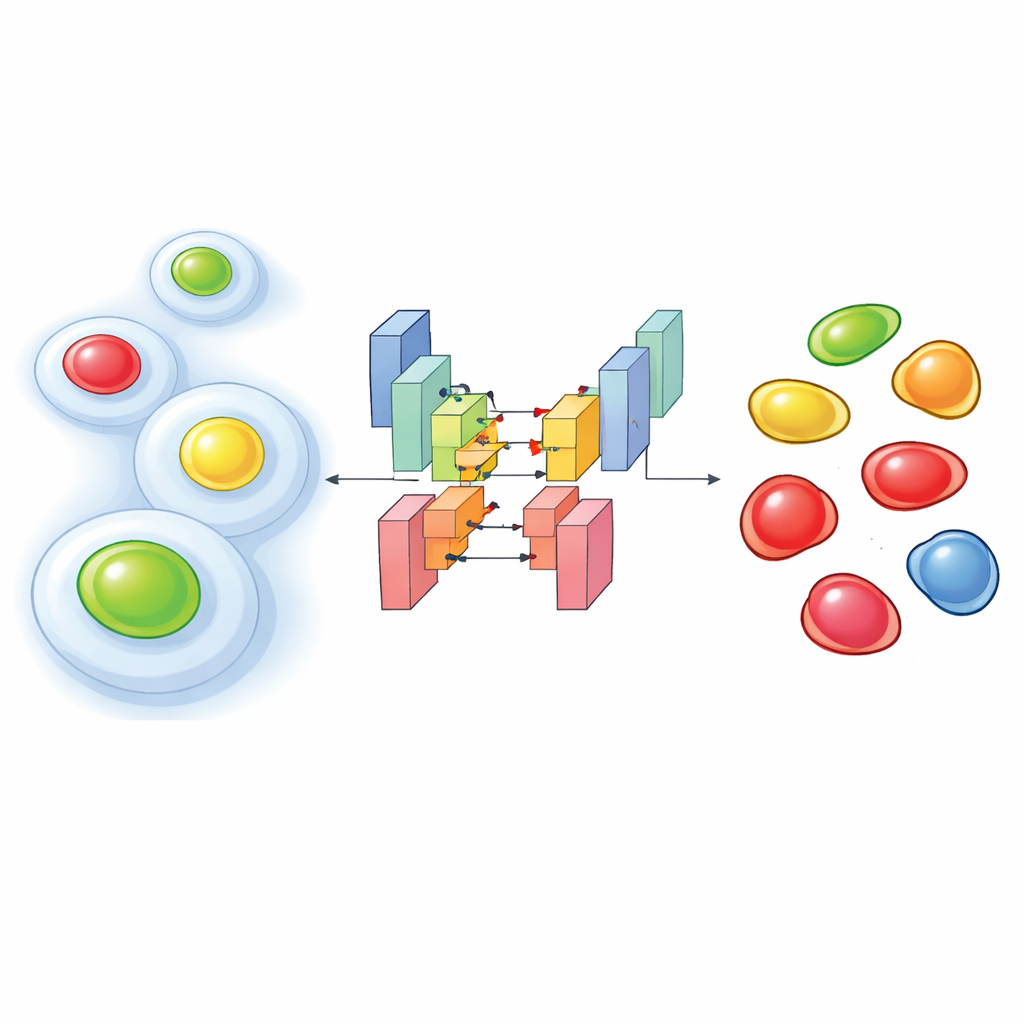
Gloeiende timers in levende cellen
Om te zien hoe cellen zich door hun levenscyclus bewegen, gebruiken onderzoekers vaak een moleculair hulpmiddel genaamd FUCCI, dat de celkern in één kleur laat oplichten tijdens vroege stadia en in een andere kleur later, met tussenvormen ertussen. Nieuwere experimenten gaan een stap verder: ze nemen FUCCI op samen met extra fluorescerende markers die het intracellulaire skelet of andere structuren accentueren. Deze "multiplexing" helpt om te koppelen wat een cel structureel doet aan waar hij zich in zijn levenscyclus bevindt. Het nadeel is dat, om levende cellen niet te beschadigen, onderzoekers ze voorzichtig moeten verlichten, wat resulteert in zwakke, ruisige beelden waarin kleuren in elkaar overlopen. Onder deze omstandigheden faalt standaard beeldanalyse-software vaak in het correct vinden van elke kern of het toewijzen van de juiste celcyclusfase.
Een algoritme leren door de ruis heen te kijken
De auteurs pakten dit probleem aan door aangepaste deep learning-netwerken te trainen op duizenden zorgvuldig geannoteerde beelden van twee humane cellijnen. Hun benadering voedt meerdere kanalen in een segmentatiemodel gebaseerd op de StarDist-architectuur, die bijzonder goed is in het omlijnen van individuele kernen. Ze testten drie inputopstellingen: één met alleen de cytoplasmatische marker (een fluorescent gelabeld structureel eiwit), één met alleen de twee FUCCI-kleuren, en één die alle drie combineert. Ondanks de ruisige omstandigheden bereikten de twee- en drie-kanaalsversies zeer hoge nauwkeurigheid in het vinden van kernen, en overtroffen ze duidelijk populaire vooraf getrainde tools wanneer het signaal zwak was. Verrassend genoeg kon zelfs het model dat alleen de cytoplasmatische marker gebruikte vaak afleiden waar de kernen zaten, omdat het omliggende skelet een kenmerkend "gat" achterlaat waar de kern zich bevindt.
Van gekleurde stippen naar celcycluslabels
Het vinden van kernen is maar de helft van de klus; onderzoekers moeten ook weten in welke fase van de celcyclus elke kern zich bevindt. Traditioneel gebeurt dit door intensiteitsdrempels op de FUCCI-kleuren te zetten, een eenvoudige methode die makkelijk in de war kan raken door overspraak van andere kanalen. Het team breidde hun netwerk uit zodat het niet alleen elke kern omlijnt maar deze ook labelt als behorend tot één van meerdere celcyclusfasen op basis van de kleurpatronen. Wanneer ze deze benadering vergeleken met de klassieke intensiteitsdrempelmethode, was de deep learning-classifier nauwkeuriger, vooral bij ruisige data. Hij generaliseerde zelfs naar een andere versie van het FUCCI-systeem van een ander laboratorium, nadat de auteurs simpelweg de mapping van kleurcombinaties naar fasen hadden aangepast—zonder hertraining.
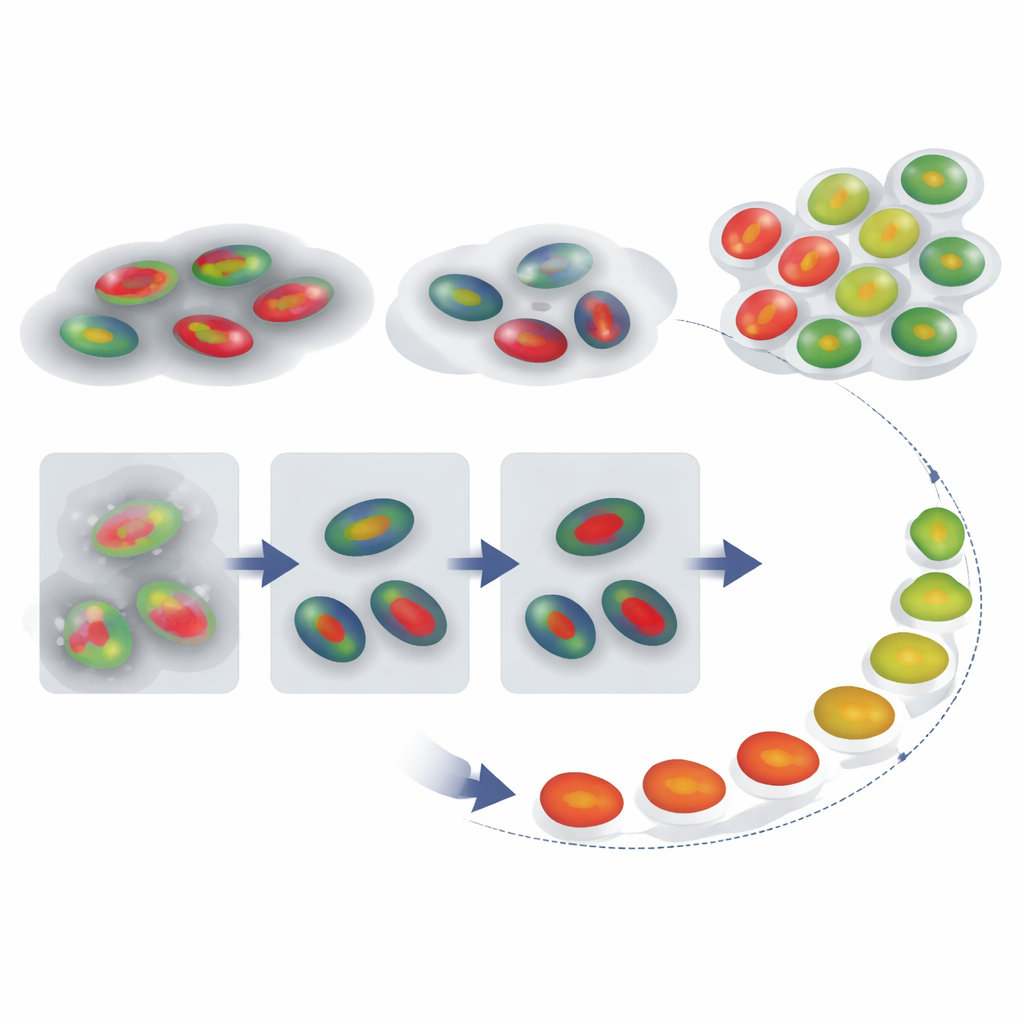
Een celreis door de tijd reconstrueren
Met betrouwbare kernomtrekken en faselabels in handen vroegen de auteurs zich vervolgens af of ze konden reconstrueren hoe individuele cellen zich in de loop van de tijd door de cyclus bewegen, zelfs wanneer een opname geen volledige deling-tot-deling reeks vastlegt. Ze volgden FUCCI-signalen van individuele cellen en vergeleken elke intensiteitstrace met een referentiepatroon voor een typische cyclus met een techniek genaamd dynamic time warping, die flexibel de tijdas uitrekt en comprimeert om de beste overeenkomst te vinden. Dit gaf elke cel een "celcycluspercentage" dat fungeert als een pseudotijd—een schatting van hoe ver de cel gevorderd is. Even belangrijk: de hoeveelheid tijdsvervorming die nodig is, fungeert als een waarschuwingssignaal: cellen waarvan de tracés sterk vervormd moeten worden om met de referentie overeen te komen, vertonen waarschijnlijk abnormaal gedrag, zoals cellen die lange tijd in één fase vastzitten.
Waarom dit belangrijk is voor gezondheid en ziekte
Door multiplex fluorescentiebeeldvorming te combineren met op maat gemaakte deep learning-tools levert dit werk een end-to-end pipeline: het segmenteert zwakke, ruisige beelden, labelt elke kern met een celcyclusfase, volgt cellen in de tijd en markeert diegenen die afwijken van een standaardpatroon. Voor niet-experts is de kernboodschap dat onderzoekers nu duizenden levende cellen betrouwbaarder en met minder handmatig werk kunnen volgen, zelfs onder voorzichtige beeldcondities die de cellen sparen. Dit opent de deur naar nauwkeurigere studies naar hoe kankergeneesmiddelen celdeling stoppen, hoe stamcellen hun lot bepalen, en hoe mechanische krachten in weefsels beïnvloeden wanneer cellen ervoor kiezen te delen of te pauzeren.
Bronvermelding: Zimmermann, J., Pezzotti, M., Torchia, E. et al. Bioimage analysis for multiplexed FUCCI acquisitions powered by deep learning. npj Imaging 4, 27 (2026). https://doi.org/10.1038/s44303-026-00159-6
Trefwoorden: celcyclus beeldvorming, deep learning-microscopie, FUCCI-sensor, celtracking, biobeeldanalyse